|
Size: 31551
Comment:
|
Size: 31662
Comment:
|
| Deletions are marked like this. | Additions are marked like this. |
| Line 3: | Line 3: |
| Allgemeine Worterklärung: Kainatrezeptoren (Kainat = [[http://de.wikipedia.org/wiki/Kainsäure|Kainsäure]] ist der spezifische [[http://de.wikipedia.org/wiki/Agonist_(Anatomie)|Agonist]] dieser [[http://de.wikipedia.org/wiki/Rezeptor|Rezeptoren]]) gehören zu den [[http://de.wikipedia.org/wiki/Glutamatrezeptor|Glutamatrezeptoren]], sie werden häufig im Zusammenhang mit [[http://de.wikipedia.org/wiki/AMPA-Rezeptor|AMPA- Rezeptoren]] erwähnt und stellen trotz ihrer ähnlichen Eigenschaften eine eigene Gruppe von Rezeptoren dar. Kainatrezeptoren können, aufgrund ihres Ionenstroms, in drei Untergruppen eingeteilt werden. Diese Untergruppen sind: schnell [[http://de.wiktionary.org/wiki/desensibilisieren|desensibilisierender]], langsam desensibilisierender und gar nicht desensibilisierender Ionenstrom. (Fahlke et al. 2008)[[#A7|7]] | Allgemeine Worterklärung: Kainatrezeptoren (Kainat = [[http://de.wikipedia.org/wiki/Kainsäure|Kainsäure]] ist der spezifische [[http://de.wikipedia.org/wiki/Agonist_(Anatomie)|Agonist]] dieser [[http://de.wikipedia.org/wiki/Rezeptor|Rezeptoren]]) gehören zu den [[http://de.wikipedia.org/wiki/Glutamatrezeptor|Glutamatrezeptoren]], sie werden häufig im Zusammenhang mit [[http://de.wikipedia.org/wiki/AMPA-Rezeptor|AMPA- Rezeptoren]] erwähnt und stellen trotz ihrer ähnlichen Eigenschaften eine eigene Gruppe von Rezeptoren dar. Kainatrezeptoren können, aufgrund ihres Ionenstroms, in drei Untergruppen eingeteilt werden. Diese Untergruppen sind: schnell [[http://de.wiktionary.org/wiki/desensibilisieren|desensibilisierender]], langsam desensibilisierender und gar nicht desensibilisierender Ionenstrom. (Fahlke et al., 2008)[[#A7|7]] |
| Line 9: | Line 9: |
| Die Non- [[http://de.wikipedia.org/wiki/NMDA|NMDA]] [[http://de.wikipedia.org/wiki/Ionotropie|inotrophen Rezeptoren]] reagieren auf den [[http://de.wikipedia.org/wiki/Neurotransmitter|Neurotransmitter]] [[http://de.wikipedia.org/wiki/Glutamat|Glutamat]] (eine [[http://de.wikipedia.org/wiki/Aminosäure|Aminosäure]]) und werden durch ihn aktiviert. Die Rezeptoren lösen postsynaptisch eine [[http://de.wikipedia.org/wiki/Exzitatorisches_postsynaptisches_Potential|exzitatorische]] Neurotransmission und präsynaptisch eine [[http://de.wikipedia.org/wiki/Inhibition_(Neuron)|inhibierende]] Neurotransmission aus. Allgemein betrachtet, bezeichnet man Glutamat deshalb als exzitatorischen Transmitter. (Horn et al. 2009)[[#A4|4]] Ein Überschuss an Glutamat kann [[http://de.wikipedia.org/wiki/Toxisch|toxisch]] wirken (Glutamatexzitatoxizität). Dem wird durch die Wiederaufnahme des Glutamates in [[http://de.wikipedia.org/wiki/Neuronen|Neuronen]] und [[http://de.wikipedia.org/wiki/Gliazellen|Gliazellen]] (Astrozyten) mit Hilfe von Natrium-abhängigem Aminosäuretransport entgegengewirkt. Generell wirkt das Glutamat auf [[http://de.wikipedia.org/wiki/Ionenkanal|Ionenkanäle]] und metabotroph gekoppelte Rezeptoren. Es spielt eine zentrale Rolle bei Regulation synaptischer Prozesse im [[http://de.wikipedia.org/wiki/Zentralnervensystem|zentralen Nervensystem]]. Unter anderem beteiligt sich das Glutamat an Vorgängen lang anhaltender synaptischer Prozesse (long term potention) im [[http://de.wikipedia.org/wiki/Gehirn|Gehirn]] und [[http://de.wikipedia.org/wiki/Rückenmark|Rückenmark]]. |
Die Non- [[http://de.wikipedia.org/wiki/NMDA|NMDA]] [[http://de.wikipedia.org/wiki/Ionotropie|inotrophen Rezeptoren]] reagieren auf den [[http://de.wikipedia.org/wiki/Neurotransmitter|Neurotransmitter]] [[http://de.wikipedia.org/wiki/Glutamat|Glutamat]] (eine [[http://de.wikipedia.org/wiki/Aminosäure|Aminosäure]]) und werden durch ihn aktiviert. Die Rezeptoren lösen postsynaptisch eine [[http://de.wikipedia.org/wiki/Exzitatorisches_postsynaptisches_Potential|exzitatorische]] Neurotransmission und präsynaptisch eine [[http://de.wikipedia.org/wiki/Inhibition_(Neuron)|inhibierende]] Neurotransmission aus. Allgemein betrachtet, bezeichnet man Glutamat deshalb als exzitatorischen Transmitter. (Horn et al., 2009) [[#A4|4]] Ein Überschuss an Glutamat kann [[http://de.wikipedia.org/wiki/Toxisch|toxisch]] wirken (Glutamatexzitatoxizität). Dem wird durch die Wiederaufnahme des Glutamates in [[http://de.wikipedia.org/wiki/Neuronen|Neuronen]] und [[http://de.wikipedia.org/wiki/Gliazellen|Gliazellen]] (Astrozyten) mit Hilfe von Natrium-abhängigem Aminosäuretransport entgegengewirkt. Generell wirkt das Glutamat auf [[http://de.wikipedia.org/wiki/Ionenkanal|Ionenkanäle]] und metabotroph gekoppelte Rezeptoren. Es spielt eine zentrale Rolle bei Regulation synaptischer Prozesse im [[http://de.wikipedia.org/wiki/Zentralnervensystem|zentralen Nervensystem]]. Unter anderem beteiligt sich das Glutamat an Mechanismen lang anhaltender synaptischer Prozesse (long term potention) im [[http://de.wikipedia.org/wiki/Gehirn|Gehirn]] und [[http://de.wikipedia.org/wiki/Rückenmark|Rückenmark]]. |
| Line 14: | Line 14: |
| Spezifische [[http://de.wikipedia.org/wiki/Botenstoff|Mediatoren]] des exzitatorischen Neurotransmittersystems spielen eine wichtige Rolle bei [[http://de.wikipedia.org/wiki/Neurodegenerative_Erkrankung|Neurodegenerativen Erkrankungen]]. Durch Veränderungen an den Kainatrezeptoren z. B. durch [[http://de.wikipedia.org/wiki/Punktmutation|Punktmutationen]] können folgenschwere Defekte entstehen, welche zu folgenden Krankheitsbildern führen: | Spezifische [[http://de.wikipedia.org/wiki/Botenstoff|Mediatoren]] des exzitatorischen Neurotransmittersystems spielen eine wichtige Rolle bei [[http://de.wikipedia.org/wiki/Neurodegenerative_Erkrankung|Neurodegenerativen Erkrankungen]].Veränderungen an den Kainatrezeptoren z. B. durch [[http://de.wikipedia.org/wiki/Punktmutation|Punktmutationen]] können folgenschwere Defekte verursachen, welche unter Anderem zu folgenden Krankheitsbildern führen: |
| Line 37: | Line 37: |
| Das [[http://de.wikipedia.org/wiki/Langzeit-Potenzierung|LTP]] (long term potention) ist der Hauptmechanismus für die Speicherung von erlernten [[http://de.wikipedia.org/wiki/Fähigkeiten|Fähigkeiten]] im [[http://de.wikipedia.org/wiki/Gehirn|Gehirn]], besonders deutlich wird dieser Prozess der Speicherung an den [[http://de.wikipedia.org/wiki/Pyramidenzelle|Pyramidalzellen]] des [[http://de.wikipedia.org/wiki/Hippocampus|Hypokampus]]. Dieser Mechanismus steht durch wiederholte Aktivierung der glutamatergen zentralen Synapsen mit der Amplitudenzunahme des [[http://de.wikipedia.org/wiki/EPSP|EPSP]]´s (Exzitatiorisches Postsynaptisches Potential) in Verbindung. Dies ist die einfachste Gedächtnisform, welche auch als Engrammbildung (Eingravieren von Lerninhalten) bezeichnet wird. Durch Wiederholen des gelernten Musters kommt es zur Konsolidierung des Gedächtnisinhaltes. So entstehen zum Beispiel auch chronische Schmerzzustände, diese werden durch anhaltende Übererregung der [[http://de.wikipedia.org/wiki/Nozizeption|nocizeptiven]] Neuronen ausgelöst. Damit ist die Beteiligung der Kainatrezeptoren an kognitiven Funktionen im Gehirn wie [[http://de.wikipedia.org/wiki/Gedächtnis|Gedächtnis]] und [[http://de.wikipedia.org/wiki/Lernen|Lernen]] bewiesen. (Leuschner W. D, 1998) [[#A9|9]] | Das [[http://de.wikipedia.org/wiki/Langzeit-Potenzierung|LTP]] (long term potention) ist der Hauptmechanismus für die Speicherung von erlernten [[http://de.wikipedia.org/wiki/Fähigkeiten|Fähigkeiten]] im [[http://de.wikipedia.org/wiki/Gehirn|Gehirn]]. Hauptwirkungsort dieses Prozesses sind die [[http://de.wikipedia.org/wiki/Pyramidenzelle|Pyramidalzellen]] des [[http://de.wikipedia.org/wiki/Hippocampus|Hypokampus]]. Das LTP steht durch wiederholte Aktivierung der glutamatergen zentralen Synapsen mit der Amplitudenzunahme des [[http://de.wikipedia.org/wiki/EPSP|EPSP]]´s (Exzitatiorisches Postsynaptisches Potential) in Verbindung. Dieser, als einfachste Form der Gedächtnisbildung, bekannte Mechanismus wird als Engrammbildung (Eingravieren von Lerninhalten) bezeichnet. <<BR>> Durch Wiederholen des gelernten Musters kommt es zur Konsolidierung des Gedächtnisinhaltes. So entstehen zum Beispiel auch chronische Schmerzzustände, diese werden durch anhaltende Übererregung der [[http://de.wikipedia.org/wiki/Nozizeption|nocizeptiven]] Neuronen ausgelöst. <<BR>>Damit ist die Beteiligung der Kainatrezeptoren an kognitiven Funktionen im Gehirn wie [[http://de.wikipedia.org/wiki/Gedächtnis|Gedächtnis]] und [[http://de.wikipedia.org/wiki/Lernen|Lernen]] bewiesen. (Leuschner W. D, 1998) [[#A9|9]] |
| Line 116: | Line 116: |
| Für kognitive Vorgänge relevante Kainatrezeptoren sind in jenen Gehirnarealen vermehrt vorhanden, deren Funktion der Lern- und Gedächtnisverarbeitung zugeschrieben wird (z.B. Hippocampus). (Horn et al. 2009) [[#A4|4]] Diejenigen, die für [[http://de.wikipedia.org/wiki/Motorik|Motorik]] und Bewegungsmotivation zuständig sind, kommen dagegen vermehrt in [[http://de.wikipedia.org/wiki/Basalganglien|Basalganglien]] und dem [[http://de.wikipedia.org/wiki/Kleinhirn|Kleinhirn]] vor. <<BR>>Die Kainatrezeptoren spielen eine wichtige Rolle bei der synaptischen Übertragung und haben eine langsamere Kinetik als [[http://de.wikipedia.org/wiki/AMPA-Rezeptor|AMPA- Rezeptoren]]. [[#A16|16]] <<BR>>Im Ruhezustand bzw. ohne Reizung ist die Kalziumionen permeabilität sehr gering, sie kann sich jedoch durch die Zusammensetzung der Untereinheiten oder [[http://de.wikipedia.org/wiki/RNA-Editing|RNA Editing]] erhöhen. Durch Kalziumionen Einstrom kommt es zu einer Depolarisation der Zellmembran und in Folge dessen zu einem Aktionspotential. Eine zu hohe oder zu lange andauernde Kalziumkonzentration kann zum [[http://de.wikipedia.org/wiki/Zelltod|Tod der Zelle]] führen. <<BR>>Durch die Erhöhung des Kalziumionen- Spiegels im Inneren der Zelle werden die [[http://de.wikipedia.org/wiki/Mitochondrien|Mitochondrien]] in ein höheres Aktivitätslevel gebracht. Allerdings kann es durch eine länger anhaltende Konzentrationserhöhung von Kalziumionen zu einer Gewöhnung [[http://de.wikipedia.org/wiki/Habituation|(Habituation)]] der Mitochondrienmembran kommen. Es bildet sich in Folge dessen keine signifikante Differenz zum Ruhezustand im Falle einer Reizung. | Für kognitive Vorgänge relevante Kainatrezeptoren sind in jenen Gehirnarealen vermehrt vorhanden, deren Funktion der Lern- und Gedächtnisverarbeitung zugeschrieben wird (z.B. Hippocampus). (Horn et al. 2009) [[#A4|4]] Diejenigen, die für [[http://de.wikipedia.org/wiki/Motorik|Motorik]] und Bewegungsmotivation zuständig sind, kommen dagegen vermehrt in [[http://de.wikipedia.org/wiki/Basalganglien|Basalganglien]] und dem [[http://de.wikipedia.org/wiki/Kleinhirn|Kleinhirn]] vor. <<BR>>Die Kainatrezeptoren spielen eine wichtige Rolle bei der synaptischen Übertragung und haben eine langsamere Kinetik als [[http://de.wikipedia.org/wiki/AMPA-Rezeptor|AMPA- Rezeptoren]]. [[#A16|16]] <<BR>>Im Ruhezustand bzw. ohne Reizung ist die Kalziumionen permeabilität sehr gering, sie kann sich jedoch durch die Zusammensetzung der Untereinheiten oder [[http://de.wikipedia.org/wiki/RNA-Editing|RNA Editing]] erhöhen. Durch Kalziumionen Einstrom kommt es zu einer Depolarisation der Zellmembran und in Folge dessen zu einem Aktionspotential. Eine zu hohe oder zu lange andauernde Kalziumkonzentration kann zum [[http://de.wikipedia.org/wiki/Zelltod|Tod der Zelle]] führen. <<BR>>Durch die Erhöhung des Kalziumionen- Spiegels im Inneren der [[http://de.wikipedia.org/wiki/Zelle_%28Biologie%29|Zelle]] werden die [[http://de.wikipedia.org/wiki/Mitochondrien|Mitochondrien]] in ein höheres Aktivitätslevel gebracht. Allerdings kann es durch eine länger anhaltende Konzentrationserhöhung von Kalziumionen zu einer Gewöhnung [[http://de.wikipedia.org/wiki/Habituation|(Habituation)]] der Mitochondrienmembran kommen. Es bildet sich in Folge dessen keine signifikante Differenz zum Ruhezustand im Falle einer [[http://de.wikipedia.org/wiki/Reizung|Reizung]]. |
Kainatrezeptoren
Allgemeine Worterklärung: Kainatrezeptoren (Kainat = Kainsäure ist der spezifische Agonist dieser Rezeptoren) gehören zu den Glutamatrezeptoren, sie werden häufig im Zusammenhang mit AMPA- Rezeptoren erwähnt und stellen trotz ihrer ähnlichen Eigenschaften eine eigene Gruppe von Rezeptoren dar. Kainatrezeptoren können, aufgrund ihres Ionenstroms, in drei Untergruppen eingeteilt werden. Diese Untergruppen sind: schnell desensibilisierender, langsam desensibilisierender und gar nicht desensibilisierender Ionenstrom. (Fahlke et al., 2008)7
Contents
Glutamatrezeptoren allgemein
Die Non- NMDA inotrophen Rezeptoren reagieren auf den Neurotransmitter Glutamat (eine Aminosäure) und werden durch ihn aktiviert. Die Rezeptoren lösen postsynaptisch eine exzitatorische Neurotransmission und präsynaptisch eine inhibierende Neurotransmission aus. Allgemein betrachtet, bezeichnet man Glutamat deshalb als exzitatorischen Transmitter. (Horn et al., 2009) 4
Ein Überschuss an Glutamat kann toxisch wirken (Glutamatexzitatoxizität). Dem wird durch die Wiederaufnahme des Glutamates in Neuronen und Gliazellen (Astrozyten) mit Hilfe von Natrium-abhängigem Aminosäuretransport entgegengewirkt. Generell wirkt das Glutamat auf Ionenkanäle und metabotroph gekoppelte Rezeptoren. Es spielt eine zentrale Rolle bei Regulation synaptischer Prozesse im zentralen Nervensystem. Unter anderem beteiligt sich das Glutamat an Mechanismen lang anhaltender synaptischer Prozesse (long term potention) im Gehirn und Rückenmark.
Das Exzitatorische Neurotransmittersystem
Spezifische Mediatoren des exzitatorischen Neurotransmittersystems spielen eine wichtige Rolle bei Neurodegenerativen Erkrankungen.Veränderungen an den Kainatrezeptoren z. B. durch Punktmutationen können folgenschwere Defekte verursachen, welche unter Anderem zu folgenden Krankheitsbildern führen:
Long Term Potention
Das LTP (long term potention) ist der Hauptmechanismus für die Speicherung von erlernten Fähigkeiten im Gehirn. Hauptwirkungsort dieses Prozesses sind die Pyramidalzellen des Hypokampus. Das LTP steht durch wiederholte Aktivierung der glutamatergen zentralen Synapsen mit der Amplitudenzunahme des EPSP´s (Exzitatiorisches Postsynaptisches Potential) in Verbindung. Dieser, als einfachste Form der Gedächtnisbildung, bekannte Mechanismus wird als Engrammbildung (Eingravieren von Lerninhalten) bezeichnet.
Durch Wiederholen des gelernten Musters kommt es zur Konsolidierung des Gedächtnisinhaltes. So entstehen zum Beispiel auch chronische Schmerzzustände, diese werden durch anhaltende Übererregung der nocizeptiven Neuronen ausgelöst.
Damit ist die Beteiligung der Kainatrezeptoren an kognitiven Funktionen im Gehirn wie Gedächtnis und Lernen bewiesen. (Leuschner W. D, 1998) 9
Einteilung
Glutamatrezeptoren werden in inotrophe und metabotrophe Rezeptoren eingeteilt. Unterschieden werden diese aufgrund ihrer Agonisten.
Inotrophe Glutamatrezeptoren werden in nicht- NMDA-, NMDA-, Waisen-Rezeptoren und Kainatbindende Proteine unterteilt.
Metabotrophe Glutamatrezeptoren werden in PI/Ca- und cAMP- gekoppelte Rezeptoren unterteilt.10
Kainatrezeptoren sind in allen prä- und postsynaptischen Membranen des zentralen Nervensystems zu finden.
AMPA- Rezeptoren und Kainatrezeptoren sind in der gleichen Region, jedoch nie in derselben Synapse zu finden.(Leuschner W. D, 1998) 9 (Abbildung 1 zeigt die NMDA- Rezeptoren in aktivierter Form und in verschiedenen Formen der Hemmung) 17
Inotrophe Glutamatrezeptoren
Nicht NMDA – Rezeptoren
- AMPA – Rezeptoren: GluR 1-4
- Kainat – Rezeptoren
- Niederaffine: GluR 5-7
- Hochaffine: KA 1-2
NMDA – Rezeptoren
- NR1
- NR2 A- D
- NR3 A und B
Waisen – Rezeptoren
kainatbinde Proteine
- KBP – frog, - chick, - fish-a, -fish-b, - toad
Metabotrophe Glutamatrezeptoren
PI/Ca – gekoppelt
- mGluR 1 und mGluR 5
cAMP – gekoppelt
- tACPD- Rezeptoren
- mGluR 2 und 3
- AP4- Rezeptor
- mGluR 4, 6, 7, 8
Kainatrezeptoren
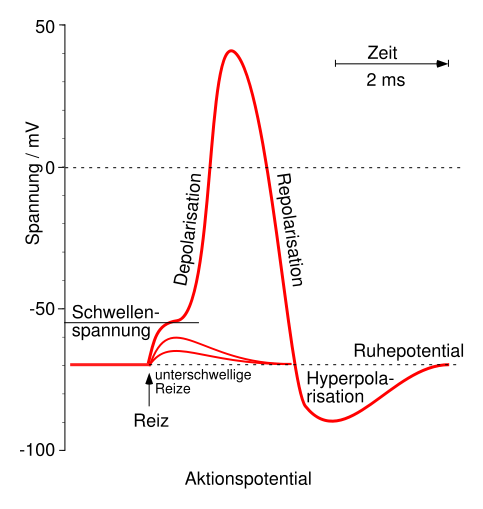
Während der Ontogenese des Gehirns entwickeln sich Kainatrezeptoren durch neuronale Aktivität. Sie sind Kationenkanäle mit einer schnellen Kinetik, welche für Natrium-, Kalium- Ionen und Wasser permeabel, für Calciumionen jedoch impermeabel sind. Im Ruhezustand sind die Kainatrezeptoren durch Magnesium- Ionen blockiert. Durch Freisetzung der, an den Rezeptor gebundenen Magnesiumionen infolge einer Depolarisation wird diese Blockade aufgehoben. (Abbildung 3 zeigt den Verlauf eines Aktionspotentials)18
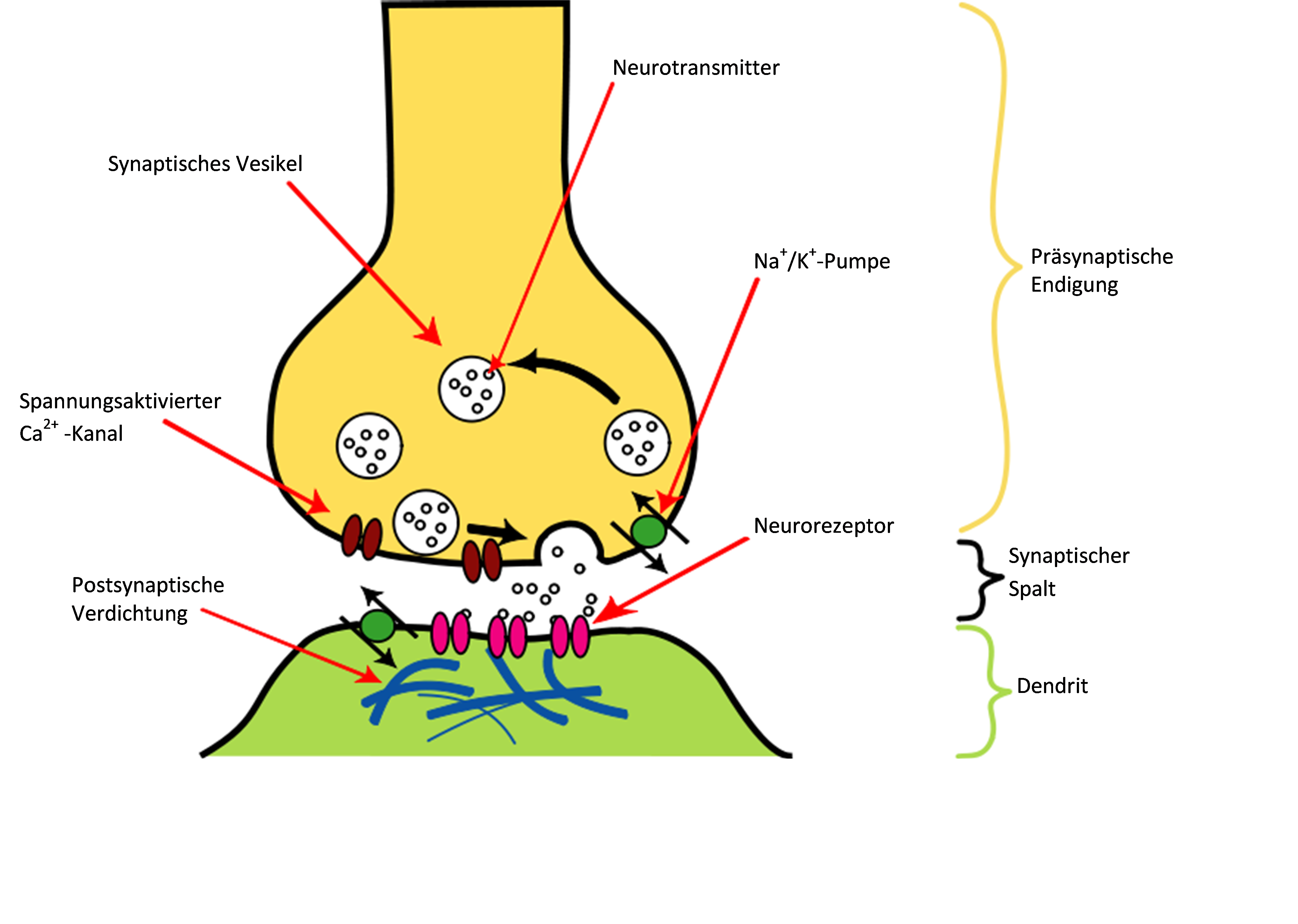
Allgemein bewirken Kainatrezeptoren eine schnelle Depolarisation an gluterminergen Synapsen. (Abbildung 2 zeigt eine Synapse mit ihrer chemischen Funktion)19 Die Depolarisation der Synapsen ist eine Folge der gesteigerten Permeabilität von Calcium- und Natriumionen.
Die Kainatrezeptoren lassen sich entsprechend ihrer Untereinheiten in niederaffine und hochaffine Gruppen einteilen. So wie die Glutamatrezeptoren, kommen auch Kainatrezeptoren überall im zentralen Nervensystem vor. (Horn et al. 2009) 4 Durch Öffnen des Ionenkanals der Kainatrezeptoren entsteht ein exzitatiorisches postsynaptisches Potential (EPSP), zusätzlich modulieren sie die Neurotransmitterfreisetzung durch präsynaptische Mechanismen. Diese Rezeptoren sind mittels Glutamat, Kainat, Domoat sowie Quisqualat aktivierbar und binden diese. Ihre Aufgabe ist unter anderem die Übertragung von Hitzeempfindung und Schmerz von der Peripherie zum Gehirn sowie die Vermittlung der synaptischen Transmission zwischen den Photorezeptoren und den "off-Bipolarzellen" der Retina. Eine Besonderheit der Kainatrezeptoren ist, dass sie nicht nur durch ihre Agonisten, sondern auch durch andere erregende Synapsen oder ein rückläufiges Aktionspotential aktiviert werden können.
Postsynaptische Kainatrezeptoren
Postsynaptische Kainatrezeptoren sind im Hypokampus, im Rückenmark, im somatosensorischen Cortex, im Cerebellum und dem medialen Cortex zu finden. Die Moosfasern CA 3 im Hypokampus (nicht zu verwechseln mit den Moosfasern des Kleinhirns) sind die am meisten untersuchten neuronalen Fasern im Zusammenhang mit der Funktion der Kainatrezeptoren. 16 Bei Stimulation lösen die postsynaptischen Kainatrezeptoren ein langsames EPSP aus.
Präsynaptische Kainatrezeptoren
Präsynaptische Kainatrezeptoren kommen vermehrt im Hypokampus vor. Ihre Hauptfunktion ist die Beeinflussung der Präsynaptischen- Terminale. Sie vereinfachen die AMPA- und NMDA- Rezeptoren abhängige Transmission an den Moosfasern CA 3. Eine geringe Kainatkonzentration ermöglicht, genauso wie eine "Frequenz- Erleichterung", ausgelöst durch kleine elektronische Schocks, eine vereinfachte Transmission. Die präsynaptischen Kainatrezeptoren sind mit verantwortlich für das Entstehen von Langzeit- Potenzierung der Moosfasern des Hypokampus. Typisch für den präsynaptischen Kainatrezeptor ist die positive "Feedback-Schleife". Die Aktivität der Rezeptoren wird durch die Freisetzung von Glutamat gesteigert, dadurch wiederum steigert sich die synaptische Transmission und führt so erneut zu einer Stimulation der Aktivität der Rezeptoren.16
Struktur / Untereinheiten
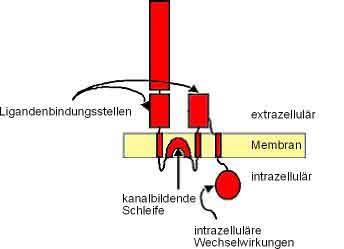
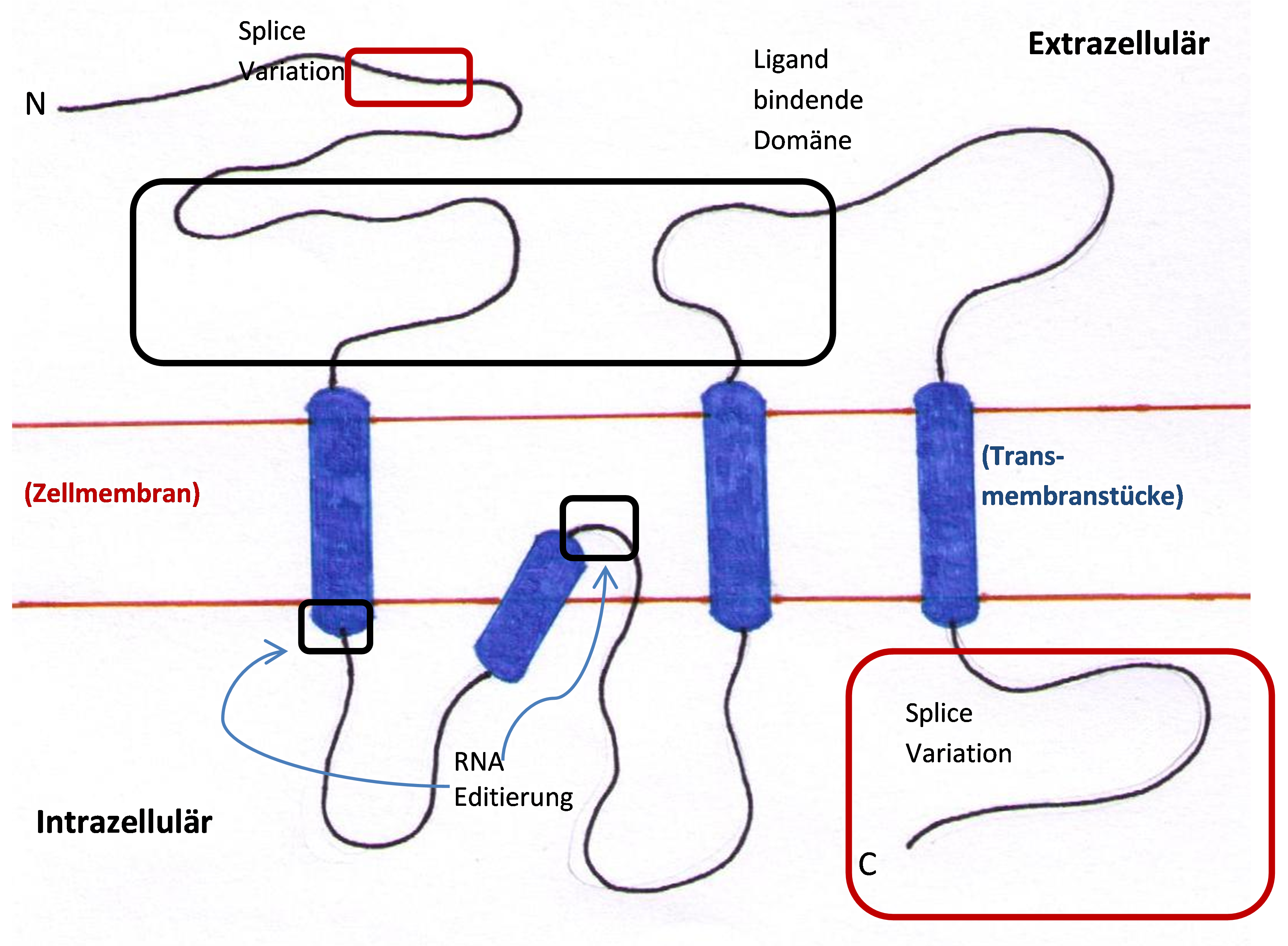
Der Kainatrezeptor besteht aus fünf Untereinheiten. Diese sind GluR 5, 6 und 7, sowie KA 1 und 2. 16 Die Untereinheiten GluR 5, 6 und 7 kommen in heteromerer und homomerer Anordnung vor. Wohingegen KA 1 und 2 nur in Kombination mit GluR 5 und 6 einen funktionellen Heterokomplex bilden können. Außerhalb dieses Komplexes haben sie keine Ionenkanalfunktion. Die Untereinheiten können in verschiedenen Variationen angeordnet werden, jede Variation stellt einen neuen und spezifischen Charakter der Kainatrezeptoren dar. 10 Jede Untereinheit besteht aus verschieden Domains, welche sich wiederum aus mehreren Polypeptidketten zusammensetzen. Sie beginnen mit 400 N- terminalen Aminosäuren außerhalb der Zellmembran und bildet damit das Segment Eins (S1), welches die Ligandenbindungsstelle formt. S1 bildet dann das Transmembranstück (M1). M1 tritt durch die Zellmembran auf die intrazelluläre Seite und wird zu M2. M2 drückt sich durch die Zellmembran halb durch und kehrt dann wieder zurück ins Zytoplasma, so entsteht der "P-loop". Diese Schleife, ähnlich der des AMPA-Rezeptors (Abbildung 4 zeigt ein Schema der Untereinheiten des AMPA-Rezeptors) 20 ist bestimmend für die Calciumpermeabilität des Rezeptors. Auf der intrazellulären Seite wird M2 zu M3 und M3 tritt auf die extrazelluläre Seite. M3 bildet dort S2. Dies ist die zweite Ligandenbindungsstelle der Untereinheit. Aus S2 wird M4, welche wieder die Membran zur intrazellulären Seite durchzieht. M4 kann auch als C- terminales Ende des Proteins angesehen werden. Durch die Unterschiede an der dritten Membran differenzieren sich die Untereinheiten GluR 6 und 7. (Abbildung 5 Struktur eines Kainatrezeptors) 21 16
|
GluR 5,6 und 7 sind niederaffine Untereinheiten. Ihr KD- Wert für Kainat liegt bei:
- GluR 5 = 70nM
- GluR 6 = 95nM
- GluR 7 = 77nM
KA1 und KA2 sind hochaffine Untereinheiten. Ihr KD- Wert für Kainat liegt bei:
- KA1 = 4,7nM
- KA2 = 15 nM
Die Untereinheiten GluR 7 weisen in HEK- 293- Zellen (HEK = Human Embrionic Kidneycells) Ionenkanalfunktionen auf. Es können Punktmutationen in der dritten Membran auftreten, welche die Funktion der Kainatrezeptoren erheblich beeinflussen. GluR 7 stellt keinen wirklich funktionellen Rezeptor dar, lediglich einen Kanal mit geringer Porenöffnung. GluR 6 und 7 werden im Gehirn an ähnlicher Stelle exprimiert. Wenn GluR 6 mit GluR 7 in heteromerer Form exprimiert wird, hat GluR 7 eine negativ modulierende Wirkung auf den ganzen Kainatrezeptor.
Funktion/ Funktionsweise
Für kognitive Vorgänge relevante Kainatrezeptoren sind in jenen Gehirnarealen vermehrt vorhanden, deren Funktion der Lern- und Gedächtnisverarbeitung zugeschrieben wird (z.B. Hippocampus). (Horn et al. 2009) 4 Diejenigen, die für Motorik und Bewegungsmotivation zuständig sind, kommen dagegen vermehrt in Basalganglien und dem Kleinhirn vor.
Die Kainatrezeptoren spielen eine wichtige Rolle bei der synaptischen Übertragung und haben eine langsamere Kinetik als AMPA- Rezeptoren. 16
Im Ruhezustand bzw. ohne Reizung ist die Kalziumionen permeabilität sehr gering, sie kann sich jedoch durch die Zusammensetzung der Untereinheiten oder RNA Editing erhöhen. Durch Kalziumionen Einstrom kommt es zu einer Depolarisation der Zellmembran und in Folge dessen zu einem Aktionspotential. Eine zu hohe oder zu lange andauernde Kalziumkonzentration kann zum Tod der Zelle führen.
Durch die Erhöhung des Kalziumionen- Spiegels im Inneren der Zelle werden die Mitochondrien in ein höheres Aktivitätslevel gebracht. Allerdings kann es durch eine länger anhaltende Konzentrationserhöhung von Kalziumionen zu einer Gewöhnung (Habituation) der Mitochondrienmembran kommen. Es bildet sich in Folge dessen keine signifikante Differenz zum Ruhezustand im Falle einer Reizung.
Aufgabe der Kainatrezeptoren
Kainatrezeptoren befinden sich in prä- und postsynaptischen Neuronen. Ihre Funktion ist im Zusammenhang mit AMPA- und NMDA- Rezeptoren bisher nicht geklärt. 7 Ihre sensorische Transduktion steht in engem Zusammenhang mit der Epilepsie. Die Kainatrezeptoren in den präsynaptischen Zellen beeinflussen die Menge der freigesetzten Neurotransmitter. Man unterscheidet zwischen schneller, langsamer und additiver Wirkung. Photorezeptoren nutzen den Neurotransmitter Glutamat um mit anderen Zellen zu kommunizieren. So wird zum Beispiel im Dunkeln Glutamat an den postsynaptischen Kainatrezeptoren ausgeschüttet, wodurch sich die präsynaptische Spannung innerhalb von 500 ms ändert. Bei Blitzlicht kommt es an Stelle einer Depolarisation direkt zu einer Hypopolarisation. Eine Begrenzung des postsynaptischen Stroms schützt die Rezeptoren vor einer Desensibilisierung.
Regulation
Allgemeine Regulation
Die Transmitterfreisetzung wird unter Einfluss von Magnesiumionen abgeschwächt, da diese die Rezeptoren blockieren. Auf die postsynaptische Rezeptormembran wirken unter anderem Kainat, Glutamat, Domoat, AMP, so wie AP 5 und CNQX durch eine kompetitive Hemmung. Eine Nicht- kompetitive Hemmung wird unter anderem durch Magnesiumionen, Kynureninsäure und Katamin induziert.
Die Antagonisten des Kainatrezeptors sind:
- CNQX
- DMQX
- NS 102
- Kynureninsäure (endogener Ligand)
- Tezampanel
- Ly 382884
- UBP 296
Der ständige Reiz der Rezeptormembran (300 Mikromol Kainat) wird durch CNQX gehemmt. Diese Inhibition ist dissoziationsabhängig. Die Antwort auf die Reizung durch Kainat kann konstant oder transient sein. NS 102 setzt die Selektivität der Ligandenbindungsstelle herab. NS244 wirkt stark hemmend auf die kainatinduzierte Ionenströme und verhindert so "Peakantworten". Ly 382884 ist ein Antagonist für GluR 5 beinhaltende Rezeptoren. Dieser beeinflusst, genauso wie UBP 296, die Induktione von NMDA- Rezeptor abhängigem LTP in den CA 3 hypokampalen Moosfasern. Die durch Kainatrezeptoren ermöglichte synaptische Übertragung, kann durch Freisetzung eines Moosfaser- LTP absolut gehemmt werden. Cyclotiazid beeinflusst den Kainatrezeptor indirekt durch die Aktivierung von AMPA- Rezeptoren.
Die Agonisten des Kainatrezeptors sind:
- Kainsäure
- ATPA
- Domoat
- AMP
- AP5
- Glutamat
Die Kainsäure ist der natürliche Agonist, nach dem die Rezeptoren benannt sind.
Das ATPA ist ein spezialisierter Agonist für GluR 5- beinhaltende Rezeptorkomplexe, der an den Untereinheiten GluR 6 und 7 relativ ineffektiv ist.
Für die Untereinheit GluR 6 werden bestimmte Modulatorproteine unterschieden:
- NDRG1
- SGK 1
- NDRG2 (hemmt in Kombination mit SGK 1 die Funktion von GluR 6)
- mTOR (hemmt ebenfalls die Aktivität von GluR 6)
- RIL (hemmt GluR 6, kann aber auch GluR 1 regulieren)
- Yotiao (Aktivierung von GluR 6)
- Grb2 (Aktivierung von GluR 6)
- Rab- Proteine (Regulatoren der GluR 6 Aktivität durch ihre Unterformen Rab 5 und 11)
Glukokortokoide
Glukokortikoide haben regulierende Wirkung auf nahezu alle Organe. Sie wirken auf den Kohlenhydrat- und Aminosäurenstoffwechsel indem sie die Glukosekonzentration im Blut durch Proteinabbau erhöhen. Durch Stabilisierung der Lysosome, Hemmung der Synthese von Lymphokinen sowie Hemmung der Histamin- Freisetzung wirken sie antiallergen. Des Weiteren haben sie Einfluss auf das Gehirn. Sie wirken auf die hypotalamischen Funktionen und beeinflussen dadurch die Hirnströme. Diese Veränderungen können mit Hilfe des Elektroenzephalogramms dargestellt werden. Psychische Veränderungen können in diesem Zusammenhang ebenfalls beobachtet werden. Glukokortikoide werden bei physischem und psychischem Stress ausgeschüttet. In solchen Stresssituationen können sie durch Stimulation des neuronalen Lernens die Gedächtniskapazität erhöhen. Bei vermehrter Ausschüttung von Glukokortikoiden kommt es zu einer Steigerung der GluR 6- Expression im Gyrus dentatus und im Hypokampus.10
Funktionsstörungen
Klinische Aspekte
Die AMPA- Rezeptoren setzen Neurotransmitter frei, die essentiell für Lern- und Erinnerungsprozesse sind. Eine zu hohe Aktivität von Neurotransmittern kann das Nervensystem und die Neuronen schädigen, in extremen Fällen sogar zum Absterben von Nervenzellen führen. Die Kainatrezeptoren sind für die Feinabstimmung bzw. die Balance zwischen neuronaler Inhibition und Exzitation verantwortlich.
Autismus
Die Ursache für Autismus wird in einer Kontaktstörung der synaptischen Übertragung gesehen. Durch einen Austausch von Nukleotiden (“several nucleotid polymorphism“) im GluR 6 Transkript kommt es dabei zu Punktmutationen. Bis heute konnten sechs verschiedene Loci für derartige Punktmutationen identifiziert werden. Drei davon befinden sich in Exons, drei sind in Introns lokalisiert. Diese Mutationen weisen einen konservativen Aminosäurenaustausch auf. Einer dieser Mutationen ist die M8361, welche im Exon lokalisiert ist, hierbei kommt es zum Austausch von zwei Aminosäuren (Methionin gegen Isoleucin) im C- terminalen Terminus. Da dieser verantwortlich für die Organisation und elektrophysiologischen Eigenschaften der Untereinheit ist, sind Mutationen in diesem Bereich besonders folgenschwer. Durch die Veränderung im C- terminalen Ende des GluR 6 Proteins kann das spezifische SAP90/PSD95 nicht mehr gebunden werden. Dadurch verändert sich die Rezeptorfunktion. So wird z.B. die Desensitisierung vermindert. M8361 kann somit eindeutig ein funktioneller Effekt zugewiesen werden.
Epilepsie
Wenn Glutamin in größeren Mengen in den medialen Kortex abgegeben wird, beschränkt sich das entstehende Potential auf diese Region. Das entstehende Potential kann durch die Aktivität der AMPA- und Kainatrezeptoren leicht abgeschwächt werden. Außerdem wird die Aufnahme von Glutamin in die Neuronen gehemmt. Im Laborversuch wurden Neurone gesunder Tiere über längere Zeit mit hohen Dosen von Kainat stimuliert. Anschließend zeigten diese auch bei geringer Reizung ein lang anhaltendes EPSP, welches zum Auftreten vieler Aktionspotentiale innerhalb kurzer Zeit führte. Bei an Epilepsie erkrankten Tieren zeigte sich nach Abbruch der Kainatstimulation ein IPSP (inhibitorisches (hemmendes) postsynaptisches Potential). Während eines epileptischen Anfalls kommt es zu einer massiven Hyperaktivität der kortikalen Neurone. Eine stark erhöhte Konzentration von extrazellulären Kaliumionen sorgt für eine Depolarisation der Neuronen und eine Absenkung des Schwellenpotentials. Der Grund hierfür liegt in der begrenzten Aufnahmefähigkeit der Gliazellen für Kaliumionen. Dadurch entstehen die, für Epilepsie typischen, generalisierten Krämpfe.(Horn et al. 2009) 4
Spreading Depression
Nach einer starken lokalen Reizung, z.B. einem Trauma, kann es zu einer Ansammlung von Kaliumionen kommen. Da diese von den Gliazellen in derart großen Mengen nicht abgefangen werden können, können die depolarisierten Neurone nicht mehr in den Ruhezustand zurückgeführt werden. Die Erregung breitet sich über immer mehr Neuronen aus, wodurch eine Zone unerregbarer Nervenzellen entsteht. Nach einer solchen Reizung kann es unter Umständen mehrere Minuten dauern bis sich der normale Erregbarkeitszustand (Ruhepotential) der Nervenzellen wieder eingestellt hat.
Neurotoxizität
Allgemein
Eine Natrium- und Chloridionen- Aufnahme lässt die Zellen anschwellen.
Unter Einfluss von Stress kommt es z.B. zu einem vermehrten Einstrom von Kalziumionen. Dies hat einen „Overload“ zur Folge, welcher zu einer Excitotoxizität führt.
Wie Glutamat wirken auch endogene exzitatorische Transmitter in hohen Dosen neurotoxisch. Sie haben Einfluss auf Mitochondrien, Enzyme und Ionenströme.
In den Mitochondrien kann es zu einer Akkumulierung (Ansammlung) von Kalziumionen kommen. Die treibende Kraft des Kalziumeinstroms ist der Ionenkonzentrationsgradient.
Die Kalziumkonzentration kann dabei derart hoch werden, dass die Mitochondrien nicht mehr in der Lage sind ausreichende Menge an ATP bereitzustellen um die Ausgangskonzentration von Kalziumionen wieder herzustellen. Das Mitochondrium wird dabei geschädigt, obwohl die Neuronen noch gesund zu sein scheinen. Auch Enzyme können eine negative bzw. schädigende Wirkung auf die Zellen ausüben. Das Enzym Phospholipase A aktiviert Arachnidonsäure, diese verursacht eine ROS- Produktion (Reaktive Oxigen Species). In dessen Folge kommt es zum „Elektronenleaking“. Dies löst eine Schwellung der Zelle bis hin zur Apoptose aus.
Auch der erhöhte ATP- Verbrauch ist ein häufiger Grund für die Apoptose.
Verteidigungsmechanismen der Zelle
Die Zellen aktivieren Antioxidantien. Diese können Rezeptorantagonisten wie z.B. MK 801 sein.
Antioxidantien fangen die ROS- Produktion mit verhältnismäßig großer Wirksamkeit ab.
EGTA (ethylene glycol tetraacetic acid) bindet Kalziumionen und verhindert somit das Anschwellen der Zelle.
Neben der Aktivierung der Antioxidantien kommt es ebenfalls zur Verminderung von freiem Glutamat.
Protektiver Effekt von Antioxidantien
Die protektive Wirkung der Antioxidantien schützt Neurone vor giftigen Effekten. Sie können ROS abfangen und somit das Elektronenleaking verhindern. Daraus lässt sich schließen, dass oxidativer Stress eine Schlüsselkomponente für alle Formen der Glutamattoxizität darstellt. Die Mitochondrien sind die primären Quellen für den reaktiven Sauerstoff.
Des Weiteren werden durch EGTA Kalziumionen gebunden, wodurch ein Ionenüberschuss in der Zelle verhindert wird.
Forschungen zeigten, dass eine Behandlung von Neuronen mit SOD (74) oder SOD mimik die Wirkung von Kainatgiften drastisch reduzieren kann. Ebenso kann eine Behandlung mit Vitamin E und Trolox die Neurone vor Neurotoxizität schützen.
Literatur
(1) Rassow J., Hauser K., Netzger R., Deutzmann R. (Thieme Verlag, 2008), Duale Reihe Biochemie: (4) 779-782
(2) Huettner J. E., (Elsevier Verlag, 2003), Progress in Neurobiology: (21) 387-407
(3) Laezza F., Wilding T. J., Sequeira S., Coussen F., Zhao Z., Hill-Robinson R., Mulle C., Huettner J. E., Craig A. M. (Elsevier Verlag, 2007), Molecular and Cellular Neuroscience: (12) 539-550
(4) Horn F., Armbruster M., Berghold S., Blaeschke F., Grillhösl C., Helferich S., Moc I., Pritsch M., Schneider N., Ziegler P., (Thieme Verlag, 2009), Biochemie des Menschen: (3) 427-429
(5) Silbernagel S., Despopoulos A., (Thieme Verlag, 2000), Taschenatlas der Physiologie: (1) 55
(6) Silbernagel S., Klinke R., (Thieme Verlag, 2001), Lehrbuch der Physiologie: (1) 77
(7) Fahlke C., Linke W., Raßler B., Wiesner R., (Elsevier, 2008), Taschenatlas Physiologie: (4) 52-53, 74-75
(8) Schlumberger C., (Dissertation 2010), Die Rolle der metabotrophen Glutamatrezeptoren der Gruppe I und II in Tiermodellen der Schizophrenie: (13) 62-74
(9) Leuschner W. D., (Dissertation 1998), Subunit-assembly of AMPA-type glutamate receptors: (6) 2-4. 8-10
(10) Wittmann M., (Dissertation 2001), Die Rolle metabotropher Glutamatrezeptoren bei der Modulation der erregenden und hemmenden synaptischen Übertragung in der Substantia nigra pars reticulata: (6) 1-5
Weblinks
(12)http://www.ncbi.nlm.hih.gov/pubmed/9923677|www.ncbi.nlm.hih.gov/pubmed/9923677
(14)http://www.nbci.nlm.gov/pubmed/892134|www.nbci.nlm.gov/pubmed/892134
(15)http://www.ncbi.nim.nih.gov/pubmed/12743362|www.ncbi.nim.nih.gov/pubmed/12743362
Bildquellen
(18)http://de.wikipedia.org/w/index.php?title=Datei:Aktionspotential.svg&filetimestamp=20110801150931
(20)http://de.wikipedia.org/w/index.php?title=Datei:GluR-Schema.jpg&filetimestamp=20040403232903
(21) selbst angefertigt (nach Vorlage von http://www.bris.ac.uk/synaptic/receptors/kar/)
Verfasst von: Julia- Nadin Onigkeit, Denise Kern, Christine Reitmayer
Besonderer Dank gilt Herrn Ingo Oeppert, der uns Nächte lang bei der Formatierung in das Wikipedia- Format unterstützt hat, sowie Frau Regine Reitmayer für die Korrekturlesungen.