Obezitás és az Agy
TARTALOMJEGYZÉK
Contents
Az elhízás, mint fogalom
Mikor napjainkban kimondjuk a szót: „obezitás”, a hétköznapi értelemben vett kövérségre gondolunk; a túlsúlyra, az elhízásra, fejünkben húsos férfiakat és nőket képzelünk el, akik éppen jó étvággyal eszik valamely divatos gyorsétterem esztétikusan kinéző, ínycsiklandó - de jobb nem belegondolni milyen alapanyagokból készülő - termékét. Tehát a legtöbb ember az obezitás, mint kifejezés alatt az elhízás nagyon súlyos fokát érti. Az egészségügyi szakértők a „túlsúlyt” úgy definiálják, hogy a testsúlynak egy felesleges mennyisége, melyet alkothat izom, csont, zsír és víz is. Azonban a mindennapi szóhasználatban, továbbá az orvosi gyakorlatban használt túlsúly, elhízás, súlytöbblet szavak alatt a testzsír túlzott mennyiségben való jelenlétét értjük, mely zsírmennyiséget az emberek a táplálékkal veszik fel. Az Egészségügyi Világszervezet (World Health Organization) pedig úgy fogalmaz, hogy a túlsúlyosság egy olyan orvosi kezelésre szoruló állapot, amelyben a testen felhamozódott többlet testzsír hatást gyakorolva az egyén egészségügyi állapotára, csökkent várható élettartamhoz, továbbá súlyos egészségügyi problémákhoz vezet (WHO, 2000). Az evolúció során a szűkös táplálékellátás körülményei között előnyt jelentett a minél nagyobb mértékű zsírraktározási képesség: ez azonban napjainkban a könnyű táplálékmegszerzési lehetőségek és a nagy energiatartalmú ételek mellett visszájára fordult. Az emberi elhízásban genetikai, környezeti és pszichoszociális tényezőknek tulajdoníthatunk szerepet - ez nemcsak az emberre, hanem az emlősökre általában is jellemző. A táplálékfelvételt szabályozó mechanizmusok a táplálékfelvételt úgy alakítják, hogy hosszabb távon az energiamérleg egyensúlyban legyen, és ezzel a legfontosabb energiaraktár, a zsírszövet tömege állandó maradjon. Az emberi és állati (emlősök) elhízás korunkban tapasztalható tömeges megjelenésének egyik tényezője biztosan az, hogy a táplálékfelvétel hedonisztikus tényezője felülírja a testtömeget állandóan tartó homeosztatikus szabályozást. A kedvezőtlen hatású tényezők kapcsolódnak: a genetikai adottságokhoz csatlakozik a kedvezőtlen táplálék-összetétel és a korunkra jellemzően egyre csökkenő izomtevékenység (Fonyó, 2011) .
Szociológiai háttér
A 18. század vége felé, az angliai fő technológiai fejlesztések előrejelezték a világszintű szociogazdasági és kultúrális változásokat, amelyek az emberiség történelmének harmadik nagy fordulópontját eredményezték. A gépesített gyártás és földművelés, amelyeket lehetővé tette az üzemanyag ipar látványos fejlődése, drámaian megnövelte a (mezőgazdasági) termékek előállításának mennyiségét. Továbbá, többé-kevésbé megvalósítható lett, hogy hosszabb időre biztonságosan tudjanak élelmiszert tárolni. A történelem során először mindenki számára elérhetőek lettek a tápanyagok. Ezzel egyidőben a motorizált munkavégzés és szállítás megszüntette a fizikai munkavégzés szükségét. A gyerekkori halálozás jelentősen visszaszorult (több ok miatt is). A Föld népessége majdnem hatszorosára duzzadt az 1800-as évek elejéhez képest. Ezen fejlődések következményeként az ipari forradalomnak nagy hatása volt az emberi energia egyensúlyra. Kevés megbízható adat áll rendelkezésünkre, amely dokumentálta a kalória bevitelt, különösen a 19. és 20. századi étel fogyasztásról nincs információnk. Azonban a józan ész azt diktálja, hogy az átlag bevitel alaposan meg kellett, hogy emelkedjen. Az Egyesült Nemzetek Élelmiszer és Mezőgazdasági Szervezete (FAO) arról ad jelentést, hogy az összes napi kalória bevitel folyamatosan növekszik, 1960 óta 20-25 %-al nőtt meg világszerte. Amerikai adatok megerősítik a jelentős növekedését az egy főre jutó kalória bevitelnek az elmúlt 30 évben. Valószínűleg még fontosabb, hogy az étrendünk összetétele is egyértelműen megváltozott: a gabonát sokkal finomabbá őrlik a gépesített malmokban, a finomított cukor is megjelent és egyre többet és többet fogyasztunk belőle, a nátrium bevitel drámaian megnövekedett, ezalatt a kálium bevitel csökkent, a mikrótápanyag sűrűsége csökkent, de a kalória sűrűsége nőtt, a rost tartalom jelentősen csökkent és a telített zsír felváltotta a telítetlent. Ezekkel egyidejűleg környezetünket tudatosan úgy alakítottuk ki, hogy minimális fizikai munkavégzést kelljen végezni. Habár a megbízható módok éppen csak felbukkantak arra, hogy meghatározzuk a teljes napi energia kiadásainkat, a fizikai aktivitás hanyatlása teljesen egyértelmű. A motorizált munkavégzés és szállítás alaposan elnyomta a kalória szükségletünket. Végül, a fűtéstechnológiai fejlődések és a ruházkodás hatékonyan megvéd minket a hideg időjárás veszélyeitől, továbbá alaposan lecsökkentik az adaptív thermogenesishez szükséges energiaigényünket.(H. Pijl., 2011)
Típusok, fokozatok
Még az elején fontos, hogy tisztázzuk, az orvosi gyakorlat megkülönbözteti a túlsúlyos egyéneket az elhízott egyénektől, azonban a kettő között nincs éles határ, ezért az állapot azonosítására az ún. testtömegindexet (body mass index, BMI) használják. A BMI a a testsúly és a testmagasság négyzetének aránya. Normális értéke férfiakban kortól függetlenül, és nőkben 35 éves kor alatt 20-25 között van. A BMI 25-30 közötti értéke túlsúlyt, a 30 feletti BMI-érték pedig elhízást jelent.
A túlsúly kialakulását környezeti hatások - úgymint viselkedés: túlevés, fizikai inaktivitás -, továbbá a szocio-gazdasági állapot is befolyásolhatja, ugyanakkor mindemellett genetikai hatások is állhatnak, amelyek nagyban hozzájárulnak az obezitás kórfolyamatához (Éder K., 2010).
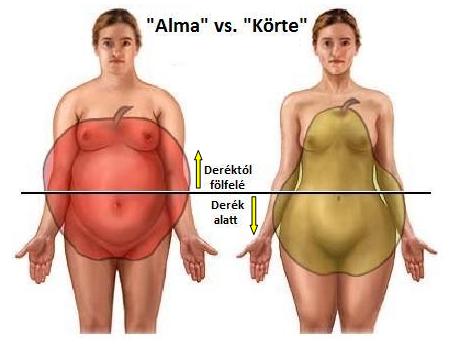
Az orvosi gyakorlatban ma alapvetően az elhízás két típusát különíthetjük el (Halmos T., 1999); az alma formájú, viscerális (zsigeri) jellegû elhízás. Itt a zsírszövet elsôsorban abdominálisan, a hasi zsigerek között helyezkedik el. Erre az elhízástípusra a csípő/derék hányados növekedése a jellemzô, és inkább a férfiak körében elterjedt. A másik típus az ún. körte formájú, vagy genitofemorális obezitás. Itt a zsírszövet a farpofákon, a combokon rakódik le, a has „kötényszerûen” omlik le. Ez a típus gyakoribb a nők körében (1. ábra).
|
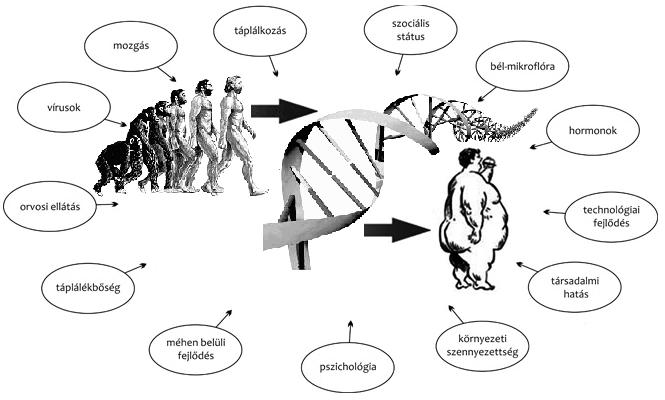
Ugyanakkor genetikai háttér alapján pedig három csoportot különíthetünk el (Ichihara, Yamada, 2008); az ún. monogénes elhízás esetén a betegség kialakulásának hátterében egyetlen gén defektusa áll. Az ilyen génhibára az jellemző, hogy a mutáció alapvető következménye a táplálékfelvétel szabályozásának sérülése, a hyperphagia. Amikor az elhízás más, jól körülhatárolt klinikai fenotípusokkal együttesen jelenik meg - úgymint mentális retardáció vagy szervspecifikus fejlődési rendellenességek -, szindrómás obezitásról beszélünk. Ezek a szindrómák nem összefüggő genetikai hibákból vagy kromoszóma-abnormalitásokból eredhetnek, lehetnek autoszomálisak (testi kromoszómán elhelyezkedő géndefektus), vagy az X nemi kromoszómához kötöttek. Bár a monogénes vagy szindrómás obezitást okozó géneltérések súlyos következménnyel járnak, populációs szinten kis százalékban fordulnak elő. Sokkal gyakoribb az ún. poligénes elhízás, aminek kialakulásában a különböző genetikai tényezők és az elhízásra hajlamosító környezet közti kölcsönhatások is szerepet játszanak (2. ábra). Nagyon sok gén működik közre a kövérség e formájának megjelenésében, de ebben meghatározott gének változatainak csak csekély szerepet tulajdonítunk. A későbbiekben még részleteiben lesz szó ezen három típusról.
|
Az elhízás okai
- Kétségtelenül megállapítható, hogy elsősorban életmódi és étrendi hatások együttes szerepéről van szó, amikor az elhízás okairól beszélünk. Napjainkban világszerte elterjedt a gyorsétkezők hálózata, ahol magas kalóriájú zsír- és szénhidrátdús ételeket szolgálnak fel. E kalóriagazdag étkezés, párosulva a mozgásszegény életmóddal, megfejelve a gyakori dohányzási és túlzott alkoholfogyasztási szokásokkal, nagymértékben felelős lehet az elhízás járványszerű elterjedéséért. Az emberek jelentős mennyiségû „luxuskalóriát” fogyasztanak, vagyis a szükséges anyagcsere-állapotuk fenntartásán túlmenô felesleges kalóriamennyiséget, mely azután zsír formájábam rakódik le szervezetünkben.
- Az elhízás okaként mindenképp meg kell jelölni az evés örömszerző voltát. Sok esetben nem azért veszünk magunkhoz táplálékot, mert energiára van szükségünk, hanem mert a speciális szag- és ízanyagok befolyásolják a táplálékfelvételt szabályzó központokat, és így elnyomják a homesztatikus szintre beállított normál értékeket. Az életmód és étrend meghatározó szerepére Karen O'Dea ausztrál orvosnő megfigyelése világított rá; a bennszülöttek Ausztráliában több mint 50%-ban jelentősen elhízottak, s az obezitással együttjáró anyagcsere-, ill. szív- és érrendszeri betegségek is magas százalékban fordulnak elő körükben. O'Dea néhány évvel ezelőtt megkért 12 bennszülöttet, hogy 10 hétre menjenek vissza az őserdőbe, s ott őseik életmódja és étrendje szerint éljenek. Alig 10 hét múltán testsúlyuk szignifikánsan csökkent, s ezzel együtt valamennyi kóros metabolikus és kardiovaszkuláris paraméterük javult.
Bizonyosan vannak genetikus okai is az elhízásnak. Ismeretes, hogy az elhízás egy-egy családban generációkon át öröklődik és jól ismert az is, hogy ugyanazon étrendi és életmódi körülmények között a populáció bizonyos része súlyát megtartja, másik része hízik, esetleg súlyából veszít. Ezek a tények genetikai okok feltételezett szerepére utalnak. A kutatásokból az is világossá vált, hogy az egyszerű Mendel-féle egy gén öröklődési séma nem magyarázhatja meg az elhízás rohamos terjedését. Valószínû, hogy – fentebb már részben megemlített – az ún. poligén, multifaktorális öröklődési mechanizmusról lehet szó. A kutatások részint laboratóriumokban használt számos generáción át tenyésztett obez patkány törzsekre terjednek ki, részint generációkon át megfigyelt nagyon sovány, ill. nagyon kövér humán egyedekre. Ezenkívül ismert, hogy zárt etnikai közösségekben, mint pl. a rezervátumokban élő amerikai indiánok, észak-ausztráliai bennszülöttek, vagy az óceániai szigetlakók stb. jelentős %-ban elhízottak. Ezt a tényt Neel dán kutató 1962-ben a „takarékos gén” (thrifty genotype) elmélettel magyarázta.(Halmos T.,1999)
A testsúlyunk változásával kapcsolatba hozható események nagyjából 4-6 millió évvel ezelőtt kezdődtek. Elődeink Kelet-Afrika (Tanzánia, Kenya, Etiópia) erdeiben éltek. Étrendjük elsősorban levelekből, gyökerekből, gyümölcsökből és magvakból állt abban az időben. Ebből kifolyólag a szénhidrát volt az ún. fő makro-tápanyagunk, amit fogyasztottunk. Megközelítőleg két millió évvel ezelőtt a klíma Kelet-Afrikában alaposan megváltozott (szárazabb és hidegebb lett), amelynek nagy hatása volt élőhelyünkre. Az erdők eltűntek és száraz füves területek jelentek meg, ahol növényevők (és nagy ragadozók) éltek. A klímaváltozás miatt főemlős elődeink élőhelyén bekövetkezett étrend-, ill. táplálkozás-beli szokások megváltozása közvetve hozzájárult agyunk növekedéséhez, fejlődéséhez. Egy ún. szénhidrátalapú étrendről áttértünk a hal- és húsalapú étkezésre, amely elegendő energiát és „építőelemet” biztosított ahhoz, hogy elősegítse az encephalizációt. Ugyanakkor a kőkorszakban a primitív ember az éhség és jóllakottság periódusaiban élt. Persze utóbbira csak ritkán került sor, rendszerint csak akkor, ha sikerült közösen valami nagyobb vadat elejteniük. Ilyenkor a vad húsát saját szervezetükben tárolták, olyan gének vezérelte „tárolási hormonok” segítségével, mint az inzulin. Bizonyára az inzulin-rezisztencia ezzel egyidőben történő megjelenésének oka az lehetett, hogy elhárítsa az agy hypoglycaemiajának veszélyét (mivel ezen időszakban a szénhidrátbevitelünk csökkent). A kognitív képességek kialakulása, ill. fejlődése pedig lehetővé tette a tűz használatát és szerszámok előállítását, amelyek így indirekt módon megnövelték az ételből kinyerhető energia mennyiségét – az étel megsütése tovább növeli a táplálékból kinyerhető energiamennyiséget, és megkönnyíti az emésztést - és megkönnyítették a ragadozókkal szembeni védekezést. Ezen felül még a táplálékellátás bizonytalansága a vadászó-gyűjtögető kultúrákban az ún. „takarékos gének” kifejlődését ösztönözte, melyek úgy hatnak, hogy azokban az egyénekben, akikben ez a gén megvan, abban maximalizálják a tápanyag bevitelt és az energia-raktározást, amikor ételhez jut az illető. Ezen gén(ek) biztosították tehát az egyén és a fajta túlélését. Később, a mezőgazdasági és az ipari forradalom gyorsan megváltoztatta környezetünket; a látszólag kifogyhatatlan élelmiszer-készleteink és a fizikai erőt igénylő munkák gépekkel történő helyettesítése eltolták az energia-egyensúlyt, különösen azoknál, akiknél még mindig a korábbi, ősi környezeti körülményekhez való alkalmazkodás dominált; így azoknál, akik genetikailag hordozzák a takarékos géneket és nincs genetikai gátlás alatt a testsúly-növekedésük. Ezért a hirtelen sokkal jobb életkörülmények közé került zárt etnikai közösségekben e géncsoportok már nem a túlélést biztosították, hanem jelentős elhízáshoz vezettek, annak minden patológiás következményével együtt. Újabban pedig még felmerült az a lehetőség is, hogy nem a genotípus, hanem a fenotípus, azaz nem determináló örökletes tényezők, hanem a jelentősen megváltozott külső körülmények vezettek az obezitás epidémiájához, mely környezeti jegyek azután generációkon át tovább örökíthetők. A méhen belüli epigenetikus – a génállomány fölött ható – mechanizmusok potenciálisan megerősítik ezeknek a géneknek a hatását – vagyis az elhízásra való hajlam növekedését.(H.Pijl., 2011)
A testsúlyváltozásra ható agyterületek
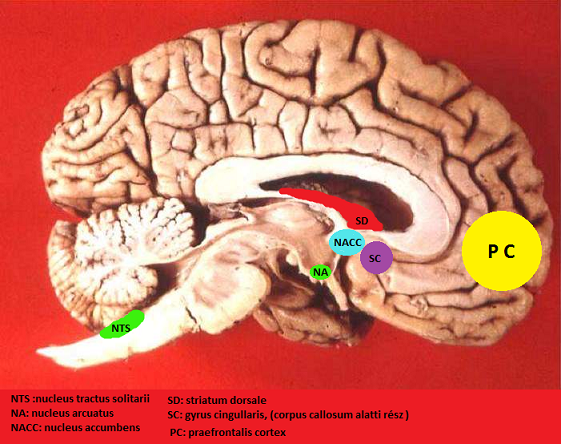
A bevezetőben említettük, hogy a táplálékfelvételt szabályozó mechanizmusok az energiamérleget egyensúlyban tartva szabályoznak. A zsírszövet tömege állandó, normál esetben nem lép fel sem lesoványodás, sem elhízás. Azonban a táplálékfelvételi késztetésnek további meghatározó komponensei is vannak: összefügg a napi ritmussal, továbbá az evés gyönyörszerző, hedonisztikus funkció, így az íz- és szagérzetek kellemes jellege, továbbá a vizualitás (pl. étterem-plakátok) nagyobb energiabevitelre ösztökél, mint amennyi az egyensúly beállításához szükséges, mind emberben, mind pedig állatokban. Ezt a gyönyörszerző hatást kompenzálhatja a szervezet belső állapotának állandóságát biztosító élettani folyamatok összessége (homeosztázis), de a hedonisztikus motiváció gyakran „felülírja” a homeosztatikus szabályozást, energiabeviteli többlethez vezet, ami elhízásban nyilvánul meg. A szervezet energetikai, víz- és hőegyensúlyát szabályozó mechanizmusok közös jellemzője, hogy központi egységük az diencephalonban helyezkedik el. Maga a táplálkozás (táplálék megkeresése, megszerzése, elfogyasztása, megemésztése) igen összetett szomatomotoros működések összessége. Ezt az egész kiterjedt mechanizmust a hypothalamusban elhelyezkedő, több elemből álló központi kapcsolóegység irányítja, amely a hozzá befutó információk – humorális mediátorok által közvetített – alapján indítja meg vagy utasítja el, vagy éppenséggel függeszti fel a már megindult evési folyamatot. A hypothalamus a hozzá eljutó humorális mediátorokon felül még a truncus cerebri-ből (agytörzs), elsősorban egyetlen visceroszenzoros magjából, a nucleus tractus solitarii (NTS) neuronjaitól is kap afferens információt. A hypothalamus azonban nemcsak az energiamérleg felvételi oldalát szabályozza, hanem az autonóm indegrendszeren és a neuroendokrin rendszeren keresztül koordinálja az energiaráfordítást a táplálékfelvétellel, így az obezitás, mint betegség kialakulásában döntő szerepe lehet ezen területek csökkent, vagy hiányos működésének. A hypothalamus magja, a nucleus arcuatus neurosecretoros sejtjei által termelt serkentő, releasing hormonok kiemelkedő szereppel bírnak a szabályozásban. Itt két, neurokémiailag azonosítható, eltérő funkciójú sejtpopuláció van: az egyikből táplálékfelvételt indukáló („orexigén”), a másikból táplálékfelvételt elutasító („anorexigén”) projekció indul ki. A két populáció neuronjai alkotják a táplálékfelvétel szabályozásának primer szenzorait: rajtuk helyezkednek el azok a receptorok, amelyek a zsírraktárak állapotát jelző hormonokra érzékenyek (ezek a tápláltsági állapot hosszú távú jelzőmolekulái, lásd őket alább, az elhízást befolyásoló hormonok fejezetben) (Fonyó A., 2011). A testsúlyváltozásra ható agyterületeket a 3. ábra mutatja be.
|
Az agy jutalmazó központja
Az agyban az élelmiszerek illetve a pszichoaktív anyagok (pl. heroin) hatására különböző agyi régiók aktivitása emelkedhethet , illetve lecsökkenhet. A jutalmazó központ fő területei a nucl. accumbens és a prefrontális kéreg .Szenvedélybeteg, illetve túlevésre és ezáltal elhízásra hajlamos egyéneknél, ezek az agyi területek nem működnek megfelelőképpen, ezért a jutalmazó hatást kiváltó anyag hiányában (dopamin), akadályozza az egyént,hogy különböző zsíros, vagy éppen káros ételekről - vagy éppen kábítószerekről - lemondjon.
A kábítószerek és élelmiszerek között bizonyos értelemben párhuzam állítható. Ennek ellenére mégis jelentős különbségeket találhatunk közöttük. Egyrészt az élelmiszer létfontosságú az élet fenntartásához, másrészt a kábítószereket nem hozták még eddig megfelelő eredményekkel kapcsolatba a relatív elhízással. Születéskor veleszületett tulajdonságunk, hogy az energiadús ételeket részesítjük előnyben. Ezek a zsíros, nagy energiájú ételek ingerlik a "jutalom-áramkört" a további táplálék felvételére. Ez a folyamat a túléléssel és fajfennmaradással állhat kapcsolatban, mint azt, ahogyan már az elhízás okai kapcsán megemlítettük. Az agy jutalom központjával kapcsolatban megemlíthetjük a hypo-válaszkészséget, amely kapcsolatban áll az elhízással.
Hypo-válaszkészség esetében az egyén táplálékfelvétele gyakoribbá válik, mivel a szervezet így képes kompenzálni a jutalmazó anyag hiányát. Ilyen jutalamzó anyag a dopamin (DA). Egy kellemes, ízletes étel elfogyasztása aktiválja a középagyat, , insula-t, a striatum dorsale-t, a subcallosal cingularis-t és prefrontális kérget. Emellett DA felszabadulás indul meg a striatum dorsale-ban, amely összefügg az étel elfogyasztásával járó kellemesség érzetével.( Kyle S. Burger and Eric Stice, 2011)
Kutatások szerint, a dopamin receptorainak mennyiségét, termelődését egy allél (TaqIA) is befolyásolja, amelynek ezáltal szerepe lehet az elhízásban. Megkülönböztetünk TaqIA A1 és A2-es allélt. A1es allél hordozói kevesebb D2 receptorral rendelkeznek az agyi egyes területein, ezért a táplálék elfogyasztása után kevéssé aktív a corpus striatumának aktivitása, ami fokozott, többszöri evésre ösztönzi az egyént. Ez jövőbeli súlygyarapodást eredményez.(Cseh J., 2012)
Az obezitást befolyásoló anyagok, hormonok
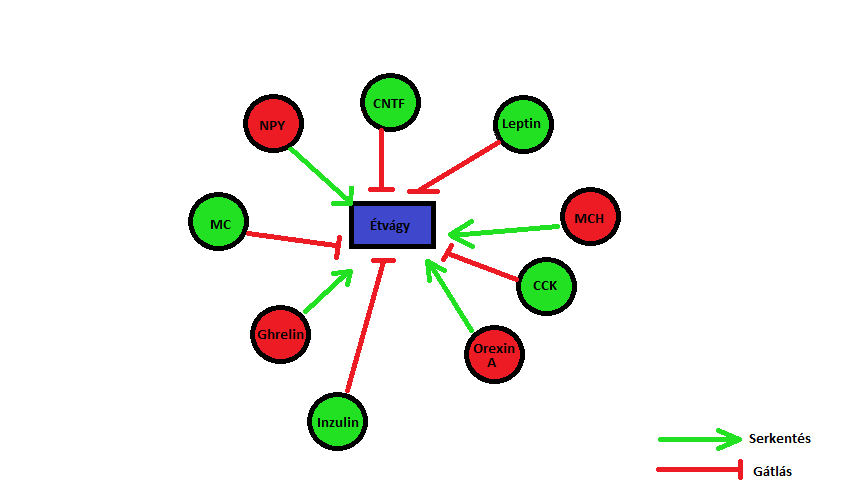
A központi idegrendszer által irányított elhízási folyamatokban szereplő anyagok az étvágy közvetlen, vagy közvetett serkentésen, vagy éppen gátlásán keresztül módosítják a szervezet zsírraktározásának mértékét. (S.S. Yeh, M. W.Schuster, 1999.) (4. ábra)
|
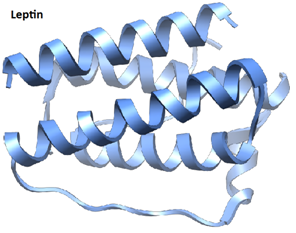
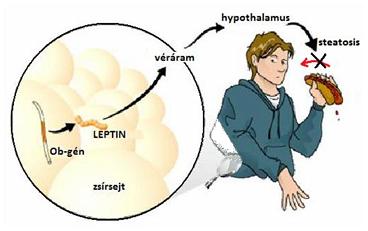
Leptin: A leptin egy 16 kDa tömegű polipeptid hormon (5. ábra), amely a fő szerepet játsza az energiafelvétel és -leadás szabályozásában, úgy mint étvágy, éhség és anyagcsere. Az egyik legfontosabb zsírszöveti hormon (adipose-derived hormon) (Brennan AM, Mantzoros CS., 2006) (Matsuzawa Y, Funahashi T, Nakamura T., 1999). Az Ob(Lep) gén (Ob – ebese, elhízott; Lep – leptin hormon) emberben a 7. kromoszómán helyezkedik el. Elsőként táplálékfelvételt gátló hatását ismerték fel (6. ábra). Ezen hatás mellett azonban jelentős még a zsíranyagcserében betöltött szabályozó szerepe: csökkenti a zsírsavszintézist a májban, növeli a zsírsavak oxidációját, ezzel a steatosis ellen ható tényező (steatosis: a lipidmolekulák sejten belüli abnormális visszatartása). Leptinhiány esetén toxikus lipidtermékek keletkeznek, ezek felelősek a nem adipocyta sejtekben a steatosisért, továbbá egyes szervekben (pl. szív cardiomyocytái, hasnyálmirigy Langerhans-szigeteinek béta-sejtjei) apoptózist indukálnak (ED és mtsai, 1995).
|
|
|
Inzulin: Az inzulin a hasnyálmirigy Langerhans-szigeteiben található béta-sejtek által termelt polipeptid hormon (7. ábra), amely a szénhidrátok, fehérjék és zsírok anyagcseréjének szabályozásában vesz részt. A szervezet sejtjei csak inzulin jelenlétében képesek felvenni a vérből a glükózt (American Society of Health-System Pharmacists, 2009).
|
Neuropeptid Y: Az NPY egy 36 aminosavból álló peptid hormon emberben, az agy és az autonóm idegrendszer közötti neurotranszmitter szerepét tölti be (Tatemoto K., 2004). A hypothalamus nucleus arcuatus magcsoportja termeli az AgRP peptidhormonnal együtt (lásd alább) (Kuo LE és mtsai, 2007). Néhány típusa előfordul sok más állatban. Olyan anyag, mely az agyra hatva stimulálja a táplálékfelvételt, tehát a leptin antagonistája; az NPY hatása űgy csökken, ha van olyan anyag, mely gátolja a NPY-receptorokat, így csökentve az étvágyat; ezen funkció betöltésében van szerepe a leptinnek (Colmers WF, El Bahn B., 2003) (Mosby's Medical Dictionary, 2009).
CNTF (=ciliary neurotrophic factor): A CNTF egy olyan fehérje (8. ábra), mely csökkentheti az elhízás mértékét és a cukorbetegség kialakulásának esélyét leptin-hiány, vagy leptin-rezisztencia esetén. Ezen anyag elsősorban a mozgató neuronok növekedéséért felelős faktorként lett leírva, mely hatását a gerincvelőben, valamint a szemüregben lokalizálódó idegdúcban (ganglion ciliare) fejti ki. Így először azon hatásait vizsgálták, melyek a motoros neuronok hypofunkcióját orvosolhatják. A kutatók a kísérletek során azonban az alanyok nem várt, és nagymértékű testtömegvesztését tapasztalták. A hatásmechanizmus leírására tudományos körökben két változat tűnt reálisnak. Az első feltevés szerint valamely betegségérzetet keltő citokin hatásához hasonló úton működik. Szemben a másodikkal, miszerint a leptinhez hasonló úton fejti ki hatását (P. D. Labert és mtsai, 2000).
|
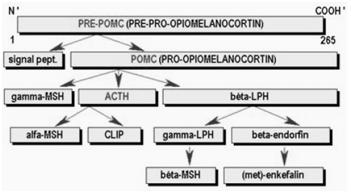
Melanocortin: Az idegsejtekben keletkező hasítási termék, mely a hypophysisben keletkezik egy pre-pro-opiomelanocortinból (Pre-POMC) pro-opiomelanocortinon (POMC) keresztül. A bőr melanocytáiban lévő paprakrin mediátor, a környező melanocyták pigemntképzését fokozza (Fonyó A., 2011). Az anyagcserében betöltött szerepe pedig abban nyilvánul meg, hogy a Neuropeptide Y anabolikus, étvágyfokozó hormon hatását képes ellensúlyozni (Halmos T., 1999).
MCH (melanin concentrating hormone): Egy cilikus 19 aminosavból álló hypothalamicus peptid, mely fő működése, a bőr pigmentációjának szabályozása. Emlősökben szerepet játszik még a táplálkozási viselkedésben, a hangulat kialakításában, az alvás-ébrenlét ciklusában, továbbá az energiamérleg kialakításában. A táplálékfelvétel stimulálásában játszik szerepet.
CCK (=cholecystokinin): A gastrointestinalis rendszer egy olyan peptidhormonja, mely felelős a zsír- és fehérje-emésztés stimulálásában.
Orexin-A: A hypothalamus által termelt 33 aminosavból álló neuropeptid-hormon, mely serkenti a táplálékfelvételt.
Ghrelin: Ahrelin nevezetű peptidhormont a gyomor specifikus endokrin sejtjei szintetizálják és szecernálják; a hypothalamust a véráram útján éri el. Az akut éhségállapot hormonja – a gyomor-bél üres állapotát jelzi –, oxigén szignálmolekula. A ghrelin szintje emberben étkezést megelőzően emelkedik. Aktiválja a nucleus arcuatusban az orexigén projekciót.
AgRP (agouti-related protein): A hypothalamus nucleus arcuatus magcsoportja által termelt hormon. Az NPY és AgRP peptideket együtt NPY-AgRP-neuronokként ismerjük (Fonyó A., 2011).
Uncoupling proteins (=szétválasztó fehérjék): A "szétválasztó" (uncoupling) fehérjékrôl már közel 30 éve vannak adataink. Elôször csak a téli álmot alvó állatok zsírszövetébôl izolálták ezen fehérjéket, melybôl kiderült, hogy azon folyamatokat szakítják meg, amelyekben a szervezet energiát termel. Szellemesen úgy jellemezték hatásukat, hogy "lyukakat fúrnak" a szervezet energiaellátó csôvezetékében. Ilyen módon az ATP-szintézis, mely az energiatárolás megindulásához szükséges kiinduló folyamat, a "szétválasztó" fehérjék mûködése miatt nem indul be, az elveszett kémiai energia hô formájában távozik, a téli álmot alvó állatok így a hideghez adaptálódni képesek (Halmos T., 1999).
Hibafaktorok
A bevezetőben már volt szó a genetikei állomány egy szakaszának defektusa, vagy módosulása következtében létrejövő elhízásokról. Az alábbiakban részleteiben ismertetjük ezen génhibákat.
Az egy gén hibájára visszavezethető elhízás:
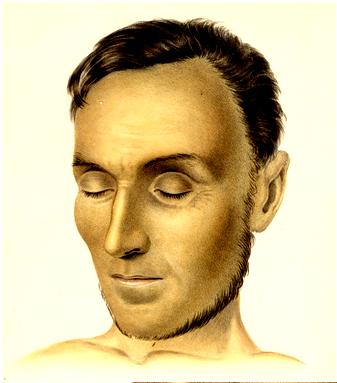
A kövérségnek ez a formája nagyon ritka. A mendeli szabályok szerint öröklődik, és jellemző rá a rendszerint a korai gyermekkorban kezdődő, gyakran extrém fokú elhízás (Farooqi, O'Rahilly, 2006). Ide tartozik például a melanocortin 4 receptor gén (MC4R) mutáció. Az MC4R-hiba a leggyakoribb, ismert, monogénes elhízást kiváltó ok. A súlyos elhízások mintegy 5 %-áért lehet felelős (Fonyó A., 2011). Az MC4R felelős az alfa-MSH megkötéséért, ezáltal az étvágy- és a testtömeg-szabályozás egyik kulcsmolekulája. A mutáció heterozigóta formában is elhízást okoz, ez magyarázza a gyakoriságát (Éder K., 2010). Amennyiben a leptin, vagy a leptin-receptor a hibás, úgy a leptin gén (LEP) és leptin receptor gén (LEPR) mutációjáról beszélünk. Mint fentebb említettük, a leptin hormon kulcsszerepet tölt be az éhség és a jóllakottság szabályozásában. Ezen típusú genetikai defetusú elhízásnál a gyerekek normál testsúllyal születnek, ám már az első pár hónapban nagyon gyorsan nő a testtömegük, és ezért nagyon korán, rohamosan elhíznak, evéskényszerük van, felnőtt korukban pedig hamar a 2-es típusú diabetes mellitus alakul ki náluk. Nem működik megfelelően a pajzsmirigyük sem, és a normális pubertáskori nemi érés sem történik meg náluk (Éder K., 2010). A leptinhiány következményeit terápiásan adott rekombináns leptinnel meg lehet szüntetni. Az emberi elhízások túlnyomó részében azonban a plazma leptinszintje magasabb a normálisnál, jelezve, hogy az állapotot nem leptinhiány okozza - nyilván a magasabb leptinszint a nagyobb mennyiségű zsírtömeg következménye (Fonyó A., 2011). A pro-opiomelanocortin gén (POMC) hibája korai elhízást, Addison-kórt (9. ábra) és vörös hajpigmentációt okoz (Ichihara, Yamada, 2008). A pro-opiomelanocortin gén egy polipeptidet kódol, ami különböző fehérjék, hormonok előalakja, úgy mint például a melanocita-stimuláló hormonok (MSH), a béta-endorfin és az adrenocorticotroph hormon (ACTH) (10. ábra) . Ezek közül az MSH - mint azt már korábban említettük - szerepet játszik a melanintermelődésben és az étvágy szabályozásában, ezért okoz a gén hibája elhízást és pigmentációs problémákat.
|
|
|
Szindrómás elhízás:
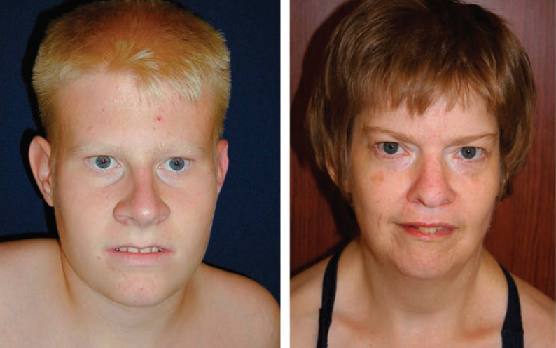
Az egyik ilyen betegség a Prader–Willi-szindróma. A szindróma korai elhízással, újszülöttkori csökkent izomtónussal, túlevéssel, és enyhe fokú mentális retardációval jellemezhető. Jellegzetes szervi elváltozások is megfigyelhetők, mint az alacsonynövés, a kicsi kéz- és lábfejek, továbbá a fejen jellegzetes még az elnyújtott arc, soványodó felső ajak, előreugró orr, a mandulavágású szem és a keskeny koponya (11. ábra). A betegség az apai eredetű kromoszóma egy bizonyos régiójának hiányából ered. Amennyiben az anyai kromoszóma ugyanezen szakasza hibás, akkor egy hasonló betegség, az Angelman-szindróma alakul ki; egy jellegezetes tünete, hogy a benne szenvedők mindig mosolyognak. Az Angelman-szindrómában szenvedőknél késik a fejlődés, főként a beszéd- és mozgásfejlődés, mentálisan visszamaradottak, gyakran EEG- rendellenesség, epilepszia fordul elő náluk, és hajlamosak az elhízásra. Szindrómás elhízás még például a Bardet–Biedl-szindróma (BBS). Ez egy pleiotróp zavar változó expresszivitással, de általában jellemző rá a korai elhízás, fokozatos látásromlás, kéz- és lábujj-rendellenességek, tanulási nehézségek, diszlexia. A betegség autoszomális recesszív öröklődésű. Az elváltozás különböző kromoszómaszakaszok mutációihoz köthető.
|
A poligénes elhízás:
A poligénes elhízás kutatása az olyan egyedi nukleotid polimorfizmusok (SNP-k) és a bázisok ismétlődésének (polyCA-k vagy mikroszatelitek) vizsgálatán alapul, amelyek az ún. jelölt, kandidáns génekben, vagy azok környezetében találhatók (Éder K., 2010). (Kandidáns génnek nevezzük az olyan gént, ami megfelel bizonyos kritériumoknak, például könnyen mérhető jellemzőt befolyásol (pl. testsúly), vagy fenotípusbeli eltérést mutat genetikai módosítás következtében (például génkiütés modellben)). Például francia populáción a morbid obezitással kapcsoltnak találták egy gén, a GAD2, glutamin dekarboxiláz gén három SNP-jét. Egy másik, független kísérletben, német populáción azonban nem sikerült ezt bizonyítani, megismételni. Bár ez a példa kérdéseket vet fel a GAD2 elhízásban betöltött szerepével kapcsolatban, ám korai lenne teljesen figyelmen kívül hagyni a francia eredményt, könnyen lehet, hogy csak populációs eltérésről van szó. Ma már több olyan polimorfizmus ismert, amelyek több független tanulmány szerint is kapcsolatba hozhatók az elhízással. A már a monogénes elhízásoknál is említett LEP- és LEPR-gének polimorfizmusairól például leírták, hogy asszociációt mutatnak az édes íz preferenciájával, ami további bizonyítéka lehet a leptin-jelátvitel elhízásban betöltött szerepének, az édesség, azaz a tipikusan magas kalóriatartalmú élelmiszerek bevitelének szabályozásával. Elhízással összefüggésbe hozható polimorfizmusokat mutattak ki a cannabinoid receptor 1 (CBR1), a dopamin receptor 2 (D2R) és szerotonin receptor 2 (5-HT2) génjeiben, és mivel ezek idegrendszeri receptorok, ez a felismerés alátámasztja az idegrendszer fontos szerepét az obezitás kialakulásában. Ezekkel a kandidáns génvizsgálatokkal szemben a teljes genomszűrésen alapuló vizsgálatok hipotézismentes megközelítést alkalmaznak, nagyszámú mintát vizsgálnak, így növelve a statisztikai erőt. Eddig a legtöbb, teljes genomszűrésen alapuló tanulmány szerint az FTO-gén (fat mass and obesity associated) polimorfizmusa összefüggésbe hozható az elhízással. Humán- és állatkísérletes vizsgálatok is azt mutatják, hogy ez a gén szerepet játszik az étvágy szabályozásában. A hajlamosító változat növeli a táplálékbevitelt, és csökkenti a jóllakottság érzését. Érdekes észrevétel, hogy a fizikai aktivitás befolyásolja a hajlamosító génváltozat hatását, így kevésbé aktív egyénekben kifejezettebb a hatás (Walley at al, 2009). Egy másik kutatás során hat különböző populáción (amerikai, európai, ázsiai, afrikai, amish és pima indián) vizsgálták, hogy milyen kromoszómaszakaszok kapcsolhatók az elhízáshoz, mely szakaszok, polimorfizmusok hajlamosíthatnak elhízásra. Az Y kromoszómát kivéve, minden kromoszómán találtak olyan gént, ami elhízással összefüggő jelleggel (például testtömegindex, csípőkerület, vérnyomás) kapcsolt, legalább az egyik vizsgált populációban (Éder K., 2010).
Konklúzió
Ma, az Egészségügyi Világszervezet (WHO – World Health Organisation) több, mint egy milliárdra becsüli a világon összesen élő azon embereket, akik súlyfölösleggel rendelkeznek, és ebből pedig legalább 300 millióan elhízottak. Ez utóbbi adat különösen aggasztó lehet, hiszen az elhízás megnöveli a krónikus betegségek kialakulásának kockázatát, úgymint a szív- és érrendszeri betegségek, a 2. típusú diabetes mellitus és a rák bizonyos formái. A European Comission egy 2008-as statisztikája látható a 12. illetve a 13. ábrán. Az előbbi az egyes európai országokban élő különböző korosztályokban előforduló elhízott, ill. túlsúlyos nők számarányát mutatja, az utóbbi pedig ugyanezt prezentája a férfiakra vetítve.
A túlsúlyos emberek számos nehézséggel szembesülnek mindennapjaik során. Már a normális életvitel is fáradtságos problémát jelent számukra. Az elhízás következtében a légzési működés is kórossá válhat, a tápcsatornát érintő betegségek is gyakoriak (mint pl. az epekőbetegség a sok koleszterin következtében). Továbbá még a túlsúlyos emberek körében nem ritka pszichés tünet a depresszió, a hipochondria, a fokozott szenzitivitás, a negatív önértékelés, a testképzavar, a kapcsolati probléma, a szexuális tünetek megjelenése, a tudattalan, felfokozott lelki védekezés Manapság az elhízás mindennapos probléma. Civilizációnkból fakad, együtt élünk és foglalkozunk vele, beszélünk róla, megoldásokat keresünk. A válasz megtalálásához először is fel kell tennünk a kérdést. Mik az elhízás okai? Milyen tényezők játszanak szerepet a testzsír kóros gyarapodásában? Mikor az obezitás okairól beszélünk, el kell különítenünk külső és belső tényezőket, viszont fontos tisztáznunk, hogy a külső, és belső faktorok egymásra erős hatást gyakorolnak, szoros kapcsolatban működnek, így egymástól elkülönített pontos hatásuk vizsgálata meglehetősen bonyolult. Talán a legfontosabb obezitás-ok bennünk van. Központi szabályzó rendszerünk többféle módon szerepet játszik a zsírraktározás stimulálásában és gátlásában. A hízás-fogyás szabályozásában rengeteg anyag, idegi központ működik együtt, bonyolult rendszert képezve, egymásba fonódva, egymást segítve, akadályozva. Jelenünkre, és jövőnkre nézve sok lehetőség, és veszély áll előttünk, ha e rendszert megbolygatjuk, saját akaratunk szerint formáljuk át. Rengeteg túlsúllyal küzdő ember és állat problémáját oldhatjuk meg, de vigyáznunk kell, nehogy tönkre tegyük az agyunk befolyásával szervezetünket, egy rendszert, ahol a legkisseb csavar is létfontosságú alkatrész, azt rendszert, ahol minden elem bonyolult kapcsolatban függ össze a többivel.
Irodalom
GreGreen ED, Maffei M, Braden VV, Proenca R, DeSilva U, Zhang Y, Chua SC Jr, Leibel RL, Weissenbach J, Friedman JM: The human obese (OB) gene: RNA expression pattern and mapping on the physical, cytogenetic, and genetic maps of chromosome 7. Genome Res. 5 (1): 5–12, 1995
- Halmos T: Az elhízás epidémiája. Magyar Tudomány: (3) 839-847, 1999
- Matsuzawa Y, Funahashi T, Nakamura T: Molecular mechanism of metabolic syndrome X: contribution of adipocytokines adipocyte-derived bioactive substances. Ann. N. Y. Acad. Sci. 892: 146–54, 1999
- P. D. Lambert, K. D. Anderson, M. W. Sleeman, V. Wong, J. Tan, A. Hijarunguru†, T. L. Corcoran†, J. D. Murray†, K. E. Thabet, G. D. Yancopoulos, és S. J. Wiegand: Ciliary neurotrophic factor activates leptin-like pathways and reduces body fat, withoutcachexia or rebound weight gain, even in leptin-resistant obesity. Proceedings of the National Academy of Sciences, Vol. 98: (8) 4652-4657, 2000
- Colmers WF, El Bahn B: Neuropeptide Y and Epilepsy. Epilepsy Currents/American Epilepsy Society 2 (3): 53–8, 2003
- Tatemoto K: Neuropeptide Y: History and Overview. In Michel MC. Handbook of Experimental Pharmacology. 162. Springer. pp. 2–15, 2004
- Haslam DW, James WP: Obesity. Lancet 366 (9492): 1197–209. 2005
- Brennan AM, Mantzoros CS: Drug Insight: the role of leptin in human physiology and pathophysiology--emerging clinical applications. Nat Clin Pract Endocrinol Metab 2 (6): 318–327. 2006
- Szentágothai J, Réthelyi M: Funkcionális Anatómia III. Medicina: 1374-1375, 1472-1473, 2006
- Kuo LE, Kitlinska JB, Tilan JU, et al.: Neuropeptide Y acts directly in the periphery on fat tissue and mediates stress-induced obesity and metabolic syndrome. Nat. Med. 13 (7): 803–11. 2007
American Society of Health-System Pharmacists. Insulin Injection. PubMed Health. National Center for Biotechnology Information, U.S. National Library of Medicine, 2009
- Bartha T: Endokrinológia. SzIE ÁOTK Élettani és Biokémiai Tanszék, 2009
- Mosby's Medical Dictionary, 8th edition. Elsevier, 2009
- Éder K: Az elhízás genetikája. Magyar Tudomány: (11) 1294-1299, 2010
- Berrington de Gonzalez A.: Body-Mass Index and Mortality among 1.46 Million White Adults. N. Engl. J. Med. 363 (23): 2211–2219., 2010
- Fonyó A: Az orvosi élettan tankönyve. Medicina: 363-383, 634-639, 2011
- H. Pijl: Obesity: evolution of a symptom of affluence. How food has shaped our existence. The Netherlands Journal of Medicine, Vol. 69: (4) 159-166, 2011
- Kyle S. Burger and Eric Stice: Variability in Reward Responsivity and Obesity: Evidence from Brain Imaging Studies. NIH Public Access Author Manuscript Vol. 4: (3) 182–189., 2011
- Cseh J: Cervixtumorok és preblasztomák kialakulását, prognózisát befolyásoló allélpolimorfizmusok vizsgálata. Pécsi Tudományegyetem, Általános Orvostudományi Kar: 21-22, 2012.