Itt írjon a(z) TromboxanSimaizom-ról/ről
Tromboxán szerepe a simaizom kontrakció szabályozásában
A tromboxán
A tromboxán egy nagyon jelentős eikozanoid. Két fajtája ismert: TXA2, TXB2
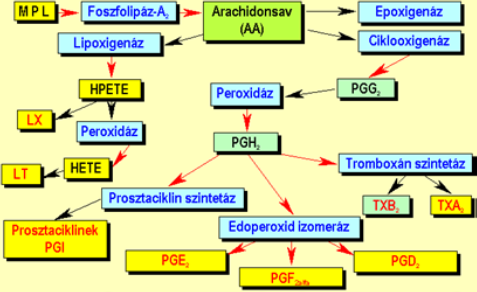
Az eikozanoidok mindenféle sejtben képesek szintetizálódni. Kiinduló vegyületeik a membránalkotó lipidek, melyekből foszolipáz A2 hasítása révén 20 szénatomszámú arachidonsav keletkezik (Δ5, 8, 11, 14 és Ω6). Eme esszenciális zsírsavból több reakcióút indulhat meg: epoxigenáz út, lipoxigenáz út (lipoxinok-LX, leukotriének-LT) és a ciklooxigenáz út. A tromboxán az utóbbi eredményeként jön létre tromboxán szintetázok által. Ugyanezen út végtermékei a prosztaciklinek(PGI) és prosztaglandinok(PGE2, PGF2alfa, PGD2) is.
Maga a foszfolipáz A2 működése G-fehérjéhez kapcsolt folyamat, mely akkor indul meg, ha megfelelő farmakon (pl. Ca-ion) aktiválja a 7M-receptort, az pedig a hozzá kapcsolódó G-proteint, mely végül beindítja az enzimműködést.
Pár érdekesség a foszfolipáz A2-ről: egyes kígyók, pókok mérgében fellelhető, hemolízist okoz. Az enzim a membránalkotó lipidek felépítésében résztvevő glicerin 2. szénatomjáról hasítja le az arachidonsavat, a lipidből pedig lizolecitin/lizokefalin lesz, növelve így a membrán rigiditását.
|
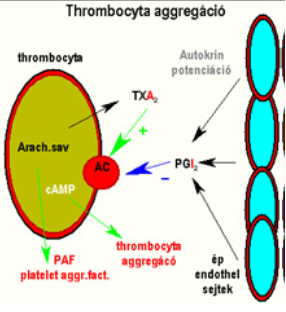
A TXA2 legalapvetőbb szerepe a thrombocyta aggregáció kialakítása.
Az érfal endothel sejtjei normál működéskor PGI2-t (és NO-t) termelnek, melyek az adenilát-ciklázon keresztül növelik az IC-tér cAMP szintjét, ezzel akadályozzák a PLA2 működését. Sérülés hatására azonban megáll a PGI2 szintézis, illetve megindul a TXA2 termelés, mely csökkenti a cAMP szintet, és thrombocyta aggregációt okoz. Ez a folyamat a fehér thrombus kialakulásának stimulátora.
|
A TXA2 a bronchus-kontrakcióban talán a legfontosabb eikoszanoid. Jelentős konstrictora az umbilicalis ereknek, ugyanakkor a koronáriákat és vesemedencét is képes összehúzni, mikor a szöveteket a lokális vérhiányos (ischemia) állapotukból kell megszabadítani.
A simaizomkontrakcióról röviden
A kontrakció – csakúgy, mint a harántcsíkos izomban – a csúszófilamentum modell alapján jellemezhető. Az aktin és miozin összekapcsolódását a MLCK (myozin-light-chain-kinase) indítja el, ha az IC Ca-ion szint a megfelelő értékre emelkedik. A kontrakció addig tart, míg a MP (myosin-foszfatáz) le nem hasít a komplexről egy foszforil csoportot. Akkor ugyanis újra kettéválik az aktin és miozin molekula, vagyis az izom relaxál.
Ez nem a minden vagy semmi elve alapján működik, hiszen a simaizom folyamatos, enyhe kontrakció alatt áll. Ez határozza meg a két enzim (MLCK és MP) aktivitásának egymáshoz viszonyított arányát. Fontos különbség a harántcsíkolt izomhoz képest, hogy az aktin molekulán a tropomiosint egy Caldesmon nevű molekula rögzíti, ami Ca hatására megköti a Calmodulin-Ca komplexet, a tropomiosin lecsúszik az alfa-hélix árkába, így szabaddá teszi a miozin kötőhelyeket. ábra ábra
Simaizom található az erek, bronchusok, belső szervek falában. Alapvető, az élethez nélkülözhetetlen mozgásokat kiviteleznek. Ilyen sajátos mozgás például a nyelőcső simaizomzata által keltett perisztaltikus mozgás.
Máj regeneráció
Máj
Az emésztőcsatornához tartozó máj igen sokrétű szereppel bír. A máj emésztéstől független feladata közé tartozik a különféle endogén metabolitok kiválasztása. Részt vesz a szénhidrát, lipid és fehérje metabolizmus szabályozásában. A máj az izom mellett a szervezet legnagyobb keményítő raktára. A máj a hormonok lebontásában és kiválasztásában is elsődleges szerepet játszik. (Bartha)
A máj működési egysége a májlebenyke, amely a centralis véna körül foglal helyet. A májlebenykék szélén a vér a portális vénából és az a. hepaticából a sejtsorok közötti sinusokba ömlik, ahonnan a centrális vénába fut. Minden egyes májsejt tehát közvetlen kontaktusban van a vérrel, amit a sinusok endothel sejtjeinek fenesztrációja biztosít. A centralis vénától radiálisan futnak a májsejtoszlopok, amelyek két sejtsorból állnak. E két sejtsor között az epekapillárisok találhatók, amelyek a májsejtek által secretált epét gyűjtik össze, és juttatják az epecsatornákba, amelyek mind nagyobb epevezetékekben folytatódnak. (Bartha)
A máj figyelemre méltó megújuló képessége teszi lehetővé a májtömeg működésének helyreállítását toxikus vagy egyéb behatások okozta sérülések miatt.(3.)
Tromboxán A2 a májban
A tromboxán A2 egy erős stimulátora a trombocita aktivációnak, valamint a simaizom összehúzódásnak. A hatását a G-proteinhez kötött receptoron fejezi ki, aminek a neve tromboxán prosztanoid receptor. TXA2 termelése túlszabályozott olyan patológiai állapotok alatt, mint az ishaemia, gyulladás és atherosclerosis. Továbbá, a Kupffer sejtek által termelt TXA2 hozzájárul az akut májgyulladás kialakításához endotoxemia, májreperfúzió és cholestasis során. A TP receptor a máj szinuszoid endotheliális sejtjeiben található, valamint a Kupffer sejtekben. Bizonyított tény, hogy a TXA2 aktiváció felelős a májregenerációért májektómia után. (3.)
A giseng poliszacharidok hatása (1.)
A Hepatic Ischemia Reperfusion Injury (HIRI), ami gyakran előfordul máj transzplantáció, májlebeny eltávolítás és szívinfarktus során; akut májkárosodáshoz vezethet. Számos tanulmány kimutatta, hogy az energia metabolizmus betegségeinél, az oxigén szabadgyökök miatti károsodásnál a nem kiegyensúlyozott, NO/ET és a TXA2/PGI2 termelés a fő problémaokozó.
A fiziológiás körülmények között szekretált bizonyos anyagok képesek szabályozni a simaizom összehúzódást, beleértve az arachidonsav metabolitjait, mint például a PGI2 és TXA2, valamint a NO és ET. Ezek az anyagok relatív körülmények között egyensúlyban vannak. Az utóbbi években kimutatták, hogy a NO/ET egyensúlytalansága egy fontos kockázati tényező a máj mikrokeringés károsodásában a reperfúziós ischaemia során. Az egyensúly PGI2 valamint a TXA2 hatása a stabil metabolitjainak arányától függ, azaz a TXB2/ PGF1 aránytól. Hypoxia és gyulladás során az endotheliális simaizom sejtválasz károsodik, és a NO/ET , TXB2/PGI1 arány kikerül az egyensúlyi állapotból. A reperfúzió a vaszkuláris endothelsejtek megnagyobbodását okozza, valamint a vérlemezkék lerakódását és ezáltal a kapillárisok blokkolását. Kialakul egy úgynevezett no-reflow jelenség. Továbbá a mikrocirkuláció diszfunkciója a májsejtek energiametabolizmusának károsodását okozza és tovább súlyosbíthatja a betegséget.
Ez az imbalacia ginzeng poliszacharid injekció hatására helyreállt, mivel ezen anyag a gyulladást kiváltó tromboxán és prosztaglandin arányát csökkentette. A ginseng poliszacharid feltételezhetően a reperfúziós májgyulladásnál elősegíti az energia metabolizmust azáltal, hogy emeli az antioxidációs készséget és szabályozza a NO/ET és a TBX2/PGF1alfa termelését. A ginseng poliszaharid a legaktívabb anyaga a ginsengnek; tanulmányok kimutatták, hogy ezen poliszaharidok ellenállnak a szabadgyökök károsító hatásának, beavatkoznak a sejt apoptózisába.
A vérlemezkék adhéziója a májregenerációban(2.)
A vérlemezkék feltételezhetően fontos szerepet játszanak a májregenerációban, a gyógyulásban májkimetszés után, valamint akut májgyulladás esetén. Vérlemezke eredetű szerotonin mediált folyamat a májsejtek proliferációja. A tromboxán prosztanoid receptor által végbemenő jelzések szerepet játszanak a gyulladás és a szövetsérülés kialakulásában a vérlemezkék összetapadása által. Más részről a TP receptor jelzései részt vesznek a szövetregenerációban és a tumor növekedésben is a véredények képződésén keresztül.
A vérlemezkék kis speciális vérsejtek, melyek a csontvelő megakaryocitáiból származtathatóak, mint sejtmag nélküli citoplazmatikus testek. Habár a fő funkciójuk a vérzés megállítása szövet-és érsérülés esetén, a vérlemezkék a gyulladás kialakításában valamint a szövetregenerációban is szerepet játszanak parakrin úton vagy direkt sejt-sejt interakció által.
A TXA2 működése patológiás állapotoknál túlszabályozott, azáltal, hogy a vér sejtjei közötti interakciót stimulálja, különösen a vérlemezkék és a mikrovaszkuláris endotheliális sejtek közt létrejövő kapcsolatot. Akut gyulladás során a TXA2/TP receptor út működése figyelhető meg, amelynek aktivációja fokozza a proinflammációs mediátorok és a tumor necrosis factor alpha (TNF-alfa) termelését. Ezen anyagok megemelkedett szintje mikrokeringési diszfunkciót vált ki, valamint az endotheliális leukociták interakcióját.
Ezek a tények a tromboxán gyulladáskeltő szerepét mutatják be, azonban a TP receptorok szignáljai szabályozzák a szinuszoidok raktározó képességét is, hogy helyreállítják a károsodott májszövetet, valamint serkentik a makrofágok működését. A TXA2 angiogenezis stimuláló anyagként szerepelhet, mely még ezen felül elősegíti a cytokinek termelését is, melyek proangiogenikus faktorként segítik elő a trombocita aktivációt.
Tromboxán A2 receptor jelzések támogatják a májszövet regenerációját a makrofágok számának fokozásával (3)
A gyógyulás folyamatát a májsejtek proliferációs képessége és a nekrotikus sejtek eltávolítása teszi lehetővé. A nem működő sejtek eltakarításáért a makrofágok és a monociták felelősek, habár az általuk termelt kémiai anyagok az ép sejteket is károsíthatják.
Egereken által végzett kísérletek igazolják, hogy a TP receptor jelzései szerepet játszanak a májregenerációban, azáltal, hogy elősegítik nemcsak a máj növekedési faktorának traszkripcióját, hanem a makrofágok felületén található monocyte chemoattractant protein-1 (MCP-1/CCL2) receptor megjelenését is. Ezen receptor megjelenése hozzájárul a makrofágok mihamarabbi toborzásához a sérült májba.
A tromboxán A2 szerepe biztos a gyulladás kialakításában a májban, azonban számos kísérlet munkálkodik azon, hogy a májregenerációhoz való hozzájárulása is végleg bizonyítást nyerjen, ugyanis még számos aktiválási és egyéb mechanizmusa nem tisztázódott.
TXA2 receptorok a vesében
Vesében betöltött szerep
- TXA2 az arachidonsav egy metabolitja, amely izomkontrakciót és thrombocyta aggregációt okoz. A vesében a renalis véráramlás, a glomerulációs filtrációs ráta és a a tubuloglomerularis feedback csökkenését okozza. Így bonyolult renalis vér-, vízáramlás és elektrolit anyagcserét tesz lehetővé. A TXA2 szerepet játszik a kórokozók kutatásában, egyes renalis betegségek kórélettanában, mint például a nephritis, transzplantáció kilökődése, illetve húgyuti traktusműködés akadályozása. A thromboxán szintézis aktivitásának csökkentésével, vagy a TXA2 receptor kötődés blokkolásával megelőzhető az általuk okozott renalis károk kifejeződése. (4.)
Az autentikus TXA2 és PGH2 receptorok helyeződése a patkány veséjében
- Polyclonális antitestet használva a TXA2 és PGH2 receptorfehérjék ellen, a mikroszkopikus immunkfluoreszcencia normál módszerével megállapítható azok eloszlása egy fiziológiás patkányvesében. A receptorok mind a glomerulusokban, mind a tubulusokban jelen vannak. Kiemelkedő a számuk a glomerulus kapillárisok lumene mentén. A Bowman-tok epitheliális sejtjei, a podocyták és mesengiális sejtek is mutatnak érzékenységet az immunfluoreszcenciális reakcióra. A tubulusok receptoreloszlása: Proximális tubulusokban főként a kefeszegély mentén, distalis kanyarulatos és a vastag felszálló csatornák luminalis felszínén fordulnak elő. Ezek a megállapítások rámutattak arra, hogy a TXA2 által a vesében jelentkező károk ezen eikoszanoid szintézisének javításával meghatározhatók.
- Számos, patkány vesén végzett vizsgálat foglalkozik a veseszövetben lévő TXA2 szintézisével, sejteredetével. Ezek a tanulmányok kimutatták, hogy a TXA2 főleg a glomerulusokban termelődik, ugyanakkor a vesetubulus hámsejtjeiben a képződése minimális vagy észrevehetetlen.
- A TXA2 nem a legfontosabb eikoszanoid, melyet a glomerulus vagy glomerulus sejtkultúra állít elő. Számuk jelentősen alacsonyabb, mint az egyéb eikoszanoidoké, ilyen például a PGF2alfa, vagy PGE2. Habár egy glomerulus sérülést nyomon követve, a TXA2 szintézise jelentősen fejlett az izolált területen. Ezt mutatták ki glomerulus sérülések számos kísérleti formájában: antitest közvetítette sérülés, diabetikus glomerulopathia, veseimplantáció kilökése. Ilyen esetekben a TXA2 jelzi a gyulladáskeltő sejtek eredetét, melyek főleg aktivált fehérvérsejtek, thrombocyták és beszivárgó glomerulus sturktúrák. Ezen sejtek egyszeri kiürülése után a TXA2 parakrin módon képes hatni az endotheliális, mesengiális és epitheliális glomerulus sejtekre, előidézve ezzel rengeteg biológiai folyamatot. Ilyen módon lehet a mesengiális sejteket legjobban jellemezni, ugyanis rajtuk nagy mennyiségű TXA2 receptor található, melyek liganddal való kötődésével különböző biológiai hatások jelentkeznek, mint például aktiválódik a PKC (foszfo-kináz C), vagy a PI3 (Inozitol-trifoszfát), jelentős DNS szintézis, kontrakció, illetve extracellulársi mátrix képződés indul meg. Az elmondottak alapján sok új információnk van a TXA2 vesében betöltött szerepéről, melynek segítségével hatékonyabban ismerhetjük meg a nephronok működését, mindazonáltal ne feledjük, eme eikoszanoid vesei feladatának kutatása még folyamatban van. (5.)
Tromboxán vesében okozott hatásai
- A trombocitákban és vaszkuláris simaizomsejtekben különböző struktúrájú agonista és antagonista ligandokat vizsgálva feltételezhető, hogy a szövetnek specifikus heterogenitása van. Ez bizonyíték lehet a TXA2 és PGH2 receptorok szövetspecifikus heterogenitásának létezésére. Néhány receptor a foszfolipáz C-n keresztük fejti ki hatását. A tromboxán és a PGH2 számos olyan reakciót indít el a vesében, melyek hozzájárulnak az ott fellépő betegségek fejlődéséhez. Ezek alatt értendő a glomerulusba belépő és kilépő arteriola összehúzódása, az intraglomerulásris trombocyta aggregáció, mesengiális sejtek kontrakciója, és azok mátrixának elburjánzása. Ezeket a hatásokat képesek vagyunk szemléltetni, ha TXA2/PGH2 analógokat és radioaktív ligandokat alkalmazunk. Így feltételezhető egy, a glomerulusban lévő specifikus kötőhelyek receptorcsoportja, mely még nem tisztázott, hogy különböző subtípusa-e a trombocytákban illetve erek simaizmaiban lokalizálódó receptoroknak, vagy affinitásuk a TXA2 és PGH2-höz teljesen megegyezik. Az információ rávilágít eme rendszer funkcionális fontosságára. Ha például a tromboxán szintézist véletlenszerűen gátoljuk, PGH2 felhalmozódást fogunk tapasztalni. TXA2-nek tulajdonítanak még ezenkívül ideg-, immunrendszeri sérüléseket, krónikus vesebetegségeket és a veseimplantációk sikertelenségét. Mindezek állatokban jelentkeznek főleg, de emberben is előfordulhatnak behatárolt kereteken belül. Így a vesekárosodások kezelésében nagy szerepet fog kapni a pharmakológiás TXA2 szintézis vagy esetleg reakcióspecifikus inhibitorok is. Mivel eme eikoszanoid veseszövetre kifejtett hatása (in vitro), és gyógyszerekkel gátolható szintézise és működése (in vivo) jelentős előrelépést jelentett, a későbbiekben így új szerek kezelésbe vonása talán még ígéretesebb eredményeket hoz majd. (6.)
Xiang, B.; Yan, W.; Gao, H.; Luo, Z.; Chen, L.; Wang, W.: International Journal of Research in Pharmacy and Biosciences, Volume 3, Issue 6, 2016, PP 34-48, ISSN 2394-5885 (Print) & ISSN 2394-5893 (Online)
- Minamino, T.; Ito, Y.; Ohkubo, H.; Shimuzu, Y.; Kojo, K.; Nishizwa, N.; Amano, H.; Narumiya, S.; Koizumi, W.; Majima, M.: Life Sciences 132 (2015) 85–92
- Minamino, T.; Ito, Y.; Ohkubo, H.; Hosono, K.; Suzuki, T.; Sato, T.; Ae, T.; Shibuya, A.; Sakagami, H.; Narumiya, S.; Koizumi, W.; Majima, M.: Toxicology and Applied Pharmacology 259 (2012) 104–114
- Takaaki, A.; Kazuhisa, T.; Nobuyuki, T.; Eikatsu, T.; Yoshiyuki, T.; and Keishi, A. (1977-1980): The Second Department of Internal Medicine, Tohoku University School of Medicine, Sendai, Japan
- Bresnahan, B. A.; Le Breton, G. C.; Lianos, E. A.: Nephrology Division, Department of Medicine, Medical College of Wisconsin, Milwaukee, Wisconsin, and Department of Pharmacology, University of Illinois, Chicago, illinois, USA
- Kidney International, Vol. 41(1992), pp. 1483—1493 Remuzzi, G.; Fitzgerald, G. A.; Patrono, C. (1992): Bergamo, Italy, Dublin, Ireland, United Kingdom and Chieti, Italy
Mentés