|
Size: 16081
Comment:
|
Size: 25521
Comment:
|
| Deletions are marked like this. | Additions are marked like this. |
| Line 36: | Line 36: |
---- /!\ '''Edit conflict - other version:''' ---- |
|
| Line 70: | Line 72: |
---- /!\ '''Edit conflict - your version:''' ---- Általánosságban az endocannabinoid-rendszer (EC-rendszer) olyan külső tényezőktől függ, mint a stressz, szöveti sérülések valamint metabolikus rendellenességek (Di Marzo et al. 2004; Piomelli 2003). Klinikai kísérletek bebizonyították, hogy az EC-rendszer krónikus túlműködést mutat az elhízott egyedek szervezetében (Blüher et al. 2006; DiMarzo 2008; Engeli 2008; Engeli et al. 2005). Az endocannabinoid-rendszer legalább két G-protein receptorból épül fel, az 1-es típusú cannabinoid receptorból (CB1), valamint a 2-es típusú cannabinoid receptorból (CB2). A CB1 receptor downregulaciója (receptor számának csökkentése a sejt felületén) eredményesnek bizonyult a táplálék felvétel csökkentésében, a hasüregi elzsírosodás megelőzésében, az éhgyomri vércukorszint redukálásában, valamint a cardiometabolikus veszély faktorok csökkentésében egyaránt. Összességében tehát a CB1 receptor alulműködése az elhízás faktoraival ellentétesen hat (Pertwee et al. 2010). == CB1 downregulációja == Klinikai esetek bebizonyították, hogy a hasüregi elzsírosodás korrelál a periférikus EC-rendszer túlműködésével az elhízott emberek esetében. Következésképpen a túlműködő receptorok downregulációja, különösképpen a CB1 receptoroké, eredményesnek bizonyulnak az elhízásból származó metabolikus rendellenességek kezelésében, csökkenteni képesek a testtömeget, az inzulinrezisztenciát és a máj elzsírosodását (Jourdan et al. 2010; Simiand et al. 1998; Trillou et al. 2003). === Inverz antagonisták === 1980-as évek óta az elhízott és túlsúlyos emberek száma mintegy háromszorosára növekedett Európában. A Rimonabant egy CB1 receptor blokkoló készítmény, mely az egyre súlyosbodó probléma megoldásaként robbant be a gastrointestinalis traktusra ható kedvező hatásai miatt. Ez a CB1 inverz antagonista kedvező hatással van a hepatocyták (máj) valamint az adipocyták (zsír) mitokondriális funkcióira, serkenti a fehér zsírszövetek barna zsírszövetté való átalakulását, valamint megakadályozza az adipocyták hypertrophiáját (Perwitz et al. 2010). Ezen előnyökön kívül a Rimonabant növelte az adiponektin koncentrációját is, amely egy zsírszövetek által szekretált plazma protein. Az adiponektin serkenti a szabad zsírsavak oxidációját, csökkenti a hyperglycemiát és ez testtömeg vesztéshez vezet (Diez and Iglesias 2003; Yamauchi et al. 2001). Bár a készítmény eredményesnek bizonyult az elhízás elleni küzdelemben, súlyos pszichés mellékhatásai (szorongás, depresszió, öngyilkos hajlam) miatt 2009 januárjában betiltották a forgalmazását és minden inverz antagonistának egyaránt (Janero and Makriyannis 2009). === A periférián ható antagonisták === Az inverz antagonisták, mint a Rimonabant is, a központi idegrendszerben található, valamint a periférián levő CB1 receptorokat egyaránt blokkolja. A metabolikus előnyök melyek a CB1 receptorok dowregulációjakor jöttek létre, tehát nem tulajdoníthatók egyedül a központi idegrendszerben elhelyezkedő CB1 receptorok blokkolásának (Quarta et al. 2011). Tanulmányok kimutatták, hogy a CB1 receptor downregulációja egy semleges (nem inverz) antagonistával, vagy egy csak szigorúan a periférián (nem érintve a központi idegrendszert) ható inverz antagonistával hasonló metabolikus előnyökkel jár súlyos idegrendszeri mellékhatások nélkül. Ezek a legújabb vizsgálatok a cannabinoid-alapú elhízás terápia jövőjét jelenthetik (Kunos and Tam 2011). Több ilyen perifériásan ható CB1 antagonista is pozitív eredményeket mutatott a kísérletek alapján, ilyen például az AM6545 (Cluny et al. 2010; Tam et al. 2010) valamint a JD5037 (Chorvat et al. 2012; Tam et al. 2012) nevezetű anyagok. A megfigyelések során az AM6545 10mg/kg napi adagolásával mind a genetikailag hízásra hajlamos, mind pedig a hízókúrával kezelt egereken 12%-os testtömeg csökkenést tapasztaltak. Ugyanez a dózis a rimonabant adagolásánál 21%-os testtömeg csökkenést mutatott, azonban itt nem tapasztaltak semmilyen idegrendszeri mellékhatást. Összességében tehát ezek a tanulmányok és kísérletek bebizonyították, hogy a periférián ható CB1 receptor blokkolói hatásosak az elhízás faktorainak eliminálásában anélkül, hogy idegrendszeri mellékhatásokat okoznának (Tam et al. 2010). === Legújabb lehetőségek a downregulációra === A perifériásan ható CB1 inverz antagonistákon kívül egy teljesen új CB1 ligandumot fedeztek fel az elmúlt években. Ez a komponens alloszterikusan képes szabályozni a CB1 receptort anélkül, hogy hozzákapcsolódna annak endogén lingand-kötő helyéhez (Ross et al. 2012). Egy ilyen alloszterikus CB1 antagonista a PSNCBAM-1. Ez az anyag kötődik a CB1 receptorhoz, de nem az aktív kötőhelyen, ahol a többi inverz CB1 antagonista is kötődik. A kötődés csökkentett táplálékfelvételt és testsúlycsökkenést okozott a kísérleti patkányokban. Még kutatás alatt áll, hogy e pozitív hatások az alloszterikus CB1 antagonistáktól felhasználhatók-e az elhízás valamint a 2-es típusú cukorbetegség kialakulása ellen (Horswill et al. 2007). ||<tablebgcolor="#eeeeee" tablestyle="float:center;font-size:0.85em;margin:0 0 0 0; "style="padding:0.5em; ;text-align:center"> {{attachment:elhízás.jpg|felugró szöveg}} <<BR>>'''2. Ábra'''<<BR>>''A CB1 receptor blokkolásának centrális és periférikus hatásai'' || = A cannabinoidok szerepe a cukorbetegségben = == A II-es típusú cukorbetegség (T2DM) kialakulása == A II-es típusú cukorbetegség (T2DM: Type 2 diabetes mellitus) egy metabolikus betegség, mely két kóros szervrendszeri elváltozás eredményeként alakul ki: a hasnyálmirigy B-sejtjei általi inzulin szekréció károsulásából, valamint az inzulinrezisztencia kialakulásából a zsírszövetben, a májban és az izomban (Ashcroft and Rorsman 2012). Ez a metabolikus betegség több mint 380 millió embert érint napjainkban. A T2DM kialakulása szoros kapcsolatban áll az elhízással (Bastard et al. 2006; Eckel et al. 2011), valamint több más faktor is szerepet játszik a betegség kifejlődésében, mint például a genetikai mutációk, az amilin nevű hormon túltermelődése vagy bármilyen zavar beállása a biológiai órában (Buxton et al. 2012; Shi et al. 2013). Tanulmányok kimutatták, hogy a magas hasi zsírfelesleg endoplazmatikus retikulum (ER) stressz okozója, valamint a zsírszövet megnagyobbodásáért is felelős egyaránt. Visszafordítva ezt az ER stresszt valamilyen genetikai vagy kémiai módszerrel, növelni tudjuk az inzulinérzékenységet a zsírszövetben, a májszövetben és az izomszövetben egyaránt (Kammoun et al. 2009; Ozawa et al. 2005). A kiegyensúlyozatlan táplálék bevitel, probléma az energiaháztartásban és a mitokondriális energianyerésben mind a mitokondrium működési zavarához és ER stresszhez vezetnek, melyek elősegítik az inzulinrezisztencia és a T2DM kialakulását (Goossens 2008; Lim et al. 2009; Rieusset 2011). == Cannabinoidok és a T2DM == A T2DM kialakulása szorosan összefügg az elhízással, ezért annak kezelésében az egyik legfontosabb faktor a testsúly folyamatos kontroll alatt tartása és ellenőrzése (Klein et al. 2004). Klinikai tapasztalatok bebizonyították, hogy az endocannabinoid rendszer túlműködése figyelhető meg mind az elhízásnál, mind a T2DM megjelenésénél. A CB1 receptorok túlzott aktivitása metabolikus stresszhez vezet, ami az inzulinrezisztencia és a T2DM kialakulásáért felelős (Scheen 2007). A CB1 receptor blokkolása az inverz antagonista rimonabant segítségével nagyon eredményesnek bizonyult. A receptor kiiktatása kedvezőleg hatott a májsejtek és zsírsejtek mitokondriális funkcióira, csökkentve ezzel az ER stressz mértékét, amely az inzulinrezisztencia és a T2DM kialakulását serkenti (Wong et al. 2012). További tanulmányok kimutatták, hogy a rimonabant amellett, hogy szignifikánsan képes csökkenteni a plazma glükóz és inzulin szintjét, még a glükóz intoleranciát is képes megelőzni, vagy esetleg visszafordítani a túlsúlyos, de cukorbetegségben még nem szenvedő emberek esetében. Kísérleti körülmények között 20 mg-os dózis csökkentette a glükóz kötődését a hemoglobinhoz, csökkentette a testsúlyt, a derékátmérőt, és a cardiometabolikus rizikó faktorokat a T2DM-ben szenvedő betegek körében (Pi-Sunyer et al. 2006; Van Gaal et al. 2005; Van Gaal et al. 2008). Összességében a rimonabant tehát rendkívül hatásos a T2DM kezelésében, idegrendszeri mellékhatásai miatt azonban nem alkalmazható sem a cukorbetegség kezelésében, sem az elhízás elleni küzdelemben. Az AM6545 majdnem olyan sikeres a glükóz tolerancia és az inzulinérzékenyítés serkentésében, mint a rimonabant, de a kedvezőtlen mellékhatások nélkül blokkolja a perifériás CB1 receptorokat, tehát használható az inzulinrezisztencia kezelésében (Tam et al. 2010). = Irodalomjegyzék = ---- /!\ '''End of edit conflict''' ---- |
A cannabinoid receptor jelátvitel mechanizmus
A Cannabis sativa egyike a legrégebben ismert növényeinknek. Leírásokat már az I. századból találhatunk mind a növényről, mind annak gyógyszertani hatásairól Dioscorides Materia Medica című művéből. Ezek közé tartozik az eufória érzete, az ellazultság, tachycardiás tünetek, hypothermia, és a fájdalomcsillapító hatás is, melyek fő okozója a leginkább ismert delta-9 -tetrahidrocannabinol (THC). Más növényi eredetű alkaloidoktól eltérően a cannabinoidok hidrophob jellegük révén nonszelektív módon változtatják meg a sejtmembránok fluiditását. A drog fő hatása ezen tulajdonságon alapul sokkal inkább, mintsem hogy szelektíven aktiváljon sejtfelszíni receptorokat.(Hillard és mtsai, 1985)
|
Contents
Az endocannabinoid receptorok
A receptorok felfedezése
Az 1990-es évek környékén végzett vizsgálatok jelentős áttöréseket hoztak a témában. A kutatásokat az a feltevés inspirálta, miszerint a cannabimimetikus molekulák potenciális lehetőséget nyújthatnak terápiás célokra való alkalmazhatóságban is. A laboratóriumok és a gyógyszerészeti ipar a delta-9-THC-hoz minőségileg hasonló szintetikus analóg vegyületcsaládot fejlesztett ki, azonban ezen anyagok nagyobb potenciát és sztereoszelektivitást mutattak. Ez utóbbi tulajdonság azonban nem összeegyeztethető a nonszelektív membrán kölcsönhatásokkal, amely így első bizonyítékként szolgált arra, hogy a delta-9-THC szelektív receptorokhoz képes kapcsolódni. Ezen eredményekből kiindulva lehetségessé vált, hogy radioaktív ligand technikával felfedezzék a cannabinoid receptorokat. Howlett és munkatársai 1988-ban írták le az agyi membránokon található magas affinitású cannabinoid anyagokat kötő receptorokat, melyek adenylyl-cikláz aktivitást gátolják. Mindezeket alátámasztja az a szerencsés véletlen, mely során ráakadtak az első G-protein kapcsolt cannabinoid receptor, melyet ma CB1 receptor néven ismerünk, kiegészítő DNS kódjára. (Matsuda, 1990) 1993-ban egy második receptort fedeztek fel ( CB2), mely az elsőhöz képest csupán 44%-os szekvenciaazonosságot mutat, melyből jelentős evolúciós eltávolodásra következtethetünk.( Munro és mtsai, 1993) Intracelluláris kapcsoltságát tekintve azonban különösképp nem tér el a két szubtípus.
A receptorok elhelyezkedése
In situ hibridizációs és immunhisztokémiai tanulmányok során kimutatták, hogy a CB1 receptorok a központi idegrendszer egyes területein és sejttípusain bőséges mennyiségben találhatók meg, de bizonyos perifériás szervek és szöveteken is jelen vannak jelentős mennyiségben. (Mailleux,1992; Matsuda, 1993; Mackei és Tsou,1998) Ez a szelektív eloszlás a központi idegrendszerben biztosítja a drog kognitív, affektív és motoros hatásai közötti anatómiai korrelációt. Azonban számos hatás (pl.: gyulladáscsökkentő, izomgörcsoldó) nem magyarázható az idegrendszeri elhelyezkedéssel. Ezekre ad választ a CB2 receptorok kizárólagosan az immunrendszer sejtjein való expressziója.
Az endocannabinoidok
Az endocannabinoidok felfedezése
A receptorok felfedezésével egyetemben a tudósokban felmerült a kérdés, miszerint ha egy receptor a szervezetben jelen van, akkor annak endogén eredetű aktivátorai is léteznek. Devane, Mechoulam és munkatársaik 1992-ben azt a stratégiát követve, miszerint az endocannabinoidok szintén annyira hidrophob anyagok, mint a THC, sertésagyon végzett kromatográfiás vizsgálatok során értek el sikereket, majd különböző analitikai módszerekkel meghatározták az újszerű anyagok kémiai struktúráját is.
Szerkezetük
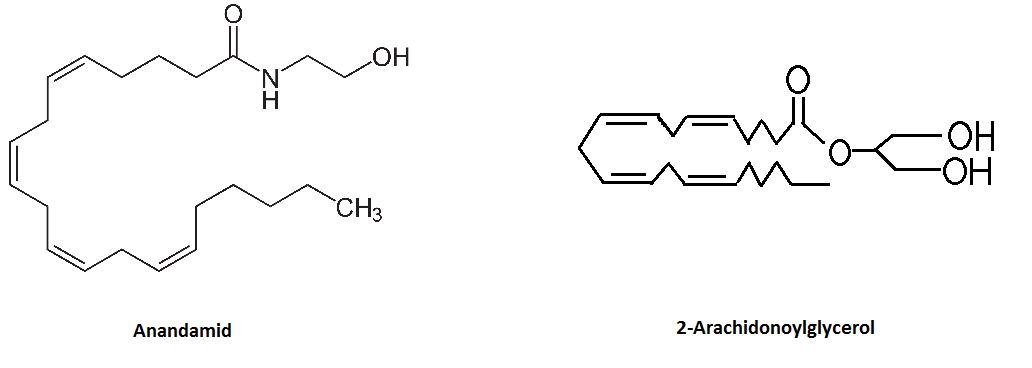
Az endokannabinoidok eikoszanoidokhoz hasonló szerkezetet mutatnak. Két fő részből állnak: egy hosszú, telítetlen zsírsavlánc és egy poláris fej alkotja, mely ethanolt vagy glycerolt tartalmaz. Két legismertebb képviselője az anandamid és a 2-AG (2-arachidonoyl-glycerol). (2.ábra)
|
Szintézisük
Az eikoszanoidoktól eltérően az endocannabinoidok nem oxidatív metabolizmus útján szintetizálódnak. Hasadás helyett a neuronok, gliasejtek és egyéb sejtek membránjában levő prekurzorokból szintetizálódnak szükség esetén. Eltérően más neurotranszmitterektől, az endocannabinoidoknak hidrophob tulajdonságukból adódóan nincs szükségük arra, hogy szinaptikus veziculumokban tárolódjanak. Az anandamid phospatidylethanolaminból , a 2-AG phosphatidylinozitolból jön létre enzimatikus reakciók során.
A CB1 receptorok szerepe a szinapszisokban
A kannabinoid receptorok preszinaptikusan helyeződnek el.( Katona, Freund, 1999) A CB1 receptorok nem csak a gátló, de a serkentő idegsejtek nyúlványain is megtalálhatóak. ( Katona és mtsai, 2006) A receptorok számai összefüggésben vannak a serkentő glutamát és a gátló GABA receptorok számával . A CB1 receptorok feladata fékező hatásukon alapszik, ugyanis a jelátvivő anyagok felszabadulása egy szinapszisban olyan mértékű is lehet, amely már károsító hatással bír. A preszinaptikus oldalon felszabaduló neurotranszmitterek a posztinaptikus membránmegvastagodás ( PSD) több receptorához is kötődnek. Erőteljes inger hatására azonban olyan mértékű lehet a jelátvivő anyagok felszabadulása( úgymond túlcsordul), hogy a fogadó sejt perifériájára is eljutnak (PSM) . Az itt membránba foglalt mGlur5 receptorokhoz ( Somogyi, 1997) kapcsoltan egy DGL-α enzim található( Katona,2006). Ez az enzim alakítja át a glutamát- receptor kapcsolódás során beindított reakciósorozatok végtermékét, a diacilglicerolt 2-AG-vé. A felszabaduló endokannabinoid retrográd módon eljut a preszinaptikus CB1 receptorokhoz. A kötődés után az inhibitorikus G-protein gátolja a feszültségfüggő Ca²+ csatornákat, ezzel megakadályozva a további glutamát felszabadulást. Ezen védőrendszer sérülése jelentős idegrendszeri károkat okozhat a szervezetben.
A cannabinoidok szerepe az elhízásban
![]() Edit conflict - other version:
Edit conflict - other version:
Általánosságban az endocannabinoid-rendszer (EC-rendszer) olyan külső tényezőktől függ, mint a stressz, szöveti sérülések valamint metabolikus rendellenességek (Di Marzo et al. 2004; Piomelli 2003). Klinikai kísérletek bebizonyították, hogy az EC-rendszer krónikus túlműködést mutat az elhízott egyedek szervezetében (Blüher et al. 2006; DiMarzo 2008; Engeli 2008; Engeli et al. 2005).
- Az endocannabinoid-rendszer legalább két G-protein receptorból épül fel, az 1-es típusú cannabinoid receptorból (CB1), valamint a 2-es típusú cannabinoid receptorból (CB2). A CB1 receptor downregulaciója (receptor számának csökkentése a sejt felületén) eredményesnek bizonyult a táplálék felvétel csökkentésében, a hasüregi elzsírosodás megelőzésében, az éhgyomri vércukorszint redukálásában, valamint a cardiometabolikus veszély faktorok csökkentésében egyaránt. Összességében tehát a CB1 receptor alulműködése az elhízás faktoraival ellentétesen hat (Pertwee et al. 2010).
CB1 downregulációja
Klinikai esetek bebizonyították, hogy a hasüregi elzsírosodás korrelál a periférikus EC-rendszer túlműködésével az elhízott emberek esetében. Következésképpen a túlműködő receptorok downregulációja, különösképpen a CB1 receptoroké, eredményesnek bizonyulnak az elhízásból származó metabolikus rendellenességek kezelésében, csökkenteni képesek a testtömeget, az inzulinrezisztenciát és a máj elzsírosodását (Jourdan et al. 2010; Simiand et al. 1998; Trillou et al. 2003).
Inverz antagonisták
1980-as évek óta az elhízott és túlsúlyos emberek száma mintegy háromszorosára növekedett Európában. A Rimonabant egy CB1 receptor blokkoló készítmény, mely az egyre súlyosbodó probléma megoldásaként robbant be a gastrointestinalis traktusra ható kedvező hatásai miatt. Ez a CB1 inverz antagonista kedvező hatással van a hepatocyták (máj) valamint az adipocyták (zsír) mitokondriális funkcióira, serkenti a fehér zsírszövetek barna zsírszövetté való átalakulását, valamint megakadályozza az adipocyták hypertrophiáját (Perwitz et al. 2010). Ezen előnyökön kívül a Rimonabant növelte az adiponektin koncentrációját is, amely egy zsírszövetek által szekretált plazma protein. Az adiponektin serkenti a szabad zsírsavak oxidációját, csökkenti a hyperglycemiát és ez testtömeg vesztéshez vezet (Diez and Iglesias 2003; Yamauchi et al. 2001). Bár a készítmény eredményesnek bizonyult az elhízás elleni küzdelemben, súlyos pszichés mellékhatásai (szorongás, depresszió, öngyilkos hajlam) miatt 2009 januárjában betiltották a forgalmazását és minden inverz antagonistának egyaránt (Janero and Makriyannis 2009).
A periférián ható antagonisták
Az inverz antagonisták, mint a Rimonabant is, a központi idegrendszerben található, valamint a periférián levő CB1 receptorokat egyaránt blokkolja. A metabolikus előnyök melyek a CB1 receptorok dowregulációjakor jöttek létre, tehát nem tulajdoníthatók egyedül a központi idegrendszerben elhelyezkedő CB1 receptorok blokkolásának (Quarta et al. 2011). Tanulmányok kimutatták, hogy a CB1 receptor downregulációja egy semleges (nem inverz) antagonistával, vagy egy csak szigorúan a periférián (nem érintve a központi idegrendszert) ható inverz antagonistával hasonló metabolikus előnyökkel jár súlyos idegrendszeri mellékhatások nélkül. Ezek a legújabb vizsgálatok a cannabinoid-alapú elhízás terápia jövőjét jelenthetik (Kunos and Tam 2011). Több ilyen perifériásan ható CB1 antagonista is pozitív eredményeket mutatott a kísérletek alapján, ilyen például az AM6545 (Cluny et al. 2010; Tam et al. 2010) valamint a JD5037 (Chorvat et al. 2012; Tam et al. 2012) nevezetű anyagok. A megfigyelések során az AM6545 10mg/kg napi adagolásával mind a genetikailag hízásra hajlamos, mind pedig a hízókúrával kezelt egereken 12%-os testtömeg csökkenést tapasztaltak. Ugyanez a dózis a rimonabant adagolásánál 21%-os testtömeg csökkenést mutatott, azonban itt nem tapasztaltak semmilyen idegrendszeri mellékhatást. Összességében tehát ezek a tanulmányok és kísérletek bebizonyították, hogy a periférián ható CB1 receptor blokkolói hatásosak az elhízás faktorainak eliminálásában anélkül, hogy idegrendszeri mellékhatásokat okoznának (Tam et al. 2010).
Legújabb lehetőségek a downregulációra
A perifériásan ható CB1 inverz antagonistákon kívül egy teljesen új CB1 ligandumot fedeztek fel az elmúlt években. Ez a komponens alloszterikusan képes szabályozni a CB1 receptort anélkül, hogy hozzákapcsolódna annak endogén lingand-kötő helyéhez (Ross et al. 2012). Egy ilyen alloszterikus CB1 antagonista a PSNCBAM-1. Ez az anyag kötődik a CB1 receptorhoz, de nem az aktív kötőhelyen, ahol a többi inverz CB1 antagonista is kötődik. A kötődés csökkentett táplálékfelvételt és testsúlycsökkenést okozott a kísérleti patkányokban. Még kutatás alatt áll, hogy e pozitív hatások az alloszterikus CB1 antagonistáktól felhasználhatók-e az elhízás valamint a 2-es típusú cukorbetegség kialakulása ellen (Horswill et al. 2007).
A cannabinoidok szerepe a cukorbetegségben
A II-es típusú cukorbetegség (T2DM) kialakulása
A II-es típusú cukorbetegség (T2DM: Type 2 diabetes mellitus) egy metabolikus betegség, mely két kóros szervrendszeri elváltozás eredményeként alakul ki: a hasnyálmirigy B-sejtjei általi inzulin szekréció károsulásából, valamint az inzulinrezisztencia kialakulásából a zsírszövetben, a májban és az izomban (Ashcroft and Rorsman 2012). Ez a metabolikus betegség több mint 380 millió embert érint napjainkban. A T2DM kialakulása szoros kapcsolatban áll az elhízással (Bastard et al. 2006; Eckel et al. 2011), valamint több más faktor is szerepet játszik a betegség kifejlődésében, mint például a genetikai mutációk, az amilin nevű hormon túltermelődése vagy bármilyen zavar beállása a biológiai órában (Buxton et al. 2012; Shi et al. 2013). Tanulmányok kimutatták, hogy a magas hasi zsírfelesleg endoplazmatikus retikulum (ER) stressz okozója, valamint a zsírszövet megnagyobbodásáért is felelős egyaránt. Visszafordítva ezt az ER stresszt valamilyen genetikai vagy kémiai módszerrel, növelni tudjuk az inzulinérzékenységet a zsírszövetben, a májszövetben és az izomszövetben egyaránt (Kammoun et al. 2009; Ozawa et al. 2005). A kiegyensúlyozatlan táplálék bevitel, probléma az energiaháztartásban és a mitokondriális energianyerésben mind a mitokondrium működési zavarához és ER stresszhez vezetnek, melyek elősegítik az inzulinrezisztencia és a T2DM kialakulását (Goossens 2008; Lim et al. 2009; Rieusset 2011).
Cannabinoidok és a T2DM
A T2DM kialakulása szorosan összefügg az elhízással, ezért annak kezelésében az egyik legfontosabb faktor a testsúly folyamatos kontroll alatt tartása és ellenőrzése (Klein et al. 2004). Klinikai tapasztalatok bebizonyították, hogy az endocannabinoid rendszer túlműködése figyelhető meg mind az elhízásnál, mind a T2DM megjelenésénél. A CB1 receptorok túlzott aktivitása metabolikus stresszhez vezet, ami az inzulinrezisztencia és a T2DM kialakulásáért felelős (Scheen 2007). A CB1 receptor blokkolása az inverz antagonista rimonabant segítségével nagyon eredményesnek bizonyult. A receptor kiiktatása kedvezőleg hatott a májsejtek és zsírsejtek mitokondriális funkcióira, csökkentve ezzel az ER stressz mértékét, amely az inzulinrezisztencia és a T2DM kialakulását serkenti (Wong et al. 2012). További tanulmányok kimutatták, hogy a rimonabant amellett, hogy szignifikánsan képes csökkenteni a plazma glükóz és inzulin szintjét, még a glükóz intoleranciát is képes megelőzni, vagy esetleg visszafordítani a túlsúlyos, de cukorbetegségben még nem szenvedő emberek esetében. Kísérleti körülmények között 20 mg-os dózis csökkentette a glükóz kötődését a hemoglobinhoz, csökkentette a testsúlyt, a derékátmérőt, és a cardiometabolikus rizikó faktorokat a T2DM-ben szenvedő betegek körében (Pi-Sunyer et al. 2006; Van Gaal et al. 2005; Van Gaal et al. 2008). Összességében a rimonabant tehát rendkívül hatásos a T2DM kezelésében, idegrendszeri mellékhatásai miatt azonban nem alkalmazható sem a cukorbetegség kezelésében, sem az elhízás elleni küzdelemben. Az AM6545 majdnem olyan sikeres a glükóz tolerancia és az inzulinérzékenyítés serkentésében, mint a rimonabant, de a kedvezőtlen mellékhatások nélkül blokkolja a perifériás CB1 receptorokat, tehát használható az inzulinrezisztencia kezelésében (Tam et al. 2010).
Irodalomjegyzék
![]() Edit conflict - your version:
Edit conflict - your version:
Általánosságban az endocannabinoid-rendszer (EC-rendszer) olyan külső tényezőktől függ, mint a stressz, szöveti sérülések valamint metabolikus rendellenességek (Di Marzo et al. 2004; Piomelli 2003). Klinikai kísérletek bebizonyították, hogy az EC-rendszer krónikus túlműködést mutat az elhízott egyedek szervezetében (Blüher et al. 2006; DiMarzo 2008; Engeli 2008; Engeli et al. 2005). Az endocannabinoid-rendszer legalább két G-protein receptorból épül fel, az 1-es típusú cannabinoid receptorból (CB1), valamint a 2-es típusú cannabinoid receptorból (CB2). A CB1 receptor downregulaciója (receptor számának csökkentése a sejt felületén) eredményesnek bizonyult a táplálék felvétel csökkentésében, a hasüregi elzsírosodás megelőzésében, az éhgyomri vércukorszint redukálásában, valamint a cardiometabolikus veszély faktorok csökkentésében egyaránt. Összességében tehát a CB1 receptor alulműködése az elhízás faktoraival ellentétesen hat (Pertwee et al. 2010).
CB1 downregulációja
Klinikai esetek bebizonyították, hogy a hasüregi elzsírosodás korrelál a periférikus EC-rendszer túlműködésével az elhízott emberek esetében. Következésképpen a túlműködő receptorok downregulációja, különösképpen a CB1 receptoroké, eredményesnek bizonyulnak az elhízásból származó metabolikus rendellenességek kezelésében, csökkenteni képesek a testtömeget, az inzulinrezisztenciát és a máj elzsírosodását (Jourdan et al. 2010; Simiand et al. 1998; Trillou et al. 2003).
Inverz antagonisták
1980-as évek óta az elhízott és túlsúlyos emberek száma mintegy háromszorosára növekedett Európában. A Rimonabant egy CB1 receptor blokkoló készítmény, mely az egyre súlyosbodó probléma megoldásaként robbant be a gastrointestinalis traktusra ható kedvező hatásai miatt. Ez a CB1 inverz antagonista kedvező hatással van a hepatocyták (máj) valamint az adipocyták (zsír) mitokondriális funkcióira, serkenti a fehér zsírszövetek barna zsírszövetté való átalakulását, valamint megakadályozza az adipocyták hypertrophiáját (Perwitz et al. 2010). Ezen előnyökön kívül a Rimonabant növelte az adiponektin koncentrációját is, amely egy zsírszövetek által szekretált plazma protein. Az adiponektin serkenti a szabad zsírsavak oxidációját, csökkenti a hyperglycemiát és ez testtömeg vesztéshez vezet (Diez and Iglesias 2003; Yamauchi et al. 2001). Bár a készítmény eredményesnek bizonyult az elhízás elleni küzdelemben, súlyos pszichés mellékhatásai (szorongás, depresszió, öngyilkos hajlam) miatt 2009 januárjában betiltották a forgalmazását és minden inverz antagonistának egyaránt (Janero and Makriyannis 2009).
A periférián ható antagonisták
Az inverz antagonisták, mint a Rimonabant is, a központi idegrendszerben található, valamint a periférián levő CB1 receptorokat egyaránt blokkolja. A metabolikus előnyök melyek a CB1 receptorok dowregulációjakor jöttek létre, tehát nem tulajdoníthatók egyedül a központi idegrendszerben elhelyezkedő CB1 receptorok blokkolásának (Quarta et al. 2011). Tanulmányok kimutatták, hogy a CB1 receptor downregulációja egy semleges (nem inverz) antagonistával, vagy egy csak szigorúan a periférián (nem érintve a központi idegrendszert) ható inverz antagonistával hasonló metabolikus előnyökkel jár súlyos idegrendszeri mellékhatások nélkül. Ezek a legújabb vizsgálatok a cannabinoid-alapú elhízás terápia jövőjét jelenthetik (Kunos and Tam 2011). Több ilyen perifériásan ható CB1 antagonista is pozitív eredményeket mutatott a kísérletek alapján, ilyen például az AM6545 (Cluny et al. 2010; Tam et al. 2010) valamint a JD5037 (Chorvat et al. 2012; Tam et al. 2012) nevezetű anyagok. A megfigyelések során az AM6545 10mg/kg napi adagolásával mind a genetikailag hízásra hajlamos, mind pedig a hízókúrával kezelt egereken 12%-os testtömeg csökkenést tapasztaltak. Ugyanez a dózis a rimonabant adagolásánál 21%-os testtömeg csökkenést mutatott, azonban itt nem tapasztaltak semmilyen idegrendszeri mellékhatást. Összességében tehát ezek a tanulmányok és kísérletek bebizonyították, hogy a periférián ható CB1 receptor blokkolói hatásosak az elhízás faktorainak eliminálásában anélkül, hogy idegrendszeri mellékhatásokat okoznának (Tam et al. 2010).
Legújabb lehetőségek a downregulációra
A perifériásan ható CB1 inverz antagonistákon kívül egy teljesen új CB1 ligandumot fedeztek fel az elmúlt években. Ez a komponens alloszterikusan képes szabályozni a CB1 receptort anélkül, hogy hozzákapcsolódna annak endogén lingand-kötő helyéhez (Ross et al. 2012). Egy ilyen alloszterikus CB1 antagonista a PSNCBAM-1. Ez az anyag kötődik a CB1 receptorhoz, de nem az aktív kötőhelyen, ahol a többi inverz CB1 antagonista is kötődik. A kötődés csökkentett táplálékfelvételt és testsúlycsökkenést okozott a kísérleti patkányokban. Még kutatás alatt áll, hogy e pozitív hatások az alloszterikus CB1 antagonistáktól felhasználhatók-e az elhízás valamint a 2-es típusú cukorbetegség kialakulása ellen (Horswill et al. 2007).
A cannabinoidok szerepe a cukorbetegségben
A II-es típusú cukorbetegség (T2DM) kialakulása
A II-es típusú cukorbetegség (T2DM: Type 2 diabetes mellitus) egy metabolikus betegség, mely két kóros szervrendszeri elváltozás eredményeként alakul ki: a hasnyálmirigy B-sejtjei általi inzulin szekréció károsulásából, valamint az inzulinrezisztencia kialakulásából a zsírszövetben, a májban és az izomban (Ashcroft and Rorsman 2012). Ez a metabolikus betegség több mint 380 millió embert érint napjainkban. A T2DM kialakulása szoros kapcsolatban áll az elhízással (Bastard et al. 2006; Eckel et al. 2011), valamint több más faktor is szerepet játszik a betegség kifejlődésében, mint például a genetikai mutációk, az amilin nevű hormon túltermelődése vagy bármilyen zavar beállása a biológiai órában (Buxton et al. 2012; Shi et al. 2013). Tanulmányok kimutatták, hogy a magas hasi zsírfelesleg endoplazmatikus retikulum (ER) stressz okozója, valamint a zsírszövet megnagyobbodásáért is felelős egyaránt. Visszafordítva ezt az ER stresszt valamilyen genetikai vagy kémiai módszerrel, növelni tudjuk az inzulinérzékenységet a zsírszövetben, a májszövetben és az izomszövetben egyaránt (Kammoun et al. 2009; Ozawa et al. 2005). A kiegyensúlyozatlan táplálék bevitel, probléma az energiaháztartásban és a mitokondriális energianyerésben mind a mitokondrium működési zavarához és ER stresszhez vezetnek, melyek elősegítik az inzulinrezisztencia és a T2DM kialakulását (Goossens 2008; Lim et al. 2009; Rieusset 2011).
Cannabinoidok és a T2DM
A T2DM kialakulása szorosan összefügg az elhízással, ezért annak kezelésében az egyik legfontosabb faktor a testsúly folyamatos kontroll alatt tartása és ellenőrzése (Klein et al. 2004). Klinikai tapasztalatok bebizonyították, hogy az endocannabinoid rendszer túlműködése figyelhető meg mind az elhízásnál, mind a T2DM megjelenésénél. A CB1 receptorok túlzott aktivitása metabolikus stresszhez vezet, ami az inzulinrezisztencia és a T2DM kialakulásáért felelős (Scheen 2007). A CB1 receptor blokkolása az inverz antagonista rimonabant segítségével nagyon eredményesnek bizonyult. A receptor kiiktatása kedvezőleg hatott a májsejtek és zsírsejtek mitokondriális funkcióira, csökkentve ezzel az ER stressz mértékét, amely az inzulinrezisztencia és a T2DM kialakulását serkenti (Wong et al. 2012). További tanulmányok kimutatták, hogy a rimonabant amellett, hogy szignifikánsan képes csökkenteni a plazma glükóz és inzulin szintjét, még a glükóz intoleranciát is képes megelőzni, vagy esetleg visszafordítani a túlsúlyos, de cukorbetegségben még nem szenvedő emberek esetében. Kísérleti körülmények között 20 mg-os dózis csökkentette a glükóz kötődését a hemoglobinhoz, csökkentette a testsúlyt, a derékátmérőt, és a cardiometabolikus rizikó faktorokat a T2DM-ben szenvedő betegek körében (Pi-Sunyer et al. 2006; Van Gaal et al. 2005; Van Gaal et al. 2008). Összességében a rimonabant tehát rendkívül hatásos a T2DM kezelésében, idegrendszeri mellékhatásai miatt azonban nem alkalmazható sem a cukorbetegség kezelésében, sem az elhízás elleni küzdelemben. Az AM6545 majdnem olyan sikeres a glükóz tolerancia és az inzulinérzékenyítés serkentésében, mint a rimonabant, de a kedvezőtlen mellékhatások nélkül blokkolja a perifériás CB1 receptorokat, tehát használható az inzulinrezisztencia kezelésében (Tam et al. 2010).
Irodalomjegyzék
![]() End of edit conflict
End of edit conflict