Az agytörzsi ébresztőrendszer
Contents
Az agy, a gerincesek központi idegrendszerének koponyaüregben elhelyezkedő része. Számos vegetatív, szomatikus és érzőműködésen kívül, ez a szerv felelős az alvás-ébrenlét, mint ciklikus működés szabályozásáért. Az agytörzs és a talamusz összehangolt munkájának köszönhető a természetes pihenő állapot kialakítása, valamint az abból való ébredés. Az egyensúly kialakításában a legfontosabb szerepet a kolinerg és adrenerg sejtek összehangolt munkája biztosítja, de emellett számos egyéb központi idegrendszer által termelt neurotranszmitter segíti azt. Az alvás folyamatát az ún. microébredések is kísérik, melyek elengedhetetlenek a ciklikus működés szabályozásában. Néhány környezeti tényező – mint, például a megvilágítás és a hőmérséklet – alapvető hatást gyakorol az alvás-ébrenlét cirkádra.
Agytörzs anatómiája
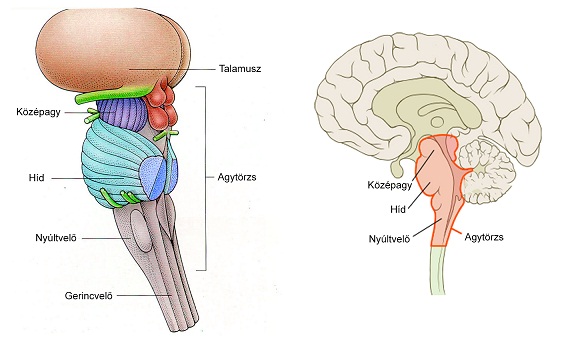
Az agytörzs a központi idegrendszer kisméretű, de működésileg életfontosságú része. Az agytörzs kiterjedt funkciói három fő csoportba sorolhatók: - Átjáróként szolgál azon felszálló és leszálló pályák számára, amelyek a gerincvelőt összekötik az előagy különböző részeiben lévő magasabb idegi központokkal; - Olyan fontos reflexek központjait tartalmazza, mint például a légzés, a vérkeringés és a tudatállapot szabályozása; - A III.-VI. agyidegek kilépési helye. Az agytörzset a nyúltvelő (medulla oblongata), a híd (pons) és a középagy (mesencephalon) alkotja. (1. ábra)
A nyúltvelő, csakúgy, mint a gerincvelő, szürke- és fehérállományra osztható, de az állományok nagy mértékben átrendeződtek. A fehérállomány adja a gerincevelőt és a felsőbb központokat összekötő fel- és leszálló pályarendszereket, illetve ez számos pálya dekuszációjának helyszíne. A szürkeállományban található meg néhány agyideg magja. A formatio reticularis is a nyúltvelőben található, mely az idegrostok és idegsejtek kis csoportjának laza hálózata. A híd a kisagy előtt található meg, a nyúltvelőt köti össze a középaggyal. Számos felszíni képlet található rajta, mely idegek kilépését, az értörzsek haladását, és a benne futó rostokat szemlélteti. A hidat caudalis részre, a tegmentum területére és a pars basilisra oszthatjuk. A középagy a hidat és a kisagyat köti össze az előaggyal. Boltozatos része a tectum két pár ikertestből (corpora quadrigemina) áll, középső része, a tegmentum átkapcsoló centrum. Bazális részén helyezkedik el a crus cerebri. (Dr. Fehér György, 1980)
|
Az alvásért felelős agyi központok az agytörzs középső részén, a hipotalamuszban (köztiagy) és a bazális előagyban találhatók. A talamusz (köztiagy) működése ezek hatására változik meg az alvás folyamán. Éber állapotban a talamusz közvetíti a külvilág ingereit az agykéregnek, míg a mély alvásban ez az, ami módosul.
Alvás fázisai
Emlősökben és madarakban az alvás két alapvető fázisra osztható, a REM (rapid eye movement) és NREM (non-REM). Mindkettő különböző fiziológiai, idegi és pszichológiai változásokkal bír, ez alapján az alvás további szakaszait lehet elkülöníteni. - NREM 1. stádium: Átmenet az ébrenlét és alvás között. Az izmok még az ébrenléthez hasonlóan aktívak, a szemek lecsukódnak. Jellemzi az elektroenkefalogrammon megjelenő Theta aktivitás (3.5-7,5 Hz). - NREM 2. stádium: a szívritmus és testhőmérséklet csökken, szemmozgás nincs, az agyhullámok lassulnak. - NREM 3. stádium: Korábban NREM3 és NREM4 szakasza volt megkülönböztetve. Lassú hullámú alvásnak (SWS -Slow Wave Sleep) is hívják, ilyenkor a nagy amplitudójú Delta aktivitás mérhető az EEG-n. Az alvó egyed ebben a fázisban legkevésbé érzékeny a környezeti hatásokra; azok az ingerek melyek a kezdeti fázisokban még zavaróak voltak, itt már nem váltanak ki választ. Emiatt ebben a szakaszban a legnehezebb felébreszteni valakit. Felszabadulnak a növekedési hormonok, az izmok még aktívak, helyreáll a szervezet energiaháztartása. - REM: Gyors szemmozgás, fokozott agyi tevékenység, szabálytalanabb légzés jellemzi, a vázizmok átmenetileg bénult állapotban vannak, az álomképek megjelenése itt történik. A REM fázis acetil-kolin szekréció hatására aktiválódik, miközben a szerotonint szekretáló neuronok gátoltak. (Helli Merica, Ronald D. Futune, 2004)
Mindezen szakaszok 90-120 percig tartó ciklusosságot mutatnak, melyek az alvás folyamán meghatározott sorendben követik egymást: N1- N2- N3- N2- REM, körülbelül négy- ötször ismétlődik ez a ciklus egy alvásprogramon belül. Az ébredés mindig a REM fázisból történik, még akkor is, ha valakit - aki az előtte lévő fázisok valamelyikében van - próbálunk felébreszteni, gyorsabban végigmegy a körön és a REM-ből ébred fel.
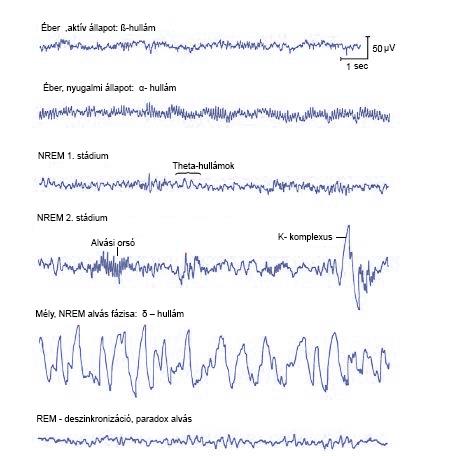
Elektroenkefalográfiával (EEG) bizonyos agyterületek aktivitása mérhető, amit hullám formában regisztrálunk és vezetünk el, ezek jellemzőek az adott fázisra.(2. ábra)
- Éber, aktív állapot: ß-hullám, ami 18-25 Hz közötti frekvenciájú, 20 μV alatti amplitudójú.
- Éber, nyugalmi állapot: α- hullám, 8-12 Hz, amplitúdója változó, de általában 50 μV alatti.
- Alvás kezdeti fázisa: Θ- hullám (theta) , 4-7 Hz, amplitudója változó, de nagyobb, mint a korábbi szakaszoknál.
- Mély, NREM alvás fázisa: δ – hullám (delta),1-4 Hz, legnagyobb amplitudójú. (Jaime R. Villablanca, 2004)
|
A reticuláris aktiváló rendszer (RAS)
A retikuláris aktiváló rendszer az emlősök agytörzsében elhelyezkedő hálózatos rendszer. Számos biológiai funkciót lát el, köztük az alvás és ébrenlét ciklusát, a viselkedés motivációt, valamint a légzés és a szívverés szabályozását. E terület traumás sérülése kómát okozhat, valamint különböző alvási rendellenességeket, például narkolepsziát.
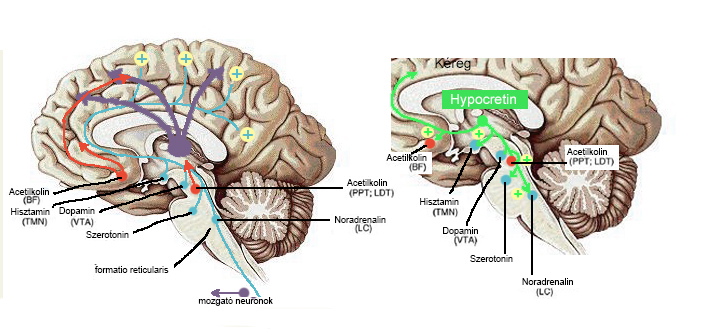
A RAS különböző neuronális útvonalakból áll az agytörzs és az agykéreg között. Az útvonalak kiindulási pontja a felsőbb agytörzs reticuláris magjai, amely keresztühalad synapticus interneuronokon a rostrális intralamináris és thalamicus területen, majd az agykéregbe érkezik, amely idegsejtjei az ébredésért felelősek. Ennek eredményeképpen azok az egyedek, melyek talamuszának intralamináris idegsejtei mindkét oldalon sérültek, aluszékonyságban és letargiában szenvednek. Néhány terület, amit még az RAS-hoz kapcsolnak: - középagy formatio reticularis-a - mesencephalicus nucleusok - hypothalamus dorsalis területei - agytörzs tegmentuma.
A RAS idegi útvonalát néhány neurotranszmitter komplex interakciója szabályozza. Az RAS tartalmaz kolinerg és adrenderg komponenseket is, amelyek összehangolják a talamokortikális aktivitását a megfelelő viselkedési állapottal. Mai ismereteink szerint az agytörzsben többségében olyan idegsejtek vannak, amelyeknek a szerotonin, illetve a noradrenalin az ingerületátvivő anyaguk. Ezek az idegsejtek szabályozzák azoknak a neuronoknak a működését, melyek az ítéletalkotásban, az emlékezésben és a tanulásban játszanak szerepet. A REM-alvás olyan idegsejtekkel van kapcsolatban, melyeknek az acetil-kolin az ingerületátvivő anyaga. Hobson és munkatársai (1989) szerint, amikor az ember az alvás NREM-szakaszában, illetve ébren van, a noradrenalin és szerotonin termelő agyitörzsi idegsejtek elnyomják az acetil-kolinnal működő társaikat. Ezzel ellentétben a REM-alvás során az idegsejtek felszabadulnak az inhibíció alól, és az acetil-kolin dominál. A folyamat során azok az agyi központok is ingerelt állapotban vannak, melyek a látással, a szemizom működéssel és az érzelmekkel kapcsolatosak, de az alvó egyed nem ébred fel, mert az acetil-kolin más csatornákon keresztül hat, mint a noradrenalin vagy a szerotonin. A Hobson elmélet szerint az acetil-kolin bénít, illetve érzéstelenít. Mivel az alvás szakaszai – mint említettük – ciklikusságot mutatnak, a noradrenalint és a szerotonint termelő idegsejtek felszabadulnak a gátlás alól, és újból elnyomják a kolinerg sejteket, ilyenkor megszakad a REM-alvás, és ha a körülmények adottak, az egyed felébredhet. (A.J.K. Phillips, P.A. Robinson, 2007)
Kolinerg sejtek és acetil-kolin
Az acetil-kolin, az elsőként felfedezett (Shute és Lewis, 1963) neurotranszmitter, a központi idegrendszer minden területén szintetizálódik, különösen magas koncentrációban agykéregben és a talamuszban.
A híd és a középagy találkozásánál található két elkülönített sejtcsoport, a laterodorsalis (LDT) illetve a nucleus tegmenti pedunculopontineus (PPN), melynek sejtjei acetil-kolint bocsájtanak ki, ez a neurotranszmitter serkenti a talamusz sejtjeit, hogy azok növeljék az elválasztási rátájukat, körülbelül egy perccel az előtt, hogy EEG diszinkronizációs állapota megjelent volna. Ezek a kolinerg neuronok transzmitterei különösen az intralamináris, a retikuláris és talamikus relésejtekre hatnak. Az acetil-kolin hatására a talamusz ingerli az agykérget, ennek hatására az ún. „bursting” üzemmódra vált, ennek következtében beáll a kortikális deszinkronizáció. Az LDT és a PPN neuronjainak változásai az alvás és ébrenlét mindegy egyes állapotában megfigyelhetőek, de az ébrenlét során az acetil-kolin kibocsájtás gyors, a NREM-alvás alatt lassú, még a SWS-alvás alatt nem észlelhető. A REM szakasz alatt az aktivitásuk hirtelen megnő, és felszabadulnak a gátlás alól. (Robert Ross MacLean, 2007)
A közelmúltban lezajlott kutatások után számoltak be arról, hogy a posterior PPN sejtek jelentős része elektromos kapcsoltságban áll. Úgy tűnik, hogy ez a hálózat teszi lehetővé az összehangolást és a ritmikus „bursting” rendszer fokozását. (E. Garcia-Rill és mtsai, 2007)
Adrenerg sejtek és a noradrenalin
A retikuláris aktivációs rendszer adrenerg része szorosan kapcsolódik a híd locus coeruleus-ának noradrenerg neuronjaihoz. A noradrenerg pályák párhuzamosak az előbb említett kolinerg utakkal, és emellett vannak közvetlenül felszálló ágai az agykéregbe és leszálló ágai a gerincvelőbe. Az adrenerg neuronok az ébrenlét és a SWS-alvás alatt magas aktivitásúak, még a REM-fázis alatt a „bursting” mechanizmus megszűnik. Emellett az adrenerg neurotraszmitterek hatása hosszabb távú, mint a kolinerg, mivel lassabban bomlanak le.
A legújabb kutatások kimutatták, hogy a nitrogén-monoxid, mint neuronális hírvívő is fontos szerepet játszik a noradrenerg neuronok modulálásában. A dendritek szabályozzák a talamusz vérellátását, melyben az ébrenlét és a REM-alvás során magas, még a SWS-fázis alatt alacsony a nitrogén-monoxid koncentráció. (S. R. Vincent, 2000)
Hypocretin/orexin neuronok
A közelmúltban felfedezett neuropeptidnek, a hypocretin-nek, vagy másnéven az orexin-nek szintén jelentős szerepe van az alvás-ébrenlét szabályozásában. A hypothalamus laterialis, posterior és perifornicalis területén elhelyezdő neuroncsoportok termelik ezeket a neuropeptideket, amelyek diffúz módon hatnak a központi idegrendszerre, azáltal, hogy aktiválják a RAS kolinerg és adrenerg összetevőit, valamint koordinálja a teljes retikuláris aktivációs rendszert. A hypocretin termelő neuronok az ébrenlét alatt a legaktívabbak, különösen a fokozott a termelésük a pszichomotoros aktivitás alatt, ezzel ellentétben jelentősen lecsökken a tevékenységük a NREM- és REM-alvás során. A hypothalamus laterialis, posterior és perifornicalis területén elhelyezdő neuroncsoportok termelik ezeket a neuropeptideket, amelyek diffúz módon hatnak a központi idegrendszerre, azáltal, hogy aktiválják a RAS kolinerg és adrenerg összetevőit, valamint koordinálja a teljes retikuláris aktivációs rendszert. A hypocretin termelő neuronok az ébrenlét alatt a legaktívabbak, különösen fokozott a termelése a pszichomotoros működés alatt, de jelentősen lecsökken a aktivításuk a NREM- és REM-alvás során. A hypocretin neuronokat a glutamát aktiválja, amely viszont növeli a hypothalamuszt körülvevő sejtek glutamát tartalmát, ez a pozitív feed-back rendszer részeként fenntartja a hypocretin termelő neuronok szintézisét. A legújabb kutatások bizonyították, hogy két féle hypocretin osztály létezik. A HcrtR1 felelős az alvás és az ébrenlét fenntartásáért, míg a HcrtR2 az ébrenléti izomtónusért felel. (S. Burlet, és mtsai, 2002)
Egyéb hormonok amelyek résztvesznek az ébredsztőrendszer működödésében
Hisztamin
A hisztamint tartják a fő ébresztő neurotranszmitternek, mivel bizonyított, hogy a H1-es receptorok agonistái indukálják az ébrenlétet, míg az antagonistái elősegítik az alvást. A hisztamin termelő neuronok aktivitása az ébrenlét alatt magas, a NREM alvás során csökken, míg a REM alvás során a legalacsonyabb. A H3 receptorok aktiválása csökkenti a hisztamin felszabadulást, ezzel kiváltja az alvást, míg a receptor blokkolása elősegíti az ébrenlétet. (M. M. Thakkar, 2011)
Szerotonin
A szerotonin fiziológiai effektusa az alvásra és az ébrenlétre vitatott. Felfedezése óta kimutatták az emlősök bélnyárkahártyájában és a központi idegrendszerben, valamint bizonyított a szerepe számos neuropszichiátriai rendellenességben, például a skrizoféniában, depresszióban, szorongásban és a Parkinson- kórban. A legújabb kutatások kimutatták, hogy a szerotonin hat az ébrenlétre, mennyisége az elalvás során nő, míg a REM alvás során csökken. A szerotonin alacsony szintje miatt alakul ki az insomnia, amely a 21. század leggyakoribb alvászavara. A szerotonint, új alvászavar-kezelő gyógyszerként alkalmazzák, használata több mint ígéretes a felmérések szerint. (Giuseppe Di Giovann, 2009)
Dopamin
A dopamin szerepe az alvás-ébrenlét szabályozásában még nem tisztázott. A farmakológiai álláspont szerint a DA olyan erős stimulussal bír mint az amfetaminok, amely bizonyítja az ébrenlét kialakításáért felelős tulajdonságát. A dopamin blokkolókat, mint az elalvássegítő faktorokat tartják számon. A legújabb kutatások szerint a Parkinson-kórban szenvedők, - akiknél a a substancia nigra és a ventralis tegmentum területén a dopamin ellátás hiányos – hasonlóságot mutattak azokkal a betegekkel akik narcolepsiában szenvednek. (Todd J. Swick, 2012)
|
Microébredések
A természetes pihenés folyamatát microébredéseknek nevezett fázikus jelenségek is kísérik. Ezeket nem, mint az alvást megszakító kártékony tényezőkként kell értékelni, hanem az ezzeljáró nélkülözhetetlen jelenségeknek. Ezek EEG, vegetatív és magatartási mutatókkal bírnak, de nem feltétel e három mutató együttes jelentkezése a microébredések során. Fontos megjegyezni, hogy ezen microébredések nem csak a REM fázisban vannak jelen, hanem a NREM-ben is amelyben az ébresztőrendszer az általánosságban elterjedt nézet szerint teljes gátlásban áll.
A microébredések szerepe abban áll, hogy fenntartsa az ébredés lehetőségét, ilyen módon az alvás ne egyezzen meg a kóma állapotával, de fenntartsa alvást is. A microébredések alvás során egyrészt információt közvetítenek az alvó agy számára, másrészt ébresztőimpulzusokat küldenek felé. Beállítják a szervezet külső és belső szükségleteinek megfelelően az alvásprogramot és az rugalmasan tud ezekhez alkalmazkodni.
|
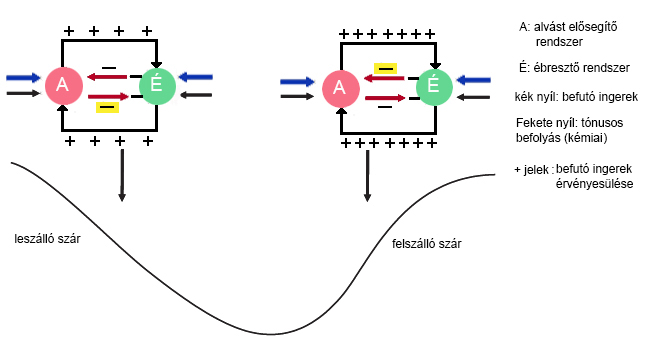
Az alvási ciklusok lefolyását, vagyis a REM, NREM fázisok szabályos váltakozását, a tónusos neurotranszmitterekkel történő hosszabb távú szabályozás mellett, a microébredésekkel járó fázisos szabályozás is befolyásolja, mely gyorsabb aktivációjú és ráépül az előbbi szabályozásra. Az alvási ciklusok szabályos váltakozását, a tónusos neurotranszmitterekkel történő hosszabb távú szabályozás mellett, a microébredésekkel járó fázisos szabályozás is befolyásolja, mely gyorsabb aktivációjú és ráépül az előbbi szabályozásra. Az alvási ciklusokat szinkronizációs és deszinkronizációs microébredések kísérik. Kimutatták, hogy ezeknek az alvás folyamatában különböző funkcióik vannak és megoszlásuk a ciklusokra nézve is eltérő; Az első alvási ciklusokra jellemzően a szinkronizációs, az alvás utolsó fázisaiban pedig a deszinronizáicós microébredések mutathatók ki leginkább. A microébredések szabályozása, így az alvást elősegítő és a vele antagonista, vagyis az ébresztő rendszer arányára vonatkozik, így alakul ki a személy pillanatnyi állapota. A ciklus leszálló szárán nő az alvást elősegítő rendszer aránya míg az ébresztő rendszeré visszaszorul. Ennek következményeképp csökken az afferens ingerekre adott válasz és a szinkronizáció fokozódik. A felszálló száron éppen ellentétesen, fokozódik az ébresztő rendszer dominanciája ennek hatásaként az ingerekre adott válaszok száma is megnő, mígnem bekövetkezik az ébredés. A két rendszer arányát alapvetően pedig az agyörzsi tónusos szabályozás szabja meg. (4. ábra) (Halász Péter, 2010)
Környezeti hatások
Fény
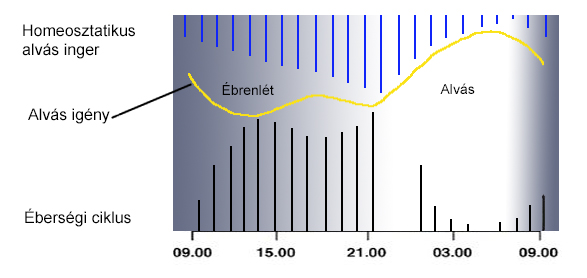
A reggeli órákban megvilágítás növekedése indukálta az ébredést, még a koraesti órákban a fényerőség csökkenése – mielőtt a hőmérséklet eléri a minimum értéket – az alvást segíti elő. (5. ábra) Megállapították, hogy nem szükséges a fényerőnek a napsugárzás intenzitását elérnie, hanem egy mesterséges izzolámpa is okozhat fáziseltolódást, ha a fény megjelenik a kritikus időben. Valamint azt is bizonyították, hogy az alvás-ébrenlét cirkád eltolódásával a vizelet kiválasztás, és a kortizol termelés ritmusa is megváltozik.
|
A reggeli órákban megvilágítás növekedése indukálta az ébredést, még a kora esti órákban a fényerőség csökkenése – mielőtt a hőmérséklet eléri a minimum értéket – az alvást segíti elő. Megállapították, hogy nem szükséges a fényerőnek a napsugárzás intenzitását elérnie, hanem egy mesterséges izzolámpa is okozhat fáziseltolódást, ha a fény megjelenik a kritikus időben. Valamint azt is bizonyították, hogy az alvás-ébrenlét cirkád eltolódásával a vizelet kiválasztás, és a kortizol termelés ritmusa is megváltozik.
Melatonin
A hormon termelésének kiindulópontja a triptofán, amelyből 5-hidroxitriptofan, szerotonin és N-acetilszerotonin köztestermék után keletkezik a melatonin. A melatonin szintézise, valamint kiválasztása, gyakorlatilag független az alvástól, legfőbb ingere a fény, illetve a sötétség. A glandula pinealis idegi összeköttetésben áll a retinával, a melatonin termelése itt megy végbe. A tobozmirigynek nincs tároló funkciója. A melatonin plazma koncentrációjának maximális értéke hajnali három és négy óra között mutatható ki, a nappal folyamán koncentrációja gyakorlatlag nulla. Ha a retinát éjszaka fény éri, akkor a melatonin koncentráció pár perc múlva jelentősen visszaesik. A melatonin a nucleus suprachiasmaticus-ba érkezik, amely szignálokat küld az agy különböző részeire, így kontrollálva a hormon termelést, a test hőmérsékletet és az álmosság érzetét. (Todd J. Swick, 2012)
Érdekességek
Az RAS további funkciója
A retikuláris aktivációs rendszer ébresztő funciója mellett, segít kialakítani az átmenetet a nyugodt ébrenlét és az aktív figyelő ébrenlét között. A fokozott éberséget és figyelmet ígénylő feladatok alatt a regionális vérámlás emelkedett a középagy formatio reticularis-ában és a talamusz intralamináris magjaiban.
Narkolepszia
A narkolepszia a központi idegrendszer eddig még ismeretlen eredetű krónikus betegsége. Olyan összetett szabályozási zavar, mely mind az alvást, mind az ébrenlétet érinti, de elsősorban a kettő ritmusát befolyásolja. A betegség lényege, az alvás – vagy álomfázis – ismételt betörése az éber állapotba. Legfőbb tünetei a feltartózhatatlan hirtelen, általában rohamokban jelentkező nappali álmosság, illetve elalvás, mely után 15-20 perccel a beteg kipihenten ébred. A narkolepsziához társulhat kataplexiás rosszullét, mely során a beteg váratlan érzelmi reakció (öröm, nevetés, meglepetés, félelem, düh) után eszméletvesztés nélküli tónusvesztése figyelhető meg.
Insomnia
Az insomnia – álmatlanság, elégtelen alvás – egy tartós alvási zavar, mely során a beteg alvási állapota zavart, illetve nem kielégítő. Ez az állapot kihat a nappali éberségre és hangulatra is, így együttjár a memória- és koncentrációzavarral, valamint fáradtságot és depressziót okozhat. A betegség az esetek döntő többségében szekunder, vagyis valamilyen testi vagy lelki betegség, kémiai anyag, pszichés állapot, életmódi vagy környezeti tényező váltja ki. Legtöbbször az előbb felsorolt tényezők együttesen váltják ki a rendellenességet. A primer insomnia ritka, kiváltó oka eddig még nem tisztázott.
Felhasznált irodalom
Dr. Fehér György (1980): A háziállatok funkcionális anatómiája III.
Burlet, S., Tyler, C. J., & Leonard, C. S. (2002): Direct and indirect excitation of laterodorsal tegmental neurons by hypocretin/orexin peptides: Implications for wakefulness and narcolepsy (Journal of Neuroscience)
Helli Merica, Ronald D. Futune (2004): State transitions between eake and sleep, and within the ultradian cycle, with focus on the link to neuronal activity
Jaime R. Villablanca (2004): Counterpointing the functional role of the forebrain and of the brainstem in the control of the sleep–waking system
Halász Péter (2006): A mikroébredések szerepe az alvás szerveződésében (Országos Pszichiátriai és Neurológiai Intézet, Epilepszia Centrum, Budapest)
Garcia-Rill E., Heister DS., Ye M., Charlesworth A., Hayar A. (2007): Electrical coupling: novel mechanism for sleep-wake control
A.J.K. Phillips, P.A. Robinson (2007): A Quantitative Model of Sleep-Wake Dynamics Based on the Physiology of the Brainstem Ascending Arousal System
Robert Ross MacLean (2007): Neurobiological mechanisms for the regulation of mammalian sleep–wake behavior: Reinterpretation of historical evidence and inclusion of contemporary cellular and molecular evidence
Giuseppe Di Giovann (2009): Serotonin and Sleep: Molecular, Functional and Clinical Aspects
Thakkar MM. (2011): Histamine in the regulation of wakefulness
Todd J. Swick (2012): The Neurology of Sleep