A Helicobacter pylori baktérium hatása a gyomor élettanára
Contents
- A Helicobacter pylori baktérium hatása a gyomor élettanára
Helicobacter-baktériumok általános jellemzése
A Helicobacter fajok gram-negatív, spirális alakú, mozgékony, ostoros baktériumok (Neiger és Simpson, 2000). A Helicobacter pylorit (H. pylori) Warren és Marshall izolálta először 1983-ban emberi gyomorszövetből. (Hwang és mtsai, 2002) A gyomor alacsony pH-jának is ellenállnak, a gyomor nyálkahártyáját borító nyálkarétegben, mirigyeiben és parietális sejtjeiben telepszenek meg és szaporodnak el (Hwang és mtsai, 2002). A H. pylori a legelterjedtebb emberi gyomor-bélrendszeri kórokozó; a világ emberi népességének mintegy felének gyomrát kolonizálja, különösen a társadalmi-gazdasági kihívásokkal küzdő régiókban. (Plósz, 2019; Martin és mtsai, 2013). A fertőzöttek kisebbségében a H. pylori peptikus fekélyeket (10–20%), gyomorrákot (1-2%) és ritkán nyálkahártyával társított limfoid szövet (MALT) lymphomát okozhat. Ha jelen van, ez a baktérium uralja az ember gyomor mikrobiomját és antimikrobiális reakciókat vált ki a gazdaszervezetben (Martin és mtsai, 2013). A legújabb bizonyítékok azt mutatják, hogy az orgaznizmusok sikeres felszámolása megakadályozza a bélfekély súlyosbodását. Így a H. pylori diagnózisa és kezelése ma már egyre nagyobb jelentőségű a fekély menedzselésében (Ho és mtsai, 1991).
Helicbacter spp. a különböző fajokban
Az emberek mellett állatokban is találkozhatunk Heliocobacter baktériumfajokkal. A különböző egyedekből izolált H. pylori törzsek rendkívül változatosak (Neiger és Simpson, 2000). Legalább 38 különböző Helicobacter-fajt azonosítottak állatokban, és a fertőzött állatok egyszerre több fajt is hordozhatnak. A H. canis, H. felis, H. heilmannii és H. bizzozeronii gyakoribbak kutyákban és macskákban (Blois, 2016). Ezek az organizmusok morfológiailag megkülönböztethetők a H. pyloritól, szorosabban tekercselt testformájukkal és nagyobb méretükkel (0.5 x 5–10 μm), de a különböző Helicobacter-szerű organizmusokat egymástól nem lehet megkülönböztetni sem fénymikroszkóppal, sem elektronmikroszkóppal, ezért együttesen "gasztrikus Helicobacter-szerű organizmusoknak (GHLO - gastric Helicobacter-like organismus)" nevezik őket (Hwang és mtsai, 2002). Átlagosan a macskák 85%-a, a kutyák 90-100%-a, a menhelyi kutyák és a laboratóriumi beagle-k 100%-a fertőzött. Visszatérő hányás miatti gyomorbiopsziás vizsgálatnál a macskák 57-76%-ánál, a kutyák 61-95%-ánál mutatták ki a GHLO-t (Neiger és Simpson, 2000). Ezeken kívül más fajokban is megtalálhatóak ezek a baktérium, mint például a gyomorfekélyes sertésekben (Helicobacter heimannii), a súlyos gasztritiszben szenvedő gepárdokban (Helicobacter acinonychis), görényekben (Helicobacter mustelae), majmokban (Helicobacter nemestrinae), rágcsálókban (Helicobacter muridarum) és a delfinekben (Hwang és mtsai, 2002). A gyomor Helicobacter-fajok mellett számos intestinalis és hepaticus Helicobacter fajt is leírtak. Kutyák és macskák ürülékéből izolálták a H. cinaedi, H. fenneliae, és ‘‘F. rappini’’ fajokat. A H. colifelis-t egy súlyos hasmenésben szenvedő macskánál írták le, a H. canisról pedig hasmenéses és hasmenés nélküli kutyákban számoltak be (Neiger és Simpson, 2000).
|
A baktérium élettani hatásai
A kórokozó megváltoztatja a gyomor fiziológiáját, pl. a gyomor gyulladását indukálja, (megzavarja a foszfolipázokat, vakuolizáló toxinokat választ ki és apoptózist vált ki) vagy megváltoztatja a gyomor szekréciós tengelyét a szomatosztatin felszabadulásának csökkenésével, hypergastrinaemia kiváltásával, a parietális sejtek reakciókészségének csökkentésével. Emberekben a fertőzés összefüggésbe hozható bizonyos gyulladásos citokininek termelődésével (Interleukin-1, IL-a, IL-8 és tumor necrosis factor-alpha – TNF). Ezeknek a termelődését összekapcsolják a gasztrin, szomatosztatin és a sav szekréció megváltozásával, valamint a gyomorhurut és fekély kialakulásával (Neiger és Simpson, 2000). A baktérium által legnagyobb mennyiségben termelt ureáz a karbamidot (ureát) ammóniára és széndioxidra bontja. Az ammónia képes ellensúlyozni a gyomor savas pH-ját, másrészt toxikus hatással bír a nyálkahártya sejtjeire és kémiai úton odavonzza a granulocytákat, melyek helyi gyulladásos választ idéznek elő, ami fokozza a hámsejt károsodását. A kóros mikrobiotát a betegségek egyre hosszabb listájával társítják, beleértve a gyulladásos bélbetegségeket, az elhízást és az atópiás betegségeket, mint például az ekcéma és az asztma (Martin és mtsai, 2013).
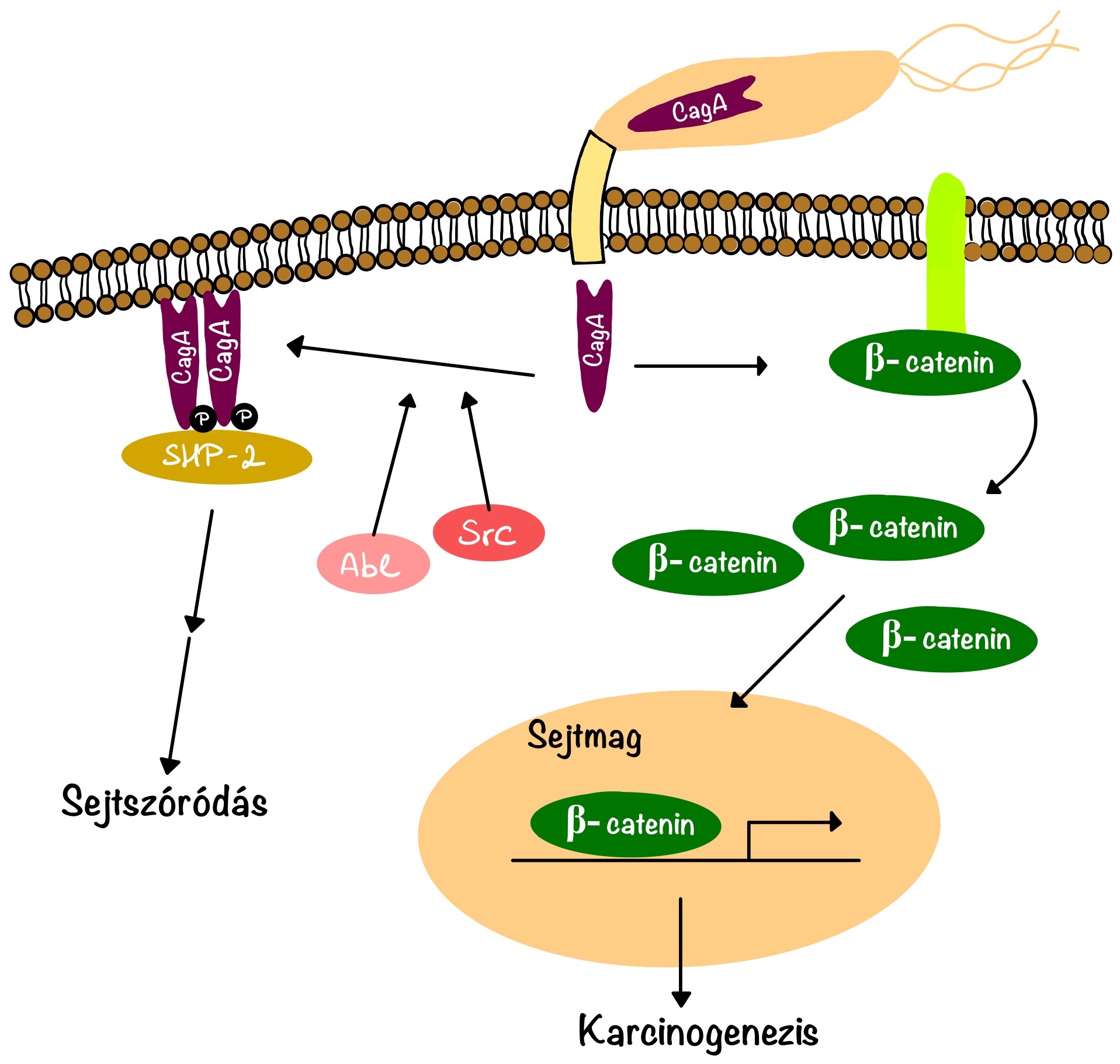
Az egyik mikrobiális determináns, amely növeli a betegség kockázatát, a cag patogenitási sziget. A H. pylori cag+ törzsek növelik a peptikus fekély és a disztális gyomorrák kockázatát azokhoz a törzsekhez képest, amelyekből hiányzik ez a cag sziget. Az intracelluláris CagA tirozin-foszforiláción megy keresztül, és aktiválja az eukarióta foszfatázt (SHP-2), valamint az ERK-t (extracelluláris jel által aktivált kinázokat) (1. ábra). A nem foszforilált CagA szintén hatásokat fejt ki a sejten belül, amelyek szerepet játszanak a karcinogenezisben. Ez az effektor egy bakteriális onkoprotein, amely bizonyítja, hogy a CagA képes csillapítani az apoptózist, és hogy a CagA transzgenikus expressziója egerekben gyomor karcinóma kialakulásához vezet. A szekretált bakteriális toxint (VacA) kódoló vacA egy másik H. pylori lokusz. A VacA apoptózist indukál, és növeli a szerves molekulák, a vas és a nikkel paracelluláris permeabilitását (Peek, 2008).
A H. pylori komponensek mellett az emberi IL-1β gén promoterén belüli olyan polimorfizmusok vannak, amelyek lehetővé teszik az IL-1β (gyulladáscsökkentő citokin) fokozott expresszióját, növelik a gyomor adenocarcinoma kockázatát. Ezek a kapcsolatok csak a H. pylori-kolonizált személyek között vannak, hangsúlyozva a gazda-környezet kölcsönhatások fontosságát a gyomorrák kialakulásában. A magas kockázatú IL-1β polimorfizmusban szenvedők között, akiket H. pylori cag+ vagy toxigén törzsek is fertőznek, a gyomorrák relatív kockázata tovább nő, 25, illetve 87-szeresére a kiindulási értékhez képest. Ez azt jelzi, hogy a specifikus gazda és mikrobiális determinánsok közötti kölcsönhatások biológiailag jelentősek a gyomorrák kialakulásában (Peek, 2008).
Helicobacter spp. macskáknál
Történtek vizsgálatok arra vonatkozóan, hogy van-e összefüggés a Helicobacter spp. általi fertőzések és a gyomor elváltozásai, valamint a nyálkahártya hámjának proliferációja között. A gyomornyálkahártya mintáit 23, 8 hónapos és 13 éves kor közötti macskától gyűjtötték össze. A macskák közül tizennyolc egészséges volt, öt állatnál pedig krónikus hányás volt tapasztalható. Egyik állat sem kapott gyógyszeres kezelést az azt megelőző hónapban (Takemura és mtsai., 2009). A pylorus antrum, a corpus és a fundus nyálkahártyájának mintáit gasztroszkópiával gyűjtötték össze. A Helicobacter spp. jelenlétét polimeráz láncreakcióval (PCR) vagy Warthin-Starry (WS) festéssel igazolták. A nyálkahártya elváltozásokat a hematoxilin és az eozin (HE) által festett metszetek vizsgálatával értékelték, a hámproliferációt pedig a nukleoláris szervező régiók (AgNOR) felsorolásával határozták meg. 20 (87%) macskában Helicobacter spp. jelenlétét mind a PCR, mind a WS megerősítette. A H. heilmannii volt a leggyakrabban azonosított faj (20 macskából 17), a H. felis pedig csak együttes fertőzésben (17 macskából 2) volt jelen (Takemura és mtsai, 2009).
A lamina propria szövettani változásai közé tartozott az enyhe mononukleáris gyulladásos infiltráció, a limfoid tüszők jelenléte, a fibrózis és a mirigy degenerációja. Ezek a változások a pylorus bejáratnál voltak a legsúlyosabbak. Jelentős összefüggés volt a gyomor Helicobacter spp. fertőzés között és a limfoid tüszők jelenléte (P = 0,03), valamint a fertőzés és a hámproliferáció között az antrumban (P <0,01), a corpusban (P <0,001) és a fundusban (P <0,001). Nem találtak összefüggést a Helicobacter spp. kolonizáció mértéke és a lamina propria mononukleáris infiltrációjának súlyossága között (P> 0,05). Tizenöt minta tartalmazott 1-5 limfoid aggregátumot a lamina proprián belül. Esetenként fibrózis és mirigy-degeneráció volt a limfocita infiltráció kísérője, azonban nem volt összefüggés a Helicobacter spp. jelenléte és a gasztritisz, a mirigy degeneráció és a lamina propria fibrózisa között. Mirigy degenerációt és a lamina propria fibrózisát gyakran megfigyelték a vizsgált fertőzött macskáknál. A mirigy elváltozása összefüggésben van a fibrózissal, a lamina propria gyulladásával és Helicobacter spp. patogenitásával, bár ezt csak fertőzött macskákban figyelték meg, nem sikerült összefüggést találni Helicobacter spp. fertőzés kapcsán. A 15 fertőzött macska közül 13 esetben limfoid tüszők jelentek meg egyidejűleg azzal, hogy mononukleáris sejtek infiltrálódtak a lamina propriába. Összességében ezek a megfigyelések arra utalnak, hogy a H.pylori fertőzés immunválaszt vált ki, ami limfoid tüszők képződésével jár a macskák gyomornyálkahártyájában (Takemura és mtsai, 2009).
Helicobacter spp. kutyában
A közelmúltban 4-6 hónapos beagle kölyköket fertőztek meg kísérletileg egérrel adaptált H. pylori törzzsel. Valamennyi kutya krónikus gasztritiszt mutatott 4 héttel a H. pylori és H. felis beoltása után és az éhgyomri pH is növekedett 10-ből 4 megfertőzött kutyánál. Ezzel szemben az SPF (meghatározott kórokozóktól mentes) kutyák 6 hónap elteltével sem mutattak összefüggést H. felis fertőzés és a gyomor gyulladásával kapcsolatban. Ezeknek a kutyáknak a gyomorbiopsziája enyhe gyomorgyulladást és limfoid tüszőket mutatott ki mind a fertőzött, mind a nem fertőzött kutyákban. Nem találtak összefüggést a megfigyelt organizmusok száma és a gyomorgyulladás mértéke, ill. a limfoid tüszők száma között (Neiger és Simpson, 2000).
A H. pylori fertőzés hagyományosan a kölyökkutyákban okoz hányást és laza székletet röviddel az oltás után. 1 hetes fertőzés után ezek a kutyák markáns polimorfonukleáris leukocita infiltrációt mutattak a lamina propriában, amely a következő néhány hétben krónikus follikuláris gyomorhuruttá változott kis limfoplazmatikus aggregátumok és limfoid tüszők jelenlétében. Ezenkívül az IL-8-at a fertőzés 1. és 2. hete után immunhisztokémiai úton detektálták a gyomor azon területeiről, ahol a neutrofil transzcitózis a legkifejezettebb volt és kimutathatatlanná vált a 8. héttől kezdődően vett biopsziákban, amikor a neutrofil infiltráció sokkal kevésbé volt látható, mint a korai fázisban fertőzés (Neiger és Simpson, 2000).
Terjedése
A helicobacter terjedésének a pontos módja még nem világos. Egyesek a széklettel való terjedést feltételezik mert a H. pylori ember és macska székletéből is egyaránt tenyészthető és egyes országokban a nem optimális egészségügyi feltételek elősegíthetik az ilyen terjedést. Lehetséges a Helicobacter fertőzések kutyáktól és macskáktól való átterjedése az emberre is (Blois, 2016). Más elméletek az orális terjedést feltételezik, mert a H. pylori kimutatható fertőzött emberek nyálából. A H. pylorit a közelmúltban izolálták felszíni vizekből is az Egyesült Államokban és Svédországban, ami arra utal, hogy a víz által okozott fertőzés fontos útvonal lehet (Neiger és Simpson, 2000).
Állatkísérletek
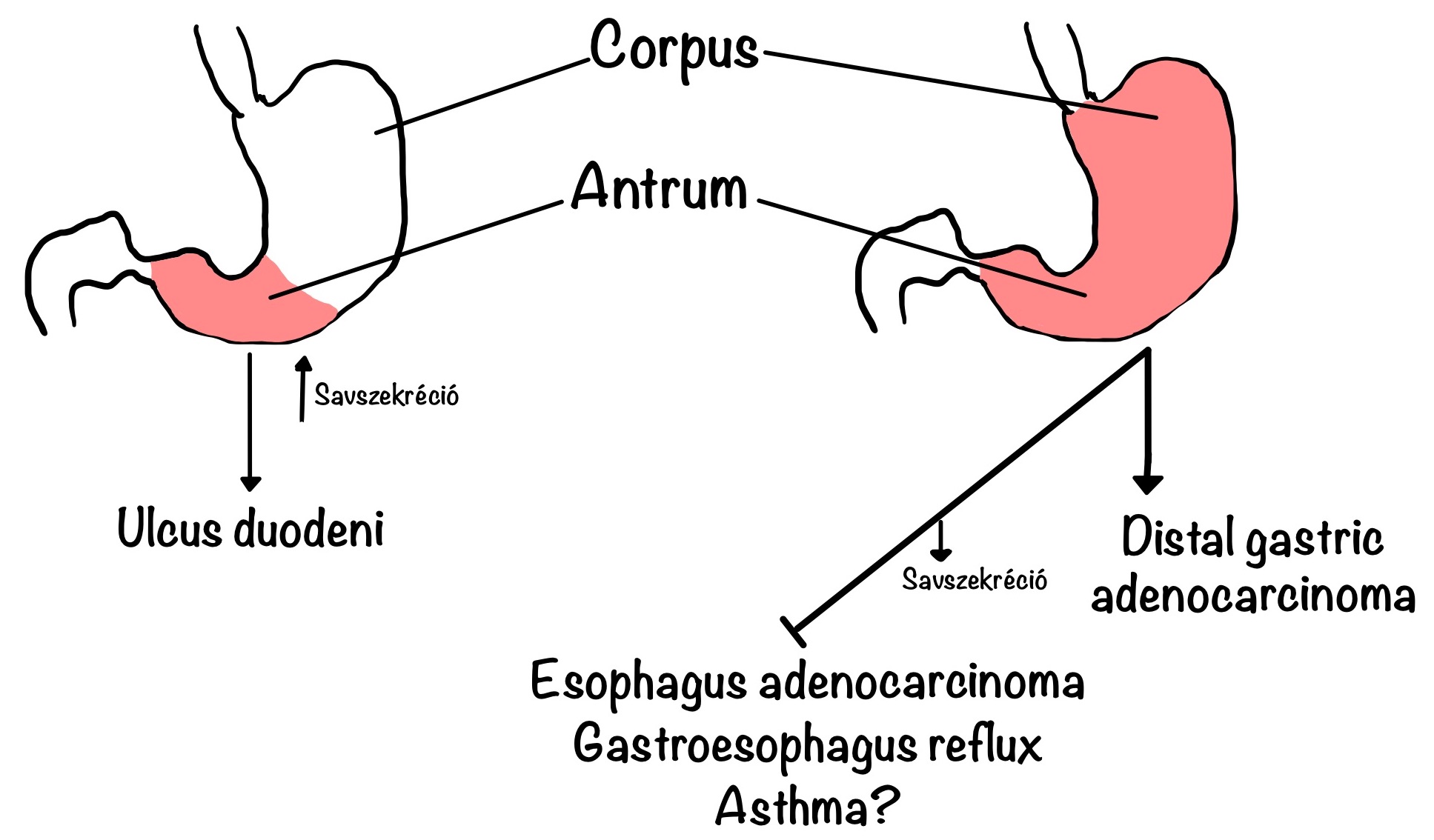
A H. pylori által kiváltott betegségek miatt állatkísérletek használata vált szükségessé, hogy pontosabban meghatározzuk azokat a mechanizmusokat és a környezeti tényezőket, amik szerepet játszanak a karcinogenezis kialakulásában (Neiger és Simpson, 2000). Modellként rágcsálókat és főemlősöket használtak. Az egér legtöbb törzsében nem alakult ki rák, csak enyhe gyulladás lépett fel a fertőzést követően. Bár a főemlősök állnak evolúciósan a legközelebb az emberhez, és ennél fogva célszerű lenne leginkább őket tanulmányozni, a majmokon végzett kísérletek nem hajthatók végre ugyanolyan nagyságrendben, mint a rágcsálókon (Peek, 2008). Vad típusú H. pylori-nak a cagA vagy cagY mutánsaival fertőzött futóegereken a gyulladás intenzitását vizsgálták. A vad típusú H. pylori-val fertőzöttekhez képest a cag mutánsokkal fertőzött futóegéreknél kevésbé súlyos gyomorhurut alakul ki. A cagA vagy cagY elvesztése olyan gyulladásos választ eredményezett, amely elsősorban a gyomor antrumára korlátozódott. A szövettani változásoknak megfelelően az intragasztrikus pH-értékeket csak a vad típusú H. pylori törzzsel fertőzöttekben növelték. Ezek az eredmények azt mutatják, hogy funkcionális cag-szekréciós rendszerre van szükség a corpus-domináns gasztritisz előidézéséhez (2. ábra), (Peek, 2008).
A vad típussal fertőzött egerek nem annyira érzékenyek a H. pylori által okozott fertőzésre. Emiatt H. felis kórokozót használtak a gyomor sérülésének kiváltására és a gyomor károsodásának mértéke általában súlyosabb a H. felissel fertőzött egereknél, mint a H. pylorival. A gyomor adenokarcinoma a vad típussal fertőzött egerekben H. felissel való fertőződés során is kialakulhat. Számos H. pylori virulencia komponens, például a cag patogenitási sziget és a vacA azonban nincs jelen a H. felis genomjában, ami korlátozza a H. pylori és az emberek közötti kapcsolatot (Peek, 2008).
Egy tanulmány H. pylori-fertőzött rhesusmajmokkal vizsgálta a gének expresszióját a cag-szigeten. Ezek az adatok azt mutatták ki, hogy a cagA magas szinten expresszálódott a fertőzés teljes időtartama alatt. Érdekes módon egyes cag gének, mint például a cagY, a fertőzés után 1 héttel jobban kifejeződtek a későbbi időpontokhoz képest, míg mások, például a cagC expressziója 2 és 3 hónap között nőtt, majd 4-6 hónappal később csökkent. Így ezekből a független állatmodell-rendszerekből nyert adatok azt jelzik, hogy a CagA és a cag patogenitási sziget más termékei fontos szerepet játszanak a H. pylori által kiváltott betegség, különösen a gyomorrák kialakulásában (Peek, 2008).
|
Kimutatás:
A diagnosztikai tesztek invazív tesztekből állnak, mint például gyors ureáz teszt, hisztopatológia, citológia, tenyésztés, PCR, elektronmikroszkópia (gyomortükrözés során vett szövetmintából/ biopsziás mintából) és noninvazív vizsgálatokból, mint urea-kilégzési Helicobacter teszt és vérvétel során ellenanyagok kimutatása, szerológiai vizsgálat nyálból, székletvizsgálat (Neiger és Simpson, 2000).
Invazív tesztek
A gyors ureáz-próba szinte az összes gyomor Helicobacter spp. ureáz termelésén alapul. Gyomorbiopsziát inkubálunk karbamidlevesben, amely pH-indikátorként fenolvöröst tartalmaz. Amint az ureáz ammóniára bontja a karbamidot, a pH emelkedik és színváltozás következik be. A háziállatokból származó minták általában 1-3 órán belül értékelhetők. Emberekben a színváltozás gyorsasága némileg arányos a H. pylori mennyiségével. A hisztopatológia a Helicobacter organizmusok megfigyelésére támaszkodik a gyomor biopsziás szövetében. Különleges festések, például Giemsa vagy toluidinkék javítják a GHLO láthatóságát (Neiger és Simpson, 2000). Gyomorbiopsziát a gyomor több területéről kell venni, mert Helicobacter eloszlása eltérő lehet a gyomor különböző pontjain (Blois, 2016). A citológia teszt Gram vagy Diff Quika festéssel egyszerű, gyors és érzékeny diagnosztikai teszt. A Helicobacter fajok azonosításának másik módja a pozitív tenyészetek Dotblot DNS hibridizációja vagy PCR-je. PCR vizsgálat lehetővé teszi a biopsziás mintából vagy a gyomornedvből kivont DNS által a Helicobacter fajok diagnosztizálását és azonosítását. A PCR-termékeket ezután klónozhatjuk és szekvenálhatjuk vagy elemezhetjük restrikciós fragmens hosszának polimorfizmusával a faj és a törzs azonosítására. A Helicobacter fajokat morfológiailag elektronmikroszkóppal akarták először megkülönböztetni egymástól, de más vizsgálatok azonban kimutatták, hogy a tenyésztett Helicobacter spp. elveszíthetik tipikus in vivo morfológiai jellemzőiket. A természetesen megszerzett Helicobacter fertőzés diagnosztizálásához kutyákban és macskákban a gyors ureázvizsgálat, a hisztopatológia és az citológia nagyon pontos. Ha a fertőző baktériumok sűrűség alacsony, a PCR pontosabb vizsgálatnak tűnik, mint a módosított Steiner-festés és a gyors ureáz-teszt (Neiger és Simpson, 2000).
Nem invazív tesztek
Az enzyme-linked immunosorbent assay vizsgálattal (ELISA) vagy immunblottolással végzett szerológiát széles körben használják diagnosztikai eszközként a humán klinikákon és az epidemiológiai vizsgálatok során. A legpontosabb ELISA teszt készletek a H. pylori eredetű különféle antigéneken alapulnak és mérik a keringő immunglobulin G-t (IgG) a szérumban. Az IgG vagy IgA a gyomornedvben is mérhető. A fertőzés diagnosztizálásán túl immunblotot alkalmaztak a H. pylori immunogén részeinek meghatározására, vagy kétértelmű ELISA teszt eredményeinek vizsgálatára. A karbamid lélegzet- és vérvizsgálat során stabil 13 C-val vagy radioaktív 14 C-val jelölt karbamidot alkalmaznak. A Helicobacter spp. által előállított ureáz az elfogyasztott jelölt karbamidot ammóniává hasítja. A felszabadult, jelölt C atomok felszívódnak a keringésbe és kilégzésre kerülnek. A kilégzett levegőt összegyűjtjük, és 13 C-karbamiddal a 13 CO2 és 12 CO2 arányát tömegspektrometriával mérik, míg a radioaktív CO2 mennyiségét 14 C-karbamiddal elemezzük. A 13 CO2 és a 12 CO2 aránya vérmintában is mérhető. A protonpumpa-gátlók és a hisztamin H2-receptor antagonisták azonban csökkentik a Helicobacter spp. ureáz aktivitását, ezért fontos az antibiotikum és antiszekréciós alkalmazás utáni tesztelés ideje. A kezelés abbahagyása után legalább 2–5 napos szünetet kell tartani. Ezenkívül az alacsony gyarmatosítási szint sok hónapig fennmaradhat, és a korai tesztelés elmaradhat (Neiger és Simpson, 2000).
Terápia
Az emberek H. pylori fertőzéseit kettős vagy hármas antimikrobiális szer-terápiával, valamint sav-szekréciós gátlóval (pl. klaritromicin, amoxicillin + bizmut és ranitidin) 2 hétig kezelik, valamint az állatgyógyászatban is hasonló terápiás megközelítéseket alkalmaztak. Jelenleg a Helicobacter szerepe a gasztritisz kórokozójaként kutyákban és macskákban nem egyértelmű. Az ajánlott kezelési módok közé tartozik az amoxicillin vagy a tetraciklin, a metronidazol, a bizmut szubszalicilát és a protonpumpa inhibitor (pl. omeprazol) vagy a H2-receptor blokkoló (pl. famotidin) 2-3 hétig. De írtak már más kombinációt is, mint omeprazol és azitromicin vagy klaritromicin. Noha sok, a fenti kombinációkkal kezelt kutyánál és macskánál nem sikerült megszabadulni a Helicobacter fertőzéstől hosszú távon újratesztelések alapján, a hányás gyakorisága és a gyomor elváltozásai sok beteg esetében javult (Blois, 2016).
A fertőzés potenciális előnyei
Noha a H. pylori jelentős kockázati tényezőt jelent a felső gasztrointesztinális traktus súlyos betegségei szempontjából, ennek a kórokozónak az epidemiológiája gyorsan változik, különösen a fejlett országokban. A H. pylori az USA-ban a 10 évesnél fiatalabb gyermekek körülbelül 10%-ában van jelen, szemben a 60 évesnél idősebbek 50-60%-ával. Mivel ebben az országban a felnőttek körében a H. pylori megjelenésének aránya <1% évente, a legtöbb kolonizált felnőtt valószínűleg fertőzését gyermekkorban szerezte meg. A legtöbb fiziológiai vizsgálat azt jelzi, hogy az antrum tájékán jelenlévő gasztritiszben szenvedő betegeknél a gyomor savassága megnövekedett, míg a pangasztritiszben szenvedő H. pylori pozitív alanyoknál a savszekréció sebessége gyengül (2. ábra) (Peek, 2008).
A parietális sejtek működésének gátlásával és/vagy az atrófiás gyomorhurut kialakulásának felgyorsításával a savat szekretáló corpusban a cag pozitív törzsek által kiváltott fokozott gyulladás tompíthatja a nyelőcső reflux (GERD) és következményeinek kialakulásához szükséges savszekréció szintjét. Számos keresztmetszeti vagy esettanulmány-vizsgálat kimutatta, hogy a H. pylori fertőzés és az asztma, az atópiás allergiás nátha és/vagy az ekcéma között jelentős fordított összefüggés van jelen. Ezenkívül ezek a kölcsönös kapcsolatok leginkább a cag pozitív törzsekkel fertőzött fiataloknál jelentkeznek. A H. pylori a gazdaszervezet immunválaszát manipulálja, ideértve a T-szabályozó sejtek aktiválódását is, ami viszont tompíthatja a környezeti allergének elleni immunmoduláló aktivitást. A kutatók és klinikusok egy alcsoportja úgy véli, hogy esetleges pozitív hatásai ellenére a H. pylori felszámolása a közegészség szempontjából a legjobb, a fertőzés és a peptikus fekélyek vagy a rák közötti pozitív összefüggés miatt (Peek, 2008).
Irodalomjegyzék
Blois SL (2016); Helicobacter Infection in Small Animals, The Merck Veterinary Manual, 394-396
Felhasznált weboldalak
Emésztőrendszeri megbetegedések - A Helicobacter pylori
Gyomor és nyombélbetegségek okozója - Helicobacter pylori
Ábrajegyzék
Peek RM (2008): Helicobacter pylori infection and disease: from humans to animal models. Disease Models & Mechanism 1: (1) 50–55. cikk ábrái alapján készült saját rajz.