Kutyákat és macskákat érintő immunmediált hemolitikus anémia
Hallgatói lecke 2018
Horváth Ariella Roxána
Lőrincz Viktória
Mónus Fanni Márta
Contents
Rövid összefoglaló
Autoimmun betegségről akkor beszélünk, ha az immunrendszer támadó választ indít a test valamely saját struktúrája ellen (Balch és Mackin, 2007).
Az immunmediált hemolitikus anémia a vérszegénység gyakran előforduló formája kutyákban és macskákban, mely során a szervezet saját vérének pusztításába kezd, ennek eredményeképp felgyorsul a VVS-állomány fogyása. Előfordulhat idiopátiás (elsődleges) formában, ám jellemzőbb a másodlagos változat, azaz egy fertőző vagy daganatos betegség következményeként lép fel.
A betegségben főképp a középkorú szuka kutyák érintettek, a fajták közül pedig az amerikai cocker spánielek és az angol springer spánielek.
Az általánosan fellépő tünetek a súlyos anémia és az azzal járó gyulladásos reakció. Jelenleg nem áll rendelkezésünkre speciális gyorsteszt a betegség diagnosztizálására, ám fontos jelző lehet a hemolitikus anémia fiatal-középkorú kutyákban vagy a gyakorta érintett fajták egyedében; autoaggluináció és/vagy spherocyták jelenléte; pozitív Coomb’s teszt; a többi vérszegénységet kialakító változó kizárása; a jellegzetes reakció az immunszupresszív terápiára (Balch és Mackin, 2007).
A legújabb kutatások és terápiás kezelések ellenére a halálozási ráta még mindig kifejezetten magas (kb. 50%)
Fogalmak
A vörösvérsejtek relatív hiányát vérszegénységnek (anémia) nevezzük. Számos örökletes és egyéb betegségben központi szereppel bír a vörösvérsejtek genetikai hibája (sarlósejtes anémia), a B-12 vitamin hiánya (vészes vérszegénység, anemia perniciosa), de a probléma forrása lehet a vas elégtelen bevitele vagy felszívódásának zavara is. Számos esetben a nem megfelelő étkezés (alkoholizmus, egyoldalú étrend), alapvető alultápláltság (fehérjehiány), krónikus mérgezések (pl. ólom), valamit pusztíthatják kórokozók is (malária). Súlyosabb vérveszteség is lehet a vérszegénység átmeneti okozója.
|
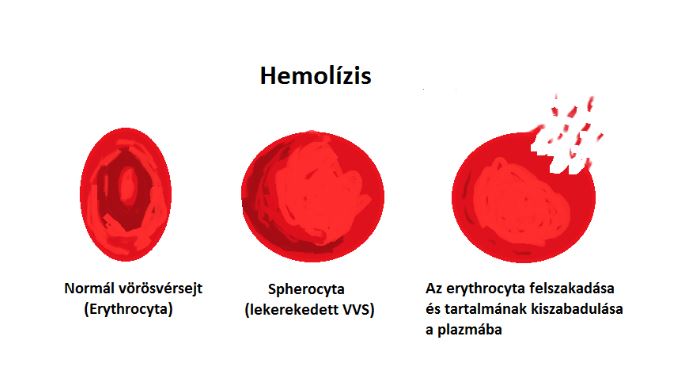
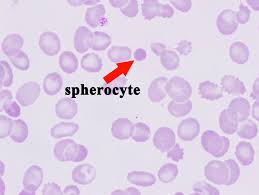
Spherocytózis {2. ábra}
Ez egy autohemolitikus anémia típus. Legfőbb jellegzetessége a spherocyták vagy erythrocyták produkciójában rejlik, hiszen a sejtek elvesztik bikonkáv alakjukat, ehelyett lekerekednek. Az örökletes sherocytózis és immunhelolitikus anémia esetén CSAK spherocyták keringenek az erekben.
Az okozó egy molekuláris hiba a VVS citoszkeletonjának egy vagy több fehérjéjében alakul ki (spektrin, ankyrin, Band3, Protein 4.2.). A váz deformitása miatt a sejt gömbalakot vesz fel, hiszen az bír a legkisebb felületi feszültséggel. A változás lekicsinyíti a sejt külső felszínét, így kisebb felületen tud oxigént és széndioxidot cserélni. Magas ozmotikus „törékenységgel” bírnak, vízbe helyezve sokkal könnyebben sérülnek mint a normál VVSek. Összességében hajlamosabbak a pusztulásra.
A számos közös pont ellenére az örökletes spherocytózis és az IMHA mégis könnyen elkülöníthető egymástól, hiszen csak az utóbbi ad Coomb’s tesztre pozitív eredményt. Az eltorzult, de egyébként egészséges VVS-eket a lép tévesen elöregedett/sérült sejteknek véli, ezért kivonva őket a forgalomból, elkezdi a lebontást. Így a folyamat során a test a saját vér, ezáltal oxigénellátását teszi tönkre (autohemolízis). A vérben csökken a hemoglobin és hematokrit érték, emellett megnő a retikulocyták aránya, ami intenzív vérsejt-képzésre utal.
|
A betegség okai, előfordulása
Az immunmediált haemolitikus anémia kutyáknál sokkal gyakoribb betegség mint macskáknál. Bármely kutyafajtánál jelentkezhet az IMHA, de a cocker és angol springer spánielekre, az ír szetterekre, a juhászkutya fajtákra, főként a hosszúszőrű skót juhászkutyára, a bichon frisékre, a finn spiccekre valamint az uszkárokra a legjellemzőbb. A szukáknál és a 6 év körüli kutyáknál egyes tanulmányok szerint nagyobb valószínűséggel fordul elő, a veszélyeztetett korosztály mégis igen tág határok, 1-13 év között mozog. A vércsoportok közül a DEA4 melynél a leggyakoribb az immunmediált haemolitikus anémia. A megbetegedések sűrűbben jelentkeznek tavasszal és nyáron, főként a melegebb hónapokban, májustól júniusig, mely a kullancscsípések által terjesztett betegségekre (mint például a babesiosis) vezethetőek vissza (Balch és Mackin, 2007).
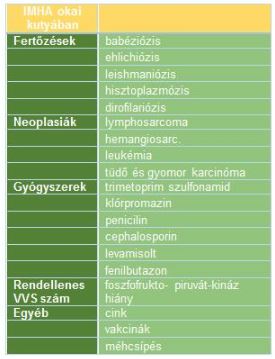
Több kór szövődményeként is jelentkezhet {3. ábra}. Előfordulhat fertőzések, neoplasia, gyógyszerek mellékhatásaként, az intrinsic/ keringő vörösvérsejtszám (RBC) vagy egyéb rendellenesség tüneteként (Balch és Mackin, 2007).
A leggyakoribb fertőzés a babesiosis, mely egy a kullancsok által terjesztett, egysejtű parazita okozta megbetegedés. Magyarországon főként nyugaton és az Északi-középhegység területén, de az őszi, tavaszi szezonban szinte bármely füves, gazos területen veszélyeztettek a kutyák a kullancscsípéssel szemben (Lobetti és mtsai, 2002). Másik, szintén kullancsok által terjesztett kór az ehrlichiosis, melyet egy baktérium ( Anaplasmataceae Ehrlichia és Anaplasma) generál. Az IMHA esetleges jele lehet a leishmaniosisnak is, mely szintén egysejtű (Leishmania donovani, Leishmania infantum) okozta és szúnyog által terjesztett fertőzés. A homoki vagy lepke szárnyú szúnyog elsődlegesen a Földközi tenger környékén fordul elő és okoz megbetegedéseket, de már északabbra is regisztráltak eseteket, Svájc, Németország és Belgium területén (Travi és mtsai, 2002). További ismert fertőzés még a dirofilariózis és a hisztoplazmózis (Balch és Mackin, 2007).
Másik releváns oka az immunmedált hemolitikus anémiának a neoplasia, mely szövetek, szervek rendellenes növekedését, a rossz- és jóindulatú daganatos megbetegedéseket foglalja magába. Ilyen kór a lymphosarcoma vagy más néven lymphoma, mely a nyirokrendszert támadja illetve a hemangiosarcoma, vagyis a vérerek daganatos megbetegedése. Leukémia, gyomor- és tüdőkarcinóma is jelentős előidézői az IMHA-nak (Balch és Mackin, 2007) (Mellanby és mtsai, 2004).
|
A keringő vörösvérsejtszám rendelleneségei közül a foszfofrukto-kináz és a piruvát-kináz hiány, valamint az örökletes ozmotikus fragilitás okozhatnak immunhaemolitikus anémiát. Egyéb kiváltó okok a cink anyagcsere zavara, egyes vakcinák vagy a méhcsípés (Balch és Mackin, 2007).
Adódhatnak mérgezések melyek tünete az immunhaemolitikus anémia. Egyik ritka, de súlyos betegség a paxilluszszindróma, melyet a cölöpgomba (Paxillus involutus) okoz. A kóros állapotot nem is közvetlenül a toxin váltja ki, hanem a gomba immunreakciót generál a szervezetben (Jakucs, 1999)
Az immunmediált haemolitikus anaemia tünetei
A betegség tünetei gyakran csak késői stádiumokban jelentkeznek, ugyanis a hemolízist az egészséges vérképzés kompenzálhatja. Az immunhaemolitikus anaemia főként nem specifikus tüneteket produkál, ezért pontos diagnózist csak a vérkép ismeretében lehet felállítani. Az IHA egész szervezetre kiható tünetegyüttesei mind a szöveti hypoxia által okozott klinikai tünetek. A fokozott hemolízisre {1. ábra}, valamint az immunmediált gyulladásos folyamatokra is figyelemmel kell lenni.
Lassú lefolyású immunhemolitikus anémia esetén a jelek minimálisak lehetnek. A szív- és érrendszerri tünetek mint tachycardia -azaz a normálisnál szaporább szívverés-, megnövekedett perctérfogat-, melyet tachypnoea –vagyis szapora légvétel- kísér, mind a vérszegénység kompenzálására szolgálnak. Mindez a vérszegénység előrehaladásával dekompenzációhoz vezet. Gyakori kardiovascularis tünet még a 3. telődési diasztolés szívhang (S3) zavara, valamint a szisztolés szívzörej. (Detweiler és Patterson, 1967).
Általános kórtörténet az eszméletvesztés, gyengeség, ataxia, letargia, anorexia, tachypnoe, dyspnoe, hányás valamint hasmenés, esetleg polyuria és polydipsia (fokozott szomjúságérzet). Sok IHA-s kutyánál nyugalmi helyzetben a tünetek nem vagy csak minimálisan jelentkeznek, azonban testmozgás vagy stressz hatására a szimptómák rosszabbodnak (Balch és Mackin, 2007).
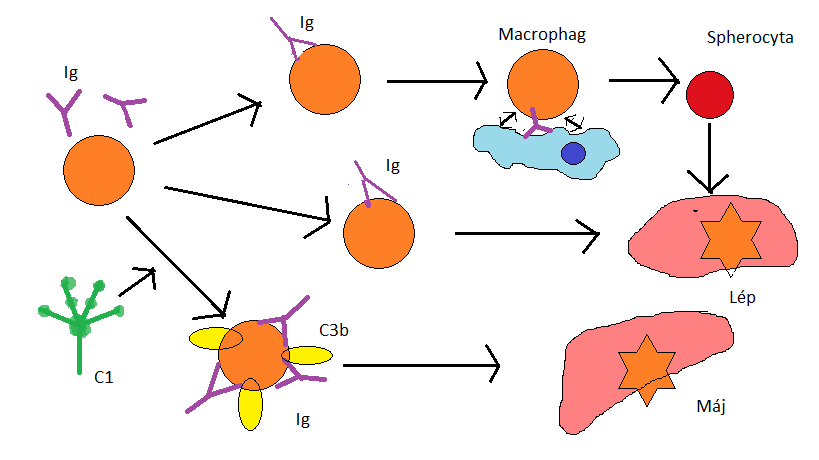
Fizikai vizsgálat esetén a legszembetűnőbb tünet a sápadt nyálkahártnya és a tachypnoe, a betegséget pedig láz kísérheti. Ezen felül a lép, valamint máj mint lebontó szerv megemelkedett produkciója miatt azok megnagyobbodása jön létre, ezt splenomegalianak és hepatomegalianak nevezzük {4. ábra}. Az icterus vagy más néven sárgaság esetén a szérum bilirubin tartalma meghaladja 2-3 mg/dl-t, ez okozza a nyálkahártya sárgás színét, mely az egyik legjellegzetesebb tünete az immunhaemolitikus anámiának. Később, a betegség előrehaladásával a bilirubin koncentrációja tovább emelkedik és a bőrön is jelentkezik a sárgaság (Balch és Mackin, 2007) (Mizumotoés és mtsai 1979).
Az immunhaemolitikus anémiás kutyák közel 50-70%-a szenved egyidejűleg thrombocytopeniában is, mely Evans-szindrómaként ismert (Carr és mtsai, 2002). Számoltak már be olyan ritka esetekről, ahol az antitestek az alacsony testhőmérséklet miatt aktiválódtak és hemolizálták a vörösvérsejeket a test hűvösebb részein, így a végtagok ischaemiás bőrelváltozását eredményezve (Balch és Mackin, 2007).
|
A betegség diagnosztizálása
A tünetek alapján több kór gyanúja merülhet fel, így további vizsgálatok szükségesek, mert a kezelés szempontjából nem mindegy mi okozza az anémiát. Másodlagosan kialakult hemolítikus anémia immunszuppresszív kezelése a problémát megoldani nem tudja, sőt, a kiváltó ok meg nem szűnése miatt az állat kondíciója rosszabbodhat, esetlegesen elhulláshoz vezethet, ezért klinikai szempontból fontos elkülöníteni, hogy primer vagy szekunder hemolítikus anémia okozza-e a tüneteket. Alapadatok mellett(fajta,nem,kor, testtömeg, testhőmérséklet, szívfrekvencia,légzésszám) fontos tudni, mióta állnak fenn a tapasztalt tünetek, illetve ismerni kell az állat oltási előzményeit, ugyanis bizonyos vakcinák okozhatnak hemolízist, vörösvérsejtszétesést. Mivel bizonyos élelmiszerek(hagyma), illetve idegen testek(melyek tartalmazhatnak cink oxidot) szintén hemolízist válthatnak ki, így a vizsgálatokat erre a területre is ki kell terjeszteni. Az elsődleges immunhemolítikus anémia diagnosztizálásához adekvát kritériumok:
- 25-30% alatti haematokrit érték
- Haemolysis kimutatható haemoglobinurivál, haemoglobinaemiával
- Kimutatható vörösvérsejt antitestek, autoagglutináció, keneten: sphaerocytosis(legömbölyödött vörösvértestek),anisocytosis(különböző méretű vörösvértestek)polychromasia(különböző mértékben festődő vörösvértestek), pozitív teszt direkt antiglobulinra (Coombs teszt)
- Egyéb haemolízist okozó faktorok kizárása
- Megfelelő válasz immunszuppresszív terápiára (Bach és Mackin, 2007)
haematológiai vizsgálatok:
Kórjelző értékkel bírnak az alábbi adatok refenciaértékektől való eltérései: A haematocrit érték(<25-30%) csökkenése a vörösvértestek lízisének közvetlen következménye, mely jelenség kísérője a vér emelkedett szabad haemoglobin szintje, ugyanis a vörösvértestekben tárolt Hb a haemolízis következtében kiszabadul a sejtekből és funkcióját veszti(haemoglobinaemia). Jelentős haemoglobinaemia következetesen haemoglobinuriát okoz, tehát a le nem bontott haemoglobin vizelet útján távozik a szervezetből. Súlyos, illetve moderált haemolítikus anaemia esetén praehepatikus hyperbilirubinaemiát figyelhetünk meg, mely miatt a nyálkahártyák elsárgulnak, icterusos lesz az állat. Klasszikus esetben regeneratív immunhaemolítikus anaemiával állunk szemben, ekkor a korrigált reticulocyta százalék emelkedik, ugyanis a csontvelő igyekszik minél több vörösvértestet előállítani. Ha a retikulocyták száma eléri a 60000 db/ mikroliter (vagy az 1% feletti) értéket, az a vörösvérsejtek regenerációját jelzi.(A reticulocyták a vörösvértestek már magját vesztett, de még érettlen alakjai. (Balch és Mackin, 2007) A vérlemezkeszám csökken a fokozott aggregáció végett, kevesebb lehet, mint 100000 db/mikroliter. Az érintett állatokban gyakran fordul elő leukcytosis(>17000 db/mikroliter), a neutruphil granulocyták számának balra tolódásval. Ennek oka lehet a fokozott vörös csontvelő működés, citokin-stimulált myeloid hyperplasia, illetve hogy migrációjuk csökken a necrotikus(üszkös, szegényes vérellátású) szövetekbe, tehát a leukocytosis hipoxia által okozott necrosisra hívja fel a figyelmet.
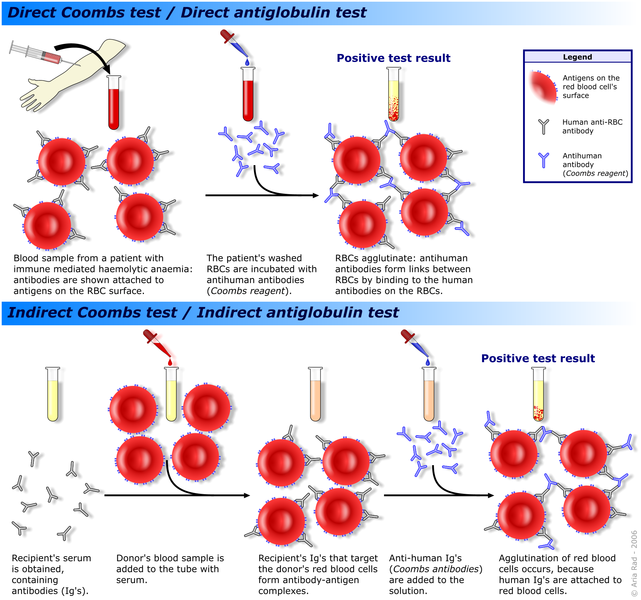
Coomb's teszt {5. ábra} (antiglobulin-teszt, AGT): az elnevezés kétféle tesztre utal (direkt (DAT) és indirekt (IAT)), amik immunhematológiában és immunológiában egyaránt használtak. A DAT vörösvérsejtek membránjához kapcsolt antiglobulinok és felszíni jelzőproteinek detektálására szolgál. A vérmintát elsőként átmossák (a plazmára és az abban lévő kötetlen proteinekre nincs szükség), majd anti-humán globulinnal (Coomb's reagens; humán vizsgálat esetén) inkubálják. Ha a vörösvérsejtek agglutinációja történik, akkor a teszt pozitív, az antitestek a vörösvérsejtek felületére, az imunglobulinokhoz tapadtak. Az IAT leginkább prenatális tesztelésre használatos, főképp terhes nők vértranszfúzióját megelőzően. Ez vörösvérsejtek elleni szabad szérum-antigéneket detektál. Immunmediált hemolitikus anémia kimutatására az előbbit használjuk. Macskák esetében kevés adat van a Coombs teszt hatékonyságáról. Macskák esetében IgG és IgM antitesteket, valamint C3b komplementet vizsgálnak, két hőmérsékleti körülmény között: 37 és 4 Celsius fokon.(esetenként kutyákban is vizsgálják mindhármat, egy hőmérsékleten) (Kohn és mtsai, 2004) (Piek és mtsai, 2008)
|
Kórokozók, valamint haematológiai eltérések vizsgálatára vérkenetet kell mikroszkóppal vizsgálni. Haemolítikus anaemia esetén gyakran fordul elő sphaerocytosis, mely diagnosztikai értékkel bír, mindemellett kutyák esetében kimutathat Ehrlichiozis, babeziozis, haemobartellinozis(Balch és Mackin, 2007) dirofilariasis, leptospirosis(Weinkle és mtsai, 2002) fertőzéseket is.
Macskák esetében szükséges FeLV(feline leukemia virus,macskaleukózis),FIV (feline immundefficiency virus,macskák immunhiányos betegsége) és FIP(feline infectious peritonitis, macska peritonitis)teszteket végezni, ugyanis ezek a betegségek okozhatnak immunhaemolítikus anaemiát. Szintén secundaer immunhaemolítikus anaemiát okozhat a Mycoplasma haemofelis haemoparazitia baktérium, melyet vérkenet segítségével észlelhetünk. (Kohn és mtsai, 2004)
Koagulációs (véralvadási) profil:
A PT (protrombin idő) esetekben emelkedést mutathat(>9mp), tehát a véralvadási idő nőhet(extrinsic út).
Az APTI (aktivált parciális thromboplasztinidő) a véralvadási kaszkád intrinsic útjának paramétere, IMHA-ban szenvedő állatoknál gyakran emelkedett(>19 mp) (Balch és Mackin, 2007)(Burgess és mtsai, 2000)
Vizsgálni kell a plazma fibrinogén szintjét, a fibrinogén bomlástermékeinek arányát és a D-dimerek arányát. (Weinkle és mtsai, 2002) D-dimerek szintjének emelkedése fokozott véralvadásra utal, ami növeli a thrombosis kockázatát.
Szérum biokémiai vizsgálata
A vérszérum biokémiai vizsgálata során különböző enzimek aktivitását mérik, melyek diagnosztikai értékkel bírnak. Ilyen enzim az aszpartát-aminotranszferáz (AST), az alanin-aminotranszferáz (ALT), a kreatin-kináz(CK), és az alkalikus-foszfatáz (ALP). Az ALT és az AST enzimek májsejt-, valamint izomsejtszétesés markerei, vesetubulus károsodáskor a vizeletből is kimutathatóak. A CK enzim megjelenése a vérszérumban szintén az izomsejtek károsodására utal. Az ALT megemelkedett szintje epeúti zavarokra utalhat. A fenn említett legtöbb enzim emelkedett szérum koncentrációja a haemolízis okozta hipoxia, thromboembólia és ischaemia következménye. (Bach és Mackel, 2007)(Weinkle és mtsai, 2000)
A szérum analízis vizsgálatai ki kell terjedjenek totál protein (TP), albumin, kálium, totál bilirubin (TB), kreatinin, és bikarbonát-anion szintjeinek meghatározására is.
Szerológiai/PCR vizsgálat
További szerológiai vizsgálatokkal, illetve polimeráz lánc reakcióval (PCR) haemolízist, másodlagos immunhaemolítikus anaemiát kiváltó kórokozókat kell keresni: Ehrlichia,Bartonella, Babesia, Leptospira, Haemocanis, Anaplasma phagocytophilum (Bach és Mackel, 2007)
Diagnosztikai képalkotási módszerek: (Bach és Mackel, 2007)
Bizonyos esetekben a tünetek immuhaemolítikus anaemiára utalnak, viszont más áll a kórkép hátterében. A pontos diagnózis felállításának és ezáltal az adekvát kezelés meghatározásának előfeltétele, hogy teljeskörű vizsgálatot végezzünk az állaton. Mivel egyes betegségek, melyek haemolízist okoznak, különböző diagnosztikai képalkotási módszerekkel észlelhetők, érdemes hasi röntgent (máj, illetve lép morfológiai elváltozásai, idegentesek a gastrointestinális rendszerben, tömeges elváltozások megfigyelése), és mellkasi röntgent (szívbetegségek, thromboembólia) készíteni. Idősebb állatok esetében ultrahang vizsgálattal releváns lehet neopláziás(daganatos) elváltozásokat keresni, melyek szintén felelősek lehetnek a tünetek kialakulásáért. A szív vizsgálata azért fontos, hogy el tudjuk különíteni az IMHA által okozott szívzörejt a primer szívbetegség miatt kialakult szívzörejtől.
Az IMHA kezelése
A kezelés a pontos diagnózis felállítását követően kezdhető meg.
Primaer(elsődleges) immunhaemolítikus anaemia esetén glükokortikoszteroidok bevitelét és vérátömlesztést, immunszupresszív hatással bíró gyógyszereket, valamint támogató terápiát szoktak javasolni. A glükokortikoszteroidok maguk is immunszuppresszív hatással bírnak, miközben növelik a vörösvértestek és a vérlemezkék számát, ilyen pl. A prednizolone és a dexamethasone. Egyéb, immunszuppresszív tulajdonsággal bíró, primaer IMHA kezelésére alkalmazható hatóanyagok: azatiophrine, ciklofoszfamid, ciklosporin, vinkrisztin, danazol, leflunomid. Általában hatóanyag kombinációkat alkalmaznak. Egy 2008-as tanulmány szerint hatékonyan alkalmazható az azatiophrin + ultra alacsony dózisú aspirin kombinációja a betegség kezelésére. (Piek és mtsai, 2008)
Egyes kutatások humán immunglobulin alkalmazásának hatékonyságát vizsgálják a betegség gyógyításában.(Scott-Moncrieff és mtsai, 1997) Az alábbi tanulmány eredménye alapján a kezdeti terápia részeként alkalmazható a kondíció fenntartására, hosszú távon viszont nem hoz szignifikáns javulást.
Secundaer immunhaemolítikus anaemia esetén a kór közvetlen kiváltóját kell a kezeléssel megcélozni és eliminálni. Ebben az esetben immunszuppresszív terápia alkalmazása nem járna sikerrel és az állat kondíciója romlana, a tünetek továbbra is fennállnának.
Prognózis
Számos faktor utalhat a betegség prognózisára. Egyes kutatások szerint a vér emlekedett urea koncentrációja, icterus (hyperbilrubinaemia), thrombocytopenia, petechiae,láz ha már a diagnózis felállításakor kimutathatóak, emelkedett valószínűséggel fog elhullás bekövetkezni a terápia első három hetében. Az anaemia súlyossága a diagnozís felállításának idejében szintén prognosztikus faktor. (Piek és mtsai, 2008) Leukocitózis és emelkedett retikulocyta arány kedvezőbb prognózist jelzett(regeneráció).(Burgess és mtsai, 2000)(Piek és mtsai, 2008) Emelkedett (+1mp)PT Burgess és mtsai (2000)vizsgálatai alapján 30%-kal növelte az elhullás valószínűségét.
Súlyos thrombocytopaenia, emelkedett szérum bilirubin szint, emelkedett alkalikus- foszfatáz szint és hypoalbuminaemia növeli a thrombosis, és ezzel az elhullás kockázatát. (Carr és mtsai, 2002)
Források és ábrajegyzék
Balch, A., Mackin, A. (2007): Canine Immune-Mediated Hemolytic Anemia: Pathophysiology, Clinical Signs, and Diagnosis. Compendium 29: (4) 217-225
Detweiler, D. K., Patterson, D. F. (1967): Abnormal Heart Sounds and Murmurs of the Dog. Journal of Small Animal Practice 8: (4) 193-205
Mizumoto, R., Kawarada, Y., Yamawaki, T., Noguchi, T., Nishida, S. (1979): Resectability and functional reserve of the liver with obstructive jaundice in dogs. The American Journal of Surgery 137: (6), 768-772
Carr, A.P., Panciera, D.L., Kidd, L. (2002): Prognostic factors for mortality and thromboembolism in canine immune-mediated hemolytic anemia: A retrospective study of 72 cases. J Vet Intern Med 16: (5) 504–509
Weinkle, T. K., Center, S. A., Randolph, J. F., Warner, K. L., Barr, S. C., Erb, H. N. (2005): Evaluation of prognostic factors, survival rates, and treatment protocols for immune-mediated hemolytic anemia in dogs: 151 cases. Journal of the American Veterinary Medical Association 226: (11) 1869-1880
Burgess, K., Moore, A., Rand, W., Cotte, S. M. (2000): Treatment of Immune-Mediated Hemolytic Anemia in Dogs with Cyclophosphamide. J Vet Intern Med 14: (4) 456–462
C.J. Piek, G. Junius, A. Dekker, E. Schrauwen, R.J. Slappendel, E. Teske (2008): Idiopathic Immune-Mediated Hemolytic Anemia: Treatment Outcome and Prognostic Factors in 149 Dogs. J Vet Intern 22: (2) 366–373
Scott-Moncrieff, J.C., Reagan, W.J., Snyder, P.W., Glickman, L.T. (1997): Intravenous administration of human immune globulin in dogs with immune-mediated hemolytic anemia Journal of the American Veterinary Medical Association 210: (11) 1623-1627
Lobetti, R., Dvir, E., J.Pearson (2002): Cardiac Troponins in Canine Babesiosis. Journal of Veterinary Internal Medicine 16: (1) 63-68 Travi, B.L., Ferro, C., Cadena, H., Montoya-lerma, J., Adler, G. H. (2002): Canine visceral leishmaniasis: dog infectivity to sand flies from non-endemic areas. Research in Veterinary Science 72: (1) 83-86
Mellanby, R.J., Holloway, A., Chantrey, J. (2004): Immune-mediated hemolytic anemia associated with a sarcoma in a flatcoated retriever. Journal in Small Animal Practice 45: (1) 21–24
Jakucs, E. (1999): Mérges gombák-gombamérgezések. Természet Világa 130: (9) 134-137
Kohn, B.,Weingart, C., Eckmann, V., Ottenjann, M., Leibold, W. (2006): Primary Immune-mediated Hemolytic Anemia in 19 Cats: Diagnosis, Therapy, and Outcome (1998-2004). J Vet Intern Med 20: (1) 159-166
Ábrajegyzék:
{1.ábra} Saját ábra
{2.ábra} www.mt.mahidol.ac.th/e-learning/ (2018.04.20.)
{3.ábra} Saját ábra
{4.ábra} Saját ábra
{5.ábra} A. Rad~commonswiki (2018.04.20.)