Physiologischer Hintergrund der Migräne
Contents
Definition
Als Migräne bezeichnet man eine Kopfschmerzerkrankung, welche sich vorwiegend in einem plötzlich auftretenden, sich wiederholenden, stark pulsierenden Kopfschmerz äußert. Meist tritt dieser nur in einer Kopfhälfte auf, am häufigsten frontal oder frontotemporal. Der Schmerz kann allerdings auch während eines Anfalls Seite wechseln. Als Begleiterscheinung des Kopfschmerzes tritt häufig Übelkeit, Erbrechen, Licht-, und Geräuschempfindlichkeit auf. Je nach Art des Schmerzes und Begleiterscheinung werden verschiedene Subtypen der Migräne unterschieden, wie beispielsweise die opthalmoplegische Migräne oder die vestibuläre Migräne. Bei bis zu 30% der Fälle kommt es außerdem zum Auftreten von sogenannten Auraphänomenen. Diese sind fokale neurologische Ausfälle, die sich je nach betroffener Hirnregion unterschiedlich äußern können. Sehstörungen wie Gesichtsfeldeinschränkungen oder Doppelbilder sind häufige Auraphänomene, aber auch Paresen, Ataxie oder Schwindel sind nicht selten. Sowohl Attacken mit als auch ohne Aura können sog. Prodromi vorausgehen. Diese äußern sich in unspezifischen Frühsymptomen, wie zum Beispiel Schwindel, Stimmungsschwankungen oder Blässe. Eine Migräneattacke dauert üblicherweise zwischen 7-72h an, mit langsam zunehmendem Schmerzlevel. Hält eine Attacke länger, spricht man von einem Status migraenosus.
Entstehung des Kopfschmerzes
Die Pathophysiologie des Kopfschmerzes ist noch nicht abschließend geklärt. Es gibt einige theoretische Ansätze, welche kontrovers diskutiert werden und mit welchen derzeit Forschung betrieben wird. Momentan geht man davon aus, dass eine Kombination aus Umwelteinflüssen und pathophysiologischen Mechanismen im individuellen Organismus zu einer Migräneattacke führen kann. Auch eine genetische Prädisposition ist nicht auszuschließen. So sind zum Beispiel Frauen 3-mal häufiger betroffen als Männer. Mögliche Triggerfaktoren aus der Umwelt können beispielsweise Wetterumschwünge, Stress, Genussmittel, tyraminhaltige Lebensmittel, die Menstruation oder die Einnahme von hormonellen Kontrazeptiva sein. Über die patophysiologischen Mechanismen gibt es verschieden Theorien.
Ein Erklärungsansatz beschreibt eine Veränderung der Serotoninkonzentration und die Aktivierung des trigeminovaskulären Systems. Während einer Migräneattacke kommt es zu einer erhöhten Freisetzung von Serotonin (5-HT) aus den Axonendigungen der Dura mater, zwischen den Anfällen ist die Serotoninkonzentration erniedrigt. Als Neutotransmitter führt das freigesetzte Serotonin indirekt zu einer Gefäßdilatation in der harten Hirnhaut, was die pulsierenden und drückenden Kopfschmerzen auslöst. Auch die Aktivierung des trigeminovaskulären Systems - welches die Tatsache beschreibt, dass alle Blutgefäße der Hirnhäute und des Gehirns von dem N.trigeminus (N.V) innerviert werden - führt zu einer Erweiterung der Gefäße. Im Verlauf dieser beiden Vorgänge soll es dann zu einer neurogenen Entzündung der Hirnhäute kommen, was wiederum länger anhaltenden Kopfschmerzen oder Nackensteifheit auslöst.
Ein weiterer theoretischer Ansatz beschreibt die sog. Streudepolarisation (SD) oder auch Cortical-spreading-Depression (CSD). Diese „gilt als pathophysiologisches Korrelat von Migräne mit Aura und Kopfschmerzattacken.“ (Chen et al, 2022) CSD ist der Auslöser für verschieden neuronale Mechanismen, die vor allem indirekt Auswirkungen auf die zerebrale Durchblutung haben. So wird beispielsweise die neuronale Aktivität des Kortex kurzzeitig unterdrückt, „die betroffenen Neuronen sind dabei etwa eine Minute lang unerregbar.“ (Freitag et al, 2005) Des weiteren kann es zu einer Störung der Ionenhomöostase kommen, was zu der Auslösung von CSD führen kann. Durch CSD kann außerdem die Aktivierung von duralen Nozizeptoren, welche für Schmerzempfindung zuständig sind, und Teilen des N.trigeminus beobachtet werden. Auch auf den Thalamus und die Amygdala hat CSD Einwirkungen. Der genauerer Zusammenhang zwischen den oben genannten Mechanismen und Migräneattacken mit Aura befindet sich allerdings noch in Forschung.
Ein dritter Ansatz erforscht derzeit Migräne im Zusammenhang mit Calziumabhängigen Kalium-Kanälen. Hierbei wird von einer Genmutation ausgegangen, welche das Gen KCNN3 betrifft. Dieses Gen ist auf einem Chromosom lokalisiert, welches bewiesen mit der autosomal dominant vererbten familiären hemiplegischen Migräne (FHM) im Zusammenhang steht. Das Gen KCNN3 codiert eine bestimmte Art Kalium-Kanal, welcher „in bestimmten Bereichen des Gehirns bevorzugt exprimiert wird und dort die Erregungsfrequenz und das Entladungsmuster der Neurone moduliert.“ (Freitag et al, 2005)
Auch der Rolle von Ionenkanäle im ZNS wird immer mehr Bedeutung zugeschrieben. Defekte an diesen Kanalproteinen können Instabilitäten im ZNS hervorrufen. So kann es beispielsweise zu pathophysiologischen Veränderungen an den P/Q-Typ Kalziumkanälen kommen. Diese können wiederrum mit CSD und der Freisetzung von Neurotransmittern, wie Serotonin, in Verbindung gebracht werden. Die neuronale Überregebarkeit, die oft bei Migränepatienten festgestellt wird, kann ebenfalls mit einer Veränderung der Ionenkanäle erklärt werde.
Phasen der Migräne
Prodromie
Oft werden unspezifische Vorboten, sog. Prodromie von den Patienten beschrieben. Sie treten wenige Tage bis Stunden vor der Migräneattacke ohne Aura bzw. mit Aura auf. Dazu gehören beispielsweise Stimmungsveränderung, Heißhunger, Appetitlosigkeit, Konzentrationsprobleme und vermehrter Durst.(vgl. Abb.1) Kurz bevor die Kopfschmerzen auftreten, klingen die Symptome meist wieder ab, sie können jedoch auch während einer Migräneattacke bestehen beleiben. Diese sind allerdings zu unterscheiden von bestimmte Auslösefaktoren, sogenannte Trigger-Faktoren. Diese können beispielsweise tyraminhaltige Nahrungsmittel (z.B. Weichkäse, Schokolade, Meeresfischerzeugnisse) Rauschmittel, Wetterumschwünge, Stress, die Menstruation oder die Einnahme von hormonellen Kontrozeptiva sein.

Abb 1: Verlauf einer Migräneattacke
Migräne mit Aura
Generell wird zwischen Migräne mit (MA) und ohne Aura (MO) unterschieden. Diese Phasen folgen jeweils der Prodromie.(vgl. Abb.2) Circa 30 % der Migränepatienten leiden an einer MA. Ein Teil der Patienten berichtet allerdings auch über das Auftreten beider Formen. Die Aura ist ein neurologisches Symptom und kann Veränderungen im Hirnstamm hervorrufen. Sie entwickelt sich innerhalb von 5 bis 20 Minuten und hält max. für 60 Minuten an. Das oft mit Migräne in Zusammenhang gebrachte Symptom Kopfschmerz muss in diesem Fall nicht obligatorisch vorhanden sein. Die Aura ist geprägt von schwerwiegenden Symptomen und die Betroffenen sind meist in ihrem Alltag eingeschränkt. Bei 99% der Migränepatienten tritt eine visuelle Aura mit Gesichtsfeldausfällen (Skotom) auf, wobei die Sehrinde beeinträchtig ist. Visuelle Blitze und Augenflimmern sind dabei die Folge und werden als Flimmerskotom bezeichnet. Circa 31 % der Betroffenen leiden unter Sensibilitätsstörungen, sowie ungefähr 18% unter Sprachstörungen. Weitere auftretende Symptome können beispielsweise eine Verstärkung der Farbwahrnehmung, Taubheitsgefühl, Schwindelgefühlen und Paresen sein.
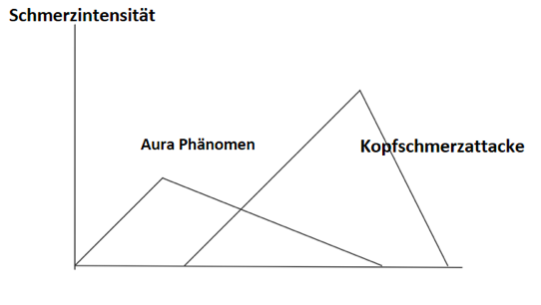
Abb. 2: Zeitliche Einteilung bei Migräne mit Aura
Migräne ohne Aura
Bei einer Migräneattacke ohne Aura ist der Kopfschmerz wohl das bekannteste Symptom. Circa 70% der betroffenen Patienten leiden unter MO. Es handelt sich um idiopathische wiederkehrende Kopfschmerzattacken. Dieser Schmerz dauert ca. 4 bis 72 Stunden an und kann dabei mäßig bis stark ausfallen. Einen länger anhaltenden Schmerz bezeichnet man als Status migraenosus. Der Kopfschmerz ist oft einseitig lokalisiert, pulsierend und wird durch Aktivitäten verstärkt. Typische Begleitphänomene sind depressive Stimmungen, Erbrechen, Schlaflosigkeit, Übelkeit, Licht -, Geräusch- und Geruchsempfindlichkeiten.
Begleitsymptomatik und der Einsatz von Medikamenten
Um einen bestmöglichen Therapieerfolg zu erreichen, ist eine frühe und hochdosierte Medikamenteneinnahme erforderlich. Bei leichtem Kopfschmerz und milden Symptomen wird von einer leichter bis mittelstarken Migräneattacke gesprochen. Die weltweit häufigsten verordneten Medikamente gehören zu der Gruppe der NSAR(nichtsteroidalen Antirheumatika). Ihre Beliebtheit resultiert aus einer schnellen analgetischen und antiphlogistischen Wirkung. Diese positiven Wirkungen kommen vor allem durch eine Hemmung der Prostaglandinsynthese zustande. Die erheblichen Nebenwirkungen werden jedoch oftmals unterschätzt. Hauptsächlich handelt es sich um Nebenwirkungen am Gastrointestinaltrakt oder an der Niere. Der Einsatz sollte deswegen immer sorgfältig bedacht werden. Die darin enthaltende Acetylsalicylsäure kann von dem Patienten oral oder intravenös verabreicht werden. Eine intravenöse Applikation sollte dabei nur bei einem Notfall in Betracht gezogen werden. Aus der Gruppe des NSAR ist Ibuprofen ist ein gängiges Medikament und sollte vom Patienten ausschließlich oral aufgenommen werden. Bei einer richtigen Applikation und Dosierung besteht ein äußerst geringes Risiko für schwerwiegende Nebenwirkungen.
Bei stärkeren Migräneattacken stellen NSAR nicht den erwünschten Effekt dar und es wird empfohlen auf den Wirkstoff Triptan umzusteigen. Triptane sind Serotoninantagonisten (wirken an 5-HT1-Rezeptor) und sind allgemein gut verträglich und sicher. Sie wirken als Entzündungshemmer und verhindern eine aseptische Entzündung der Duraarterien. Die Ausschüttung von Entzündungsmediatoren wird dabei gehemmt und eine Konstriktion der Gefäße herbeigeführt. Triptane sollten nach der Auraphase (Beginn der Kopfschmerzphase) eingenommen werden, da sich die Symptomatik sonst verschlimmern könnte. Triptane können in drei Untergruppen aufgeteilt werden. Die erste Gruppe beinhaltet den Arzneistoff Sumatriptan, welcher subcutan verabreicht wird, und weist eine schnelle und starke Wirkung mit einer kurzen Wirkdauer und einer hohen Nebenwirkungswahrscheinlichkeit auf. Durch dessen Verabreichung wird die migränetypische Gefäßdilatation verringert, wodurch die Kopfschmerzsymptomatik verbessert wird. Die zweite Gruppe setzt aus den Arzneistoffen wie Eletriptan, Rizatriptan, Almotriptan, Sumatriptan und Zolmitriptan zusammen. Sumatriptan sollte hier allerdings oral eingenommen werden. Die dritte Untergruppe ermöglicht eine lange Wirkdauer mit einem langsamen Wirkungseintritt. Zu dieser Gruppe gehören die Arzneistoffe Frovatriptan und Naratriptan. Eine erhöhte Dosierung kann zwar eine erhöhte Wirksamkeit bieten, sollte jedoch, um unerwünschte Nebenwirkungen zu vermeiden, nicht durchgeführt werden. Ein Blutdruckanstieg zählt zu den am häufigsten auftretenden Nebenwirkungen. Bei Anzeichen von Ischämien, Kopfschmerz, Schwindel und Müdigkeit sollte sofort ein Arzt aufgesucht werden. Eine Kombination von Triptan + NSAR kann bei langen oder wiederkehrenden Migräneattacken eingenommen werden. Bei Übelkeit, sollte zusätzlich ein Antiemetikum verabreicht werden. Die Wirkstoffe Metoclopramid (RCP) und Domperidon sind dabei sehr gängig und werden oral eingenommen. Metoclopramid kann allerdings den Hirnstamm angreifen und zu extrapyramidale Störungen führen. Dies ist jedoch nur bei Vorschädigungen des extrapyramidalen Bereiches zu erwarten. Eine Kombination mit Antidepressiva sollte unbedingt vermieden werden. Im Gegensatz zu Metoclopramid hat Domperidon jedoch keine extrapyramidalen Nebenwirkungen. Außerdem kann das Hormon Prolaktin kann unter der Therapie ansteigen, dieses normalisiert sich jedoch wieder nach dem Absetzen von Domperidon.
Bei akuten Migräne-Notfällen können Analgetika wie Metamizol-Natrium und Paracetamol verabreicht werden.Denn eine Vielzahl von Schmerzursachen kann auch durch die Schmerzmittelgabe abgedeckt werde. Eine zusätzliche Infusionstherapie ist dabei sehr zu empfehlen.
Auswirkungen auf das Zentrales Nervensystem
Zellen speichern in einem Gradienten von geladenen Teilchen Energie. Bei einer Migräneattacke geben die Zellen des zentralen Nervensystems zu viel Energie ab, teilweise mehr, als bei einem epileptischen Anfall. Neurone, die diesen Prozess durchlaufen, stecken per Diffusion ihre Nachbarneuronen an. Das zentrale Nervensystem wird so langanhaltenden und hochfrequenten Spannungen ausgesetzt. Wird es zu stark, zu intensiv und zu schnell aktiviert bzw. beeinflusst, kann zunächst eine Überaktivierung und daraufhin eine Erschöpfung des Systems resultieren. Daraus entstehen neuronale Schäden, diese setzen wiederum sekundäre Entzündungsstoffe frei. Es resultiert eine strukturelle Veränderung des Nervensystems und eine Begünstigung von auftretenden Begleiterkrankungen. Durch einen erhöhten Glutamatspiegel kommt es zusätzlich zu einer ständigen Überaktivierung des Nervensystems. Hierbei wird vermutet, dass dies auch bei dem Auftreten anderer Erkrankungen eine wichtige Rolle spielt. Im neurologischen Bereich können Epilepsie, einen Medikamentenübergebrauchskopfschmerz oder ein Schlaganfall die Folge einer Migräne sein. Auf der psychischen Ebene können Depressionen, Angst- und Panikerkrankungen das Leben der Patienten stark beeinflussen.
Sonderformen
Neben dem typischen Verlauf der Migräne kann es auch zu Sonderformen der Kopfschmerzerkrankungen kommen. Die atypischen Symptome machen es allerdings schwieriger eine endgültige Diagnose zu stellen. Im Folgenden werden drei dieser abweichenden Formen genauer betrachtet.
Vestibuläre Migräne
Das klinische Bild der vestibulären Migräne äußert sich vor allem in Schwindelformen, die durch eine Störung des Vestibularorgans hervorgerufen werden. Betroffene Patienten berichten von Dreh-, Schwank- und Lageschwindel, begleitet von Schwierigkeiten beim Gehen und Aufrechtstehen. Bei ca. 75% der Fälle wird der Schwindel von einem starken Kopfschmerz begleitet. Zusätzlich kann häufig ein Nystagmus und eine Störung des Vestibulookulären Reflexes beobachtet werden. Eine solche Migräneattacke kann sowohl einige Sekunden bis Minuten andauern, als auch mehrere Stunden bis Tage. Weibliche Patienten sind bis zu 4-mal häufiger von dieser Sonderform der Migräne betroffen als männliche. Vor allem Patienten, die die Menopause erreicht haben, leiden speziell unter verstibulärer Migräne. Allerdings treten die Symptome oftmals erst einige Jahre nach Beginn der Menopause auf, was eine Diagnose erschwert. Bei der Pathophysiologie der vestibulären Migräne geht man sowohl von zentralen, als auch von peripheren verstibulären Störungen aus. So konnte man während einer Migräneattacke beispielsweise eine erhöhte Freisetzung an Neurotransmittern in den Affereinzien der verstibulären Kernen festestellen. Vor allem Serotonin und Noradrenalin spielen hierbei eine wichtige Rolle. Ob vestibuläre Migräne ein vererbbar Gendefekt ist, wird derzeit noch diskutiert.
Ophathalmoplegische Migräne
Bei dieser seltenen Sonderform liegt eine Parese des N.oculomotorius (N.III), des N.trochlearis (N.IV) oder des N.abducens (N.VI) vor. Ein einseitiger sich wiederholender Kopfschmerz und eine Parese sind Anzeichen dieses speziellen Migränetyps. Oftmals schwächen sich die Symptome bis zum sechsten Tag nach Beginn des Migräneanfalls ab. In der Regel ist ab dem 10. Tag eine vollständige Restitutio ad intergrum zu beobachten.
Retinale Migräne
Diese seltene Sonderform setzt den Kopfschmerz mit visuellen Vorgängen in Verbindung. Als Visuelle Phänomene können Blindheit, Flimmern oder Skotome während eines Anfalls auftreten. Ein solcher Migräneanfall entwickelt sich innerhalb von 5 Minuten und dauert ca. 5 bis 60 Minuten an. Kopfschmerzen können die Attacke begleiten, dies muss jedoch nicht zwingend der Fall sein. Auftretende Symptome eines solchen Anfalls sind beispielsweise Übelkeit, Photophobie, Schwindel etc.. Manche Patienten berichten über Halluzinationen und dem Sehen von Doppelbildern.
Migräne bei Ratten
Durch eine meningeale Reizung und eine Aktivierung der trigeminalen Nerven kann ein migräneähnliches Verhalten bei Ratten herbeigeführt werden. Die Aktivierung des trigeminovaskulären Systems wird als Grundlage des Migränekopfschmerzes betrachtet. Im Experiment resultierte eine Ausschüttung von CGRP (Calcitonin Gene-Related Peptide) in einer Vasodilatation der meningealen Gefäße bzw. in einem Proteinaustritt im Gewebe. Bei den Tieren konnte daraufhin eine Verhaltensänderung beobachtet werden. Die auftretenden Krankheitssymptome haben große Ähnlichkeit mit Menschen und bestätigten, dass Ratten meningeale Reize empfinden können. Das Martino und Perkins‘ Voice-records-Modell war lage Zeit die einzige Untersuchung, die basierend auf thermische und mechanische Hypersensibilität durchgeführt worden ist. Parameter wie beispielsweise das Putzen, das lokomotorische Verhalten, (z.B. Laufgeschwindigkeit, Messung der zurückgelegenen Strecke) Nahrungs -und Wasseraufnahme wurden dabei beurteilt. Aufgrund einer Verhaltensänderungen der kranken Tiere kann ein besseres Verständnis der Migräne erfolgen und so eine große Hilfe in der darauffolgenden Forschung der Erkrankung sein. Durch eine meningeale Reizung und eine Aktivierung der trigeminalen Nerven kann ein migräneähnliches Verhalten bei Ratten herbeigeführt werden.
Quellen
Literaturverzeichnis
BAUER, H.; MÄRKER-HERMANN, E. (2003): Therapie mit nichtsteroidalen Antirheumatika (NSAR). Der Orthopäde 32: (12) 1088-1094. doi: 10.1007/s00132-003-0559-2
CHEN, M.; FU, X.; LI, P; LU, J. (2022): Cortical spreading depression induces propagating activation of the thalamus ventral posteromedial nucleus in awake mice. The journal of Headache and Pain 23: (1) 15. doi: 10.1186/s10194-021-01370-z
EBERSBERGER, A. (2002): Pathophysiologie der Migräne. Der Anaesthesist 51: (8) 661-667. doi: 10.1007/s00101-002-0342-5
FELBER, W.; FICKER, F. (1977): Metoclopramid – (Cerucal R) – Nebenwirkung als extrapyramidale Störung bei Kombination mit einem Antidepressivum. Psychiatrie, Neurologie und medizinische Psychologie 29: (5) 304-306. PMID: 882611
FISCHER, J.M.; LENNERT, J.K.; MESSLINGER, K. (2011): Neuropeptidwirkungen im trigeminalen System: Pathophysiologie und klinische Bedeutung bei der Migräne. Schmerz 25: (4) 393-398, 400-401. doi: 10.1007/s00482-011-1069-5
FREITAG, C.M.; LESCH, K.P.; MARZINIAK, M.; MEYER, J.; MÖSSNER, R.; SOMMER, C.; WEICHSELBAUM, A. (2005): A highly polymorphic poly-glutamine stretch in the potassium channel KCNN3 in migraine. Headache 45: (2) 123-136. doi: 10.1111/j.1526-4610.2005.05027.x
LEMPERT, T.; VON BREVERN, M. (2019): Vestibular Migraine. Neurologic Clinics 37: (4) 695-706. doi: 10.1016/j.ncl.2019.06.003
TRIEBE, F. (2012): Verhaltensbiologische Untersuchungen in einem experimentellen Kopfschmerzmodell. Charité - Universitätsmedizin Berlin. doi: 10.17169/refubium-6651
TROOST, B.T (1996): Ophthalmoplegic migraine. Biomedicine & Pharmacotherapy 50: (2) 49-51. doi: 10.1016/0753-3322(96)84712-3
WECKER,S. (2013): Die Bedeutung primärer und sekundärer trigeminaler Neurone für die Ausschüttung von Calcitonin Gene-Related Peptide in einem tierexperimentellen Migräne-Modell. Charité - Universitätsmedizin Berlin. doi: 10.17169/refubium-7647
Abbildungsverzeichnis
Abb 1: Verlauf einer Migräneattacke, erstellt von Lisa Holldorf
Abb 2: Zeitliche Einteilung bei Migräne mit Aura, erstellt von Lisa Holldorf
