Mangán indukálta neuroinflammáció
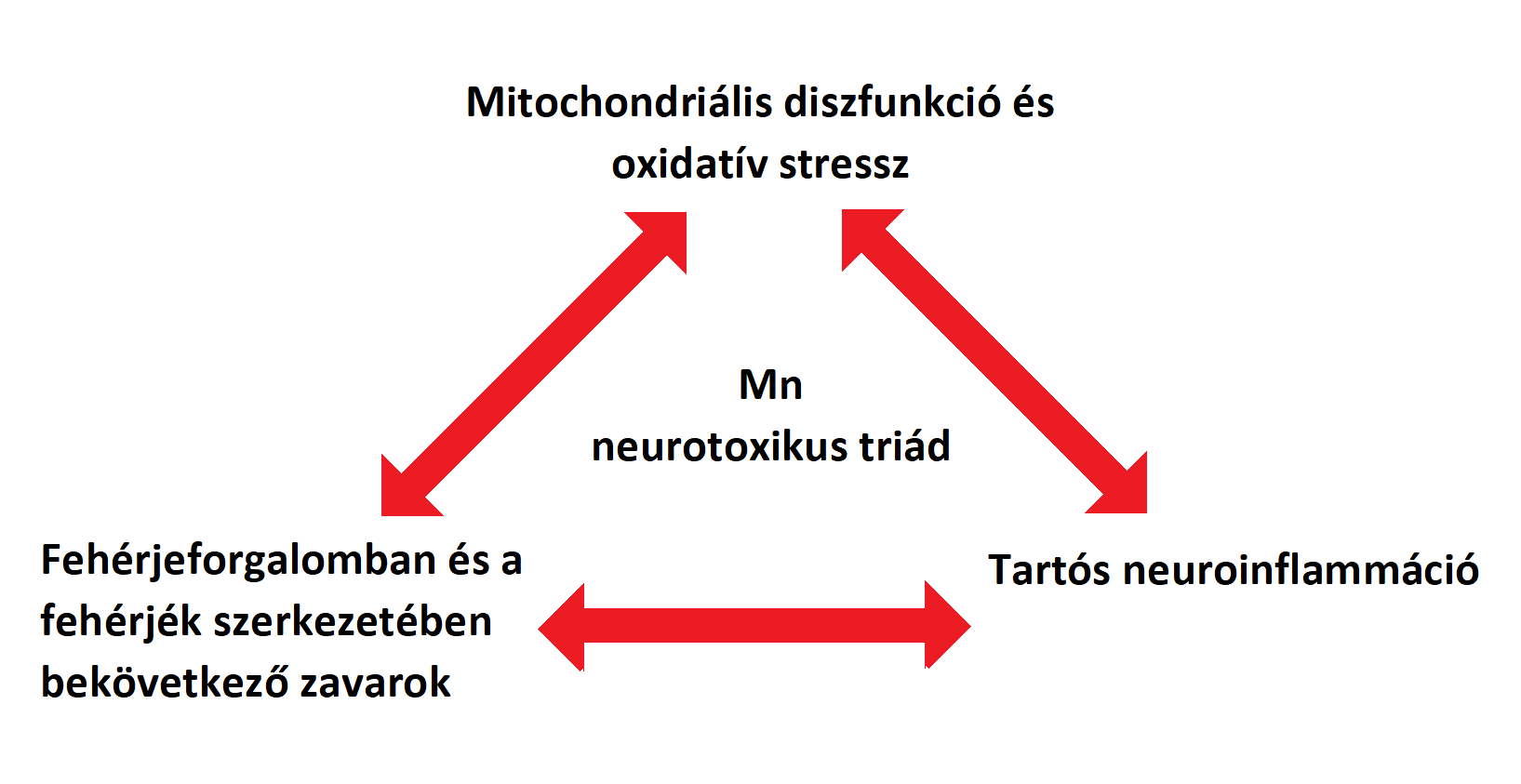
A mangán okozta neurotoxikáció („Manganism”) egy idegrendszert érintő betegség, mely hasonló tünetek kialakulásához vezet, mint a Parkinson-kór (PD). A PD-hoz hasonlóan ez a betegség is a központi idegrendszert érinti, azon belül is főként a nigrostriatális pályát, ami később viselkedési és motorikus károsodásokhoz vezet. A betegséget 1837-ben fedezték fel először, azóta számos kutatás született a témában. A korai kísérletek a magas mangán-koncentráció hatását kutatták a mitochondrium működésére és az ebből kifolyólag létrejövő oxidatív stressz kialakulására. Napjainkban főként a sejtes és molekuláris utakat kutatják, melyek részt vehetnek a mangánmérgezésben. Emellett friss kísérletek szerint a mangán részt vehet olyan fehérjék szerkezetének módosításában is, mint az alfa-synukleninek és amyloidok, ezáltal hitelt adva a feltételezésnek, hogy a környezetből felvett mérgező anyagok elindíthatnak, vagy akár tovább is terjeszthetnek neurodegeneratív folyamatokat azáltal, hogy befolyásolnak egyes betegség-specifikus fehérjéket. A Mn, a „manganizmuson” és a PD-on kívül, így szerepet játszhat még prionbetegségekben és a Huntington-kórban is. Tekintve, hogy a Mn hatással van a fehérjék szerkezetére, a mitochondriumok működésére, ezáltal a neuroinflammáció és neurodegeneráció kialakulására, egyes kutatók bevezették a „Mn Mechanistic Neurotoxic Triad” fogalmát (1. mitochondriális funkciózavar és oxidatív stressz, 2. protein „trafficking” és „misfolding”, valamint 3. neuroinflammáció). Ez a megközelítés segít megérteni és feltárni a túlzott Mn-expozíció által kiváltott folyamatokat és ezek összefüggéseit (D. S. Harischandra, S. Ghaisas, et al. 2019), (1.kép)
tartalom
Múltbéli kutatások, rövid kutatástörténet
A mangán okozta idegrendszeri betegségek kutatása szorosan összefügg az ipar fejlődésével. Elsőként 1837-ben John Couper írta le a jelenséget Skóciában. A glasgow-i Charles Tennant fehérítő gyárban (a kor legnagyobb fehérítő gyára volt a korban) dolgozó munkások még újnak számító technológiával klórt állítottak elő. A folyamat nagy mennyiségű mangánt kívánt, így a dolgozók minden nap magas mangán-koncentrációnak voltak kitéve, amely végül mérgezéshez vezetett. A század előrehaladtával, az új fémelőállítási technikák használata szintén jelentősen megnövelte a mangán felhasználását. Az új tudományos megfigyelésig azonban egészen 1901-ig kellett várni. Embden és von Jaksch egymástól függetlenül számoltak be esetekről, melyeket a sok mangánport tartalmazó levegő okozott. Az első világháború előtti évekből már 9 beteget jelentettek mangán okozta idegrendszeri megbetegedéssel Európa különböző pontjairól. A világháborúban fegyverkezési célokra használták fel, amitől tovább növekedett a mangánnal történő érintkezések száma. A XX. század közepétől kezdve az új diagnosztikai technológiák segítségével egyre több beteget regisztráltak. (Blanc 2018) Az ember napjainkban is számos területen ki lehet téve már károsnak számító Mn-koncentrációnak a mezőgazdaságtól (Mn-tartalmú peszticidek) a bányászaton (2. kép) és kohászaton át a szennyezett ivóvízig. A Mn és a szervezetre gyakorolt hatása ma is egy erősen kutatott terület, amelyben még sok az ismeretlen mechanizmus.
A Mn-indukálta neuroinflammáció részfolyamatai Mangán-aktiválta NLRP3 inflammasoma jelpálya, exosomák, ASC a microglia sejtekben A krónikus Mn-terhelés károsítja a nigrostriatális régiót (37, 42, 62-66 K. S. Kirkley, K. A. Popichak, et al., 2017; T. V. Peres, M. R. C. Schettinger, et al., 2016; T. R. Guilarte, 2010, 2013; T. R. Guilarte, K. K. Gonzales, 2015; M. Aschner, K. M. Erikson, et al., 2009; K. J. Horning, S. W. Caito, et al., 2015), főemlősökben microglia-aktivációt vált ki a substantia nigra pars compacta területén (67 T. Verina, S. F. Kiihl, et al., 2011), és astrogliális inflammációt indukál (37 K. S. Kirkley, K. A. Popichak, et al., 2017). Szintén elősegíti a gliasejtek proinflammatorikus cytokin-termelését (68-70 C.-J. Chen, Y.-C. Ou, et al., 2006; P. L. Crittenden, N. M. Filipov, et al., 2008; N. M. Filipov, C. A. Dodd, et al., 2011) valamint serkenti az NFκB és p38 mitogén-aktiválta protein-kináz útvonalat a gliasejtekben (30, 69 N. M. Filipov, R. F. Seegal, et al., 2005; P. L. Crittenden, N. M. Filipov, et al., 2008). A Mn-indukálta neurotoxicitás hátterében húzódó krónikus gyulladás mechanizmusa még nem teljesen ismert. Az inflammasoma-aktiváció különféle neurodegeneratív rendellenességekkel (pl. Parkinson-kór, Alzheimer-kór, traumatikus agyi sérülés) áll kapcsolatban (14 L. C. Freeman, J. P.-Y. Ting, 2015). Az ATP-től (58 E. -K. Jo, J. K. Kim, et al., 2016) különféle ásványokon (59, 60 F. Martinon, V. Pétrilli, et al., 2006; C. Dostert, V. Pétrilli, et al., 2008) és mitochondriális inhibitoron (17, 61 R. Zhou, A. S. Yazdi, et al., 2011; V. Lawana, N. Singh, et al., 2017) keresztül a szerkezetükben módosult proteinekig (15,16 A. Halle, V. Hornung, et al., 2008; G. Codolo, N. Plotegher, et al., 2013) nagyon sok tényező kiválthat NLRP3 inflammasoma-aktivációt. Bár a teljes folyamat még nem ismert, számos stimulusról bebizonyosodott, hogy az NLRP3 inflammasoma-kaszkád aktiválásának 2-es szignáljaként működnek. Megannyi faktor (pl. mitochondriális és lysosoma diszfunkció, mitochondriális superoxid-termelés) képes előidézni az NLRP3 felszaporodását és aktiválását (17, 18, 72, 43 R. Zhou, A. S. Yazdi, et al., 2011; S. Alfonso-Loeches, J. R. Ureña-Peralta, et al., 2014; S. Sarkar, E. Malovic, et al., 2017; E. Aflaki, N. Moaven, et al., 2016). Az astrocyták és neuronok mitochondriumainak funkciózavarát, illetve superoxid-termelését a bennük felgyülemlő Mn képes előidézni (26, 34, 50, 73 D. Milatovic, Z. Yin, et al., 2007; Z. Yin, J. L. Aschner, et al., 2008; J. A. Roth, C. Horbinski, et al., 2002; K. V. R. Rao, M. D. Norenberg, et al., 2004). A PD-ral összefüggésben lévő PARKIN gén egyik terméke, a mitochondriális fúziós protein 2 (Mfn2) fontos szerepet játszik a mitochondriális fúzióban (74, 75 A. Rakovic, A. Grünewald, et al., 2011; N. Rocha, D. A. Bulger, et al., 2017). Bebizonyították, hogy a Mn túlzott jelenléte csökkent Mfn2-expresszióhoz vezet, amivel mitochondriális diszfunkció és inflammasoma-aktiváció jár együtt. A VPS35 retromer komplex protein mutációja vagy csökkent expressziója képes kiváltani a mitochondriumok funkciózavarát akár az Mfn2 csökkentésével a dopaminerg neuronokban (54 F.-L. Tang, W. Liu, et al., 2015), akár a dynamin-like protein 1 komplex újra felhasználásával (78 W. Wang, X. Wang, et al., 2016). Kimutatták, hogy a Mn-terhelés csökkenti a VPS35 mennyiségét az LPS-primed microglia sejtekben, serkentve az Mfn2 degradációját, ami kapcsolatban áll a mitochondriális ubiquitin-ligáz (Mul1) expressziójával. A pontos mechanizmus még nem ismert. Mindemellett, a VPS35 befolyásolja az exosomák celluláris biogenezisét és felszabadulását (81, 82 J. Follett, S. J. Norwood, et al., 2014; L. J. Vella, A. F. Hill, et al., 2016). Ezek az exosomák hozzájárulnak a neurodegeneratív betegségek kifejlődéséhez. Az általuk szállított aggregálódott α-Synuclein kulcs szignálként működik a többi sejt számára, így szintén segítenek a neuroinflammáció modulálásában (86 A. Gupta, L. Pulliam, et al., 2014). Úgy látszik, egy újfajta pyroptotikus-phagocytikus kaszkád terjeszti el az NLRP3 inflammasoma és annak adapter molekulájának (ASC) együttesét a sejtek között, hasonlóan a prionokhoz (19 B. S. Franklin, L. Bossaller, et al., 2014). A Mn serkenti az ASC exosomális felszabadulását az LPS-primed microgliákból, ugyanakkor az exosoma-felvétel blokkolása csökkenti az interleukin-1β (IL-1β) felszabadítását. Ezeknek az eredményeknek számos vonzata lehet, mivel az exosomák akár szervek közötti kommunikáció lebonyolítására is képesek és a vér-agy gáton is át tudnak hatolni. (3. kép)
