|
Size: 30872
Comment:
|
Size: 24805
Comment:
|
| Deletions are marked like this. | Additions are marked like this. |
| Line 2: | Line 2: |
| '''A portoszisztémás sönt idegrendszeri következményei''' | = A portoszisztémás sönt idegrendszeri következményei = |
| Line 5: | Line 5: |
| . '''I. A betegségről általában''' |
== I. A betegségről általában == |
| Line 11: | Line 10: |
| '''Egyszeres sönt''' – általában veleszületett, a vena portae-t a vena cava caudalishoz köti | ~+Egyszeres sönt+~ |
| Line 13: | Line 12: |
| · extrahepatikus - a veleszületett söntök közül a leggyakoribb, elsősorban kistestű fajtákra jellemző (yorkshire terrier, schnauzer, uszkár, máltai, Shih Tzu, tacskó) | Általában veleszületett, a vena portae-t a vena cava caudalishoz köti. |
| Line 15: | Line 14: |
| · intrahepatikus – nagyobb testű kutyákra jellemző (ír farkas, golden és Labrador retriever, szamojéd) | ''extrahepatikus'' - a veleszületett söntök közül a leggyakoribb, elsősorban kistestű fajtákra jellemző (yorkshire terrier, schnauzer, uszkár, máltai, Shih Tzu, tacskó) |
| Line 17: | Line 16: |
| · Máltaiban és ír farkasban örökletes, yorkie-ban feltételezések szerint örökletes | ''intrahepatikus'' – nagyobb testű kutyákra jellemző (ír farkas, golden és Labrador retriever, szamojéd) |
| Line 19: | Line 18: |
| · Macskákban mindkét típus előfordulhat | Máltaiban és ír farkasban örökletes, feltételezések szerint yorkie-ban is, míg macskákban mindkét típus előfordulhat. |
| Line 21: | Line 20: |
| '''Többszörös sönt''' – szerzett, a vena portaeban uralkodó tartósan magas nyomás hatására és cirrhosis esetén alakul ki. A német juhászok és a dobermannok hajlamosak a betegségre, ez a rendellenesség műtéttel nem korrigálható | ~+Többszörös sönt+~ Szerzett, a vena portaeban uralkodó tartósan magas nyomás hatására és cirrhosis esetén alakul ki. A német juhászok és a dobermannok hajlamosak a betegségre, ez a rendellenesség műtéttel nem korrigálható |
| Line 25: | Line 26: |
| '''Veleszületett portoszisztémás sönt (CPSS) által érintett kutya klinikai tünetei''' | ~+Veleszületett portoszisztémás sönt (CPSS) által érintett kutya klinikai tünetei+~ |
| Line 29: | Line 30: |
| '''Többszörös, szerzett portoszisztémás sönt által érintett kutya klinikai tünetei''' | ~+Többszörös, szerzett portoszisztémás sönt által érintett kutya klinikai tünetei+~ |
| Line 31: | Line 32: |
| Ezen rendellenesség esetén idősebb korban lépnek fel a tünetek, néha kölykökben is kialakulhatnak. Sok esetben a máj károsodásának következménye a sönt kialakulása, például egy bizonyos méreg fogyasztása komoly májbetegséghez vezet, a májnak megnő az ellenállása. A kutya szemfehérje, bőre, ínye sárgás színelváltozást mutat, ha az epeutak is érintettek. Nagyon magas portális nyomás vagy hypoproteinaemia esetén a filtráció mértéke nő, pangó hasűri folyadék keletkezk (ascites). A máj kiesett működése miatt véralvadási zavarok, bevérzések jelenhetnek meg. | Ezen rendellenesség esetén idősebb korban lépnek fel a tünetek, néha kölykökben is kialakulhatnak. Sok esetben a máj károsodásának következménye a sönt kialakulása, például egy bizonyos méreg fogyasztása komoly májbetegséghez vezet, a májnak megnő az ellenállása. A kutya szemfehérje, bőre, ínye sárgás színelváltozást mutat, ha az epeutak is érintettek. Nagyon magas portális nyomás vagy hypoproteinaemia esetén a filtráció mértéke nő, pangó hasűri folyadék keletkezk (ascites). A máj kiesett működése miatt véralvadási zavarok, bevérzések jelenhetnek meg ''(Tobias, 2003)''. |
| Line 33: | Line 34: |
| '''II. Hepatikus encefalopátia''' | == II. Hepatikus encefalopátia == A hepatikus encefalopátia (HE) úgy definiálható, mint a máj működésbeli zavarának következtében kialakuló neurológiai tünet együttes, mely tulajdonképpen a központi idegrendszerben a csökkenő neuron aktivitás által létrehozott abnormális mentális státusz. A HE leggyakrabban PSS következménye. A patogenezis nem teljesen tisztázott, inkább csak teóriák vannak a kialakulásával kapcsolatban. A csökkenő neuron aktivitást lényegében az okozza, hogy a toxikus anyagcsere termékek akkumulálódnak az agyban, mivel valamilyen okból kifolyólag nem bomlanak le a májban. |
| Line 35: | Line 37: |
| A hepatikus encefalopátia (HE) úgy definiálható, mint a máj működésbeli zavarának következtében kialakuló neurológiai tünet együttes, mely tulajdonképpen a központi idegrendszerben a csökkenő neuron aktivitás által létrehozott abnormális mentális státusz. A HE leggyakrabban PSS következménye. A patogenezis nem teljesen tisztázott, inkább csak teóriák vannak a kialakulásával kapcsolatban. | === Csoportosítás === . A HE a májjal kapcsolatos megbetegedések és a klinikai tünetek alapján csoportokba sorolható. |
| Line 37: | Line 40: |
| A csökkenő neuron aktivitást lényegében az okozza, hogy a toxikus anyagcsere termékek akkumulálódnak az agyban, mivel valamilyen okból kifolyólag nem bomlanak le a májban. '''II/1. Csoportosítás: ''' A HE a májjal kapcsolatos megbetegedések és a klinikai tünetek alapján csoportokba sorolható. 1. Klinikai tünetek alapján. Ezt a csoportosítást az alábbi táblázat szemlélteti. ||||||||<tablewidth="632px" tablestyle="border: none;" tableclass="MsoTableGrid"rowstyle="mso-yfti-irow:0;mso-yfti-firstrow:yes;height:35.2pt"^ width="632px" style="width: 474.2pt; border-color: windowtext; background-color: rgb(192, 0, 0); padding: 0cm 5.4pt; height: 35.2pt; background-position: initial initial; background-repeat: initial initial;">'''A hepatikus encefalopátia stádiumai''' || ||<rowstyle="mso-yfti-irow:1;height:27.2pt"^ width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(0, 153, 255); padding: 0cm 5.4pt; height: 27.2pt; background-position: initial initial; background-repeat: initial initial;">'''Első stádium''' ||<^ width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(0, 153, 255); padding: 0cm 5.4pt; height: 27.2pt; background-position: initial initial; background-repeat: initial initial;">'''Második stádium''' ||<^ width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(0, 153, 255); padding: 0cm 5.4pt; height: 27.2pt; background-position: initial initial; background-repeat: initial initial;">'''Harmadik stádium''' ||<^ width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(0, 153, 255); padding: 0cm 5.4pt; height: 27.2pt; background-position: initial initial; background-repeat: initial initial;">'''Negyedik stádium''' || ||<rowstyle="mso-yfti-irow:2;height:35.2pt"width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 35.2pt; background-position: initial initial; background-repeat: initial initial;">Enyhe zavarodottság ||<width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 35.2pt; background-position: initial initial; background-repeat: initial initial;">Levertség ||<width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 35.2pt; background-position: initial initial; background-repeat: initial initial;">Koordinációs zavarok ||<width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 35.2pt; background-position: initial initial; background-repeat: initial initial;">Elfekvés || ||<rowstyle="mso-yfti-irow:3;height:45.05pt"width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 45.05pt; background-position: initial initial; background-repeat: initial initial;">Étvágytalanság ||<width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 45.05pt; background-position: initial initial; background-repeat: initial initial;">Ataxia ||<width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 45.05pt; background-position: initial initial; background-repeat: initial initial;">Zavarodottság ||<width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 45.05pt; background-position: initial initial; background-repeat: initial initial;">Általános reakciócsökkenés vagy hiány || ||<rowstyle="mso-yfti-irow:4;height:20.3pt"width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.3pt; background-position: initial initial; background-repeat: initial initial;">Elbutulás ||<width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.3pt; background-position: initial initial; background-repeat: initial initial;">Látványos elbutulás ||<width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.3pt; background-position: initial initial; background-repeat: initial initial;">Zsibbadás ||<width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.3pt; background-position: initial initial; background-repeat: initial initial;">Kóma || ||<rowstyle="mso-yfti-irow:5;height:18.0pt"width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18pt; background-position: initial initial; background-repeat: initial initial;">Ingerlékenység ||<width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18pt; background-position: initial initial; background-repeat: initial initial;">Személyiségváltozás ||<width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18pt; background-position: initial initial; background-repeat: initial initial;">Fokozott nyálzás ||<width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18pt; background-position: initial initial; background-repeat: initial initial;">Halál || ||<rowstyle="mso-yfti-irow:6;height:18.2pt"width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18.2pt; background-position: initial initial; background-repeat: initial initial;"> ||<width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18.2pt; background-position: initial initial; background-repeat: initial initial;">Vakság ||<width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18.2pt; background-position: initial initial; background-repeat: initial initial;">Rohamok ||<width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 18.2pt; background-position: initial initial; background-repeat: initial initial;"> || ||<rowstyle="mso-yfti-irow:7;mso-yfti-lastrow:yes;height:20.6pt"width="127px" style="width: 95.4pt; border-right-color: windowtext; border-bottom-color: windowtext; border-left-color: windowtext; border-top-style: none; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.6pt; background-position: initial initial; background-repeat: initial initial;"> ||<width="156px" style="width: 117pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.6pt; background-position: initial initial; background-repeat: initial initial;">Dezorientáció ||<width="180px" style="width: 135pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.6pt; background-position: initial initial; background-repeat: initial initial;">Agresszió ||<width="169px" style="width: 126.8pt; border-top-style: none; border-left-style: none; border-bottom-color: windowtext; border-right-color: windowtext; background-color: rgb(189, 214, 238); padding: 0cm 5.4pt; height: 20.6pt; background-position: initial initial; background-repeat: initial initial;"> || |
1. Klinikai tünetek alapján. Ezt a csoportosítást az alábbi táblázat szemlélteti. ''(Táblázat 1.)'' ||<tablebgcolor="#eeeeee" tablestyle="float:center;font-size:0.85em;margin:0 0 0 0; "style="padding:0.5em; ;text-align:center">{{attachment:táblázat 1.1_jpg|felugró szöveg}} <<BR>>'''1. Táblázat'''<<BR>>''A hepatikus encefalopátia stádiumai'' || |
| Line 59: | Line 47: |
| * Az A típusú HE májelégtelenséggel van kapcsolatban. | |
| Line 60: | Line 49: |
| * A B típus PSS jelenlétével van összefüggésben, azonban májelégtelenséggel nem társul. | |
| Line 61: | Line 51: |
| · Az A típusú HE májelégtelenséggel van kapcsolatban. | * A különböző máj parenchima elégtelenséggel és portális vérnyomás emelkedéssel kapcsolatos C típus gyakran társul szerzett PSS-el. Ez a leggyakoribb humán esetekben, míg állatoknál a B a leggyakrabban előforduló HE típus. |
| Line 63: | Line 53: |
| · A B típus PSS jelenlétével van összefüggésben, azonban májelégtelenséggel nem társul. · A különböző máj parenchima elégtelenséggel és portális vérnyomás emelkedéssel kapcsolatos C típus gyakran társul szerzett PSS-el. Ez a leggyakoribb humán esetekben, míg állatoknál a B a leggyakrabban előforduló HE típus. '''II/2. Patogenezis''' |
=== Patogenezis === |
| Line 71: | Line 56: |
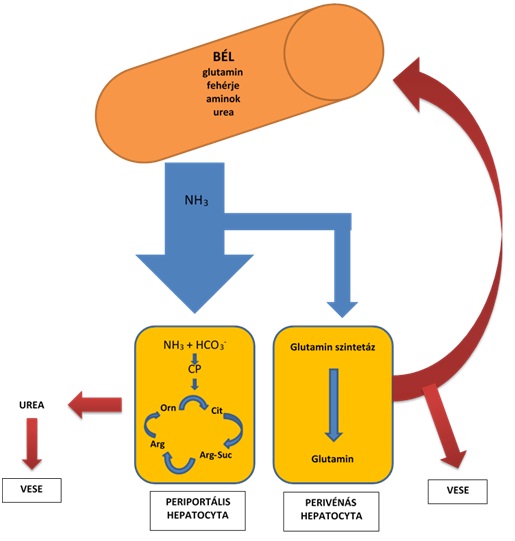
| '''II/3. Teóriák''' | === Teóriák === ==== Megváltozott ammónia metabolizmus ==== ||<tablebgcolor="#eeeeee" tablestyle="float:center;font-size:0.85em;margin:0 0 0 0; "style="padding:0.5em; ;text-align:center"> {{attachment:ammónia.jpg|felugró szöveg}} <<BR>>'''1. Ábra: Ammónia metabolizmus'''<<BR>>''Ammónia a fehérjék és urea lebontása során keletkezik a bélben, illetve az enterocyták glutamin anyagcseréje folyamán. A periportális hepatocytába a portális vénán keresztül jut az ammónia, ahol nagy része bikarbonát ionnal karbamoil foszfáttá alakul (CP). A CP az urea ciklusban citrullin – arginoszukcinát – arginin - ornitin átalakulásokon megy keresztül. Az így keletkező urea a szisztémás keringésbe kerül, majd a vesék választják ki. Az ammónia azon része, melyből nem keletkezik urea, a perivénás hepatocytákba kerül, ahol glutaminná alakul. Ezt végül a vese választja ki, vagy visszakerül az enterocytákba. Ennek köszönhetően az ammónia nem kerül a szisztémás keringésbe.'' || |
| Line 73: | Line 60: |
| ''A. ''''Megváltozott ammónia metabolizmus'' {{file:///C:/Users/Borka/AppData/Local/Temp/OICE_C96069C6-188F-452D-BC0F-67BB8B718B51.0/msohtmlclip1/01/clip_image002.png||width="503",height="530",v:shapes="Kép_x0020_20"}} |
|
| Line 81: | Line 65: |
| ''Ammónia metabolizmus'' | Az ammónia négy mechanizmus során keletkezik a szervezetben: (1) ureázt termelő mikroorganizmusok által a vastagbélben, amelyek a bélben lévő fehérjéket és az ureát bontják, (2) a táplálékból felvett aminosavak májban végbemenő metabolizmusa, (3) a glutamin enterocytákban zajló metabolizmusa, és (4) perifériás szövet (izom) katabolizmusa. A vérben található ammónia több, mint 50 %-a a bélben történő fehérje- és ureabontásból származik. Normál ammónia metabolizmus során ''(1. Ábra)'' az ammónia eléri a májat a portális keringésen keresztül. Az ammónia nagy része az urea ciklusba kerül majd a vesék által exkretálódik. A maradék felhasználódik a glutamát-glutamin átalakulás során a glutamin szintetáz segítségével. A végtermék a keringésbe kerül és metabolizálódik a bél mucosájában, illetve a vesében, így újra felszabadítva az ammóniát. Az első tézis a túlzott ammónia akkumuláción alapszik. A különböző eredetű máj elégtelenségek következtében csökken az ammónia detoxifikáció, míg PSS során az ammóniában gazdag vér közvetlenül a szisztémás keringésbe jut, így okozva hyperammonaemiát. Az agy mentes az urea ciklustól, helyette a hatékony ammónia eltávolítás érdekében glutamin szintézis folyik az astrocytákban. Normális esetben a folyamat a következő: Az idegi stimuláció glutamát felszabadulást eredményez, ami egy, a preszinaptikus sejtekből származó, serkentő neurotranszmitter. Az astrocyták felveszik a felesleges glutamátot a szinaptikus résből, majd a vérből származó ammóniával együtt glutaminná alakítják azt. A glutamin ezután aktívan kiválasztódik az astrocytából és a preszinaptikus idegvégződés veszi fel, ahol ismét glutamáttá alakul, így újra felhasználhatóvá válik a neurotranszmissziós folyamatokban. Az astrocyta ezáltal megvédi az agyat a túlzott ingerületátviteltől. Hyperammonaemia esetén fokozódik a glutamin termelés, a leadás viszont gátlódik, ezáltal felhalmozódik a sejtekben. Az ozmotikusan aktív glutamin vizet vonz a sejtbe, agyi ödémát okozva. |
| Line 83: | Line 67: |
| ''Ammónia a fehérjék és urea lebontása során keletkezik a bélben, illetve az enterocyták glutamin anyagcseréje folyamán. A periportális hepatocytába a portális vénán keresztül jut az ammónia, ahol nagy része bikarbonát ionnal karbamoil foszfáttá alakul (CP). A CP az urea ciklusban citrullin – arginoszukcinát – arginin - ornitin átalakulásokon megy keresztül. Az így keletkező urea a szisztémás keringésbe kerül, majd a vesék választják ki. Az ammónia azon része, melyből nem keletkezik urea, a perivénás hepatocytákba kerül, ahol glutaminná alakul. Ezt végül a vese választja ki, vagy visszakerül az enterocytákba. Ennek köszönhetően az ammónia nem kerül a szisztémás keringésbe. '' | A sejten belüli ödémát súlyosbítja az astrocyta ammónia metabolizmusa, ezt '''„Trójai faló”''' hipotézisként ismerjük. A hipotézis szerint amikor az ammónia reagál a glutamáttal az astrocytán belül, glutamint alkotva, a glutamin a mitokondriumokba kerül. A mitokondrium ammóniaszint-emelkedése reaktív nitrogén és oxigén gyökök kialakulásához vezet, ami meggátolja az astrocytát a hatékony intracelluláris térfogatszabályozásban. Ez további cytotoxikus agyi ödémához vezet. Az ammónia felhalmozódásának eredményeképp csökken az agyi glükóz és oxigén metabolizmus, nő a vérkeringés redisztribúciója a kérgi területről a szubkortikális régiókhoz, és a vér-agy gát permeabilitása emelkedik ammóniára nézve. Az astrocyták megduzzadása az akut HE kritikus komponense. Az A típusú HE során fellépő agyi ödéma növekvő intrakraniális nyomáshoz, agysérvhez és halálhoz vezet. Kismértékű agyi ödéma rendszerint a B és C típusú HE során jelentkezik. A hyperammonaemia számos agyra gyakorolt hatása ellenére a vérammónia szint nincs szoros összefüggésben a HE klinikai tüneteivel, ami arra enged következtetni, hogy az ammónia nem az egyedüli tényező a HE kialakításában. |
| Line 87: | Line 71: |
| Normál ammónia metabolizmus során az ammónia eléri a májat a portális keringésen keresztül. Az ammónia nagy része az urea ciklusba kerül majd a vesék által exkretálódik. A maradék felhasználódik a glutamát-glutamin átalakulás során a glutamin szintetáz segítségével. A végtermék a keringésbe kerül és metabolizálódik a bél mucosájában, illetve a vesében, így újra felszabadítva az ammóniát. Az első tézis a túlzott ammónia akkumuláción alapszik. A különböző eredetű máj elégtelenségek következtében csökken az ammónia detoxifikáció, míg PSS során az ammóniában gazdag vér közvetlenül a szisztémás keringésbe jut, így okozva hyperammonaemiát. Az agy mentes az urea ciklustól, helyette a hatékony ammónia eltávolítás érdekében glutamin szintézis folyik az astrocytákban. Normális esetben a folyamat a következő: Az idegi stimuláció glutamát felszabadulást eredményez, ami egy, a preszinaptikus sejtekből származó, serkentő neurotranszmitter. Az astrocyták felveszik a felesleges glutamátot a szinaptikus résből, majd a vérből származó ammóniával együtt glutaminná alakítják azt. A glutamin ezután aktívan kiválasztódik az astrocytából és a preszinaptikus idegvégződés veszi fel, ahol ismét glutamáttá alakul, így újra felhasználhatóvá válik a neurotranszmissziós folyamatokban. Az astrocyta ezáltal megvédi az agyat a túlzott ingerületátviteltől. Hyperammonaemia esetén fokozódik a glutamin termelés, a leadás viszont gátlódik, ezáltal felhalmozódik a sejtekben. Az ozmotikusan aktív glutamin vizet vonz a sejtbe, agyi ödémát okozva. Ez kritikus komponense a HE kialakulásának, mert megnövekedett koponyaűri nyomáshoz, agysérvhez, majd halálhoz vezet. |
|
| Line 101: | Line 73: |
| ''B. ''''Gyulladás'' |
==== Gyulladás ==== |
| Line 105: | Line 76: |
''C. ''''Glutamát transzmisszió megváltozása'' |
==== Glutamát transzmisszió megváltozása ==== |
| Line 117: | Line 83: |
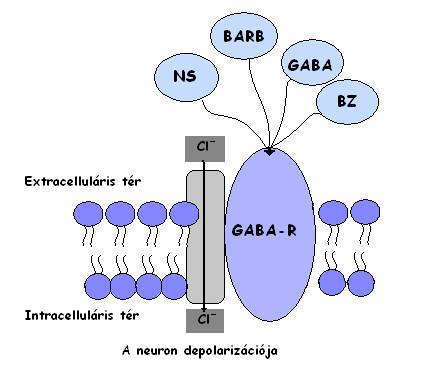
| ''D. ''''GABA agonisták szintjének megemelkedése'' | ==== GABA agonisták szintjének megemelkedése ==== ||<tablebgcolor="#eeeeee" tablestyle="float:center;font-size:0.85em;margin:0 0 0 0; "style="padding:0.5em; ;text-align:center"> {{attachment:1420300_10151965658879526_1336270842_n.jpg|felugró szöveg}} <<BR>>'''2. Ábra: A GABA receptor komplex'''<<BR>>''A receptor komplex egy GABA receptorból (GABA-R) és egy kloridion csatornából áll. A GABA receptorhoz történő kötése nyitja az ioncsatornát, a membrán hyperpolarizálódik, a neurotranszmisszió gátlódik. A receptor komplex benzodiazepin (BZ), barbiturátok (BARB) és neuroszteroidok (NS) általi aktivációja elősegíti a GABA receptorhoz történő kötődését.'' || |
| Line 119: | Line 86: |
| ''A GABA receptor komplex | |
| Line 121: | Line 87: |
| '' | A GABA hipotézis a megnövekedett, vagy lecsökkent érzékenységre alapul GABA-val (GABA: gamma aminobutric acid - egy gátló neurotranszmitter) szemben. A GABA a béltraktusból származik. HE esetén a plazma GABA szintje nő, mivel a máj kiválasztó funkciója csökken. Ez esetben a vér-agy gát átjárhatósága nő, így a GABA bejut az agyba és aktiválja a receptor komplexet. A klorid csatornák nyitnak, és az így fellépő hyperpolarizáció miatt gátlás alakul ki a központi idegrendszerben. Kialakítva a HE tüneteinek egy részét. Ez magyarázza a következő jelenséget: |
| Line 123: | Line 89: |
| ''A receptor komplex egy GABA receptorból (GABA-R) és egy kloridion csatornából áll. A GABA receptorhoz történő kötése nyitja az ioncsatornát, a membrán hyperpolarizálódik, a neurotranszmisszió gátlódik. A receptor komplex benzodiazepin (BZ), barbiturátok (BARB) és neuroszteroidok (NS) általi aktivációja elősegíti a GABA receptorhoz történő kötődését.'' | . Egy akut májelégtelenség miatt kómában lévő nyúl modellben vizuális ingerek által keltett akciós potenciál kialakulást mértek. Az eredmények megegyeztek a drogokkal indukált kómában mérhető potenciál értékekkel. A drogok a GABA receptor komplexet aktiválták úgy, mint benzodiazepin, vagy barbiturát agonisták.''(2.Ábra)'' ==== Benzodiazepin szerű ligandok növekedése ==== A máj csökkenő filtrációs funkciójának következtében a benzodiazin szerű anyagok koncentrációja megemelkedik a plazmában. A benzodiazin receptorok az astrocyták mitokondriumainak külső membránján helyezkednek, és a számuk megemelkedik mind az akut, mind a krónikus HE esetén. A receptoroknak szerepe van a neuroszteroidok szintézisében, ezen anyagok pedig GABA agonisták. A GABA és az ammónia teória nem kizárólagosak. Egyes tanulmányokban az ammónia közvetlenül emeli a GABA általi neurotranszmissziót illetve növeli a benzodiazepin agonisták hatását. ==== Megváltozott szerotoninerg szisztéma ==== Megfigyelhető emberek és állatok HE-je esetében szerotonin, Ser receptor és monoamin oxidáz szintjének emelkedése. Humán kísérletek során leírták egy szerotonin praecursor, a triptofán koncentrációjának megemelkedését a plazmában májelégtelenség során. Az összefüggés a plazma triptofán szintje és a HE között még nem teljesen bizonyított, de feltehetően nem jelentős a szerepe a patogenezisben. ==== Megváltozott aminosav metabolizmus ==== HE során az aromás aminosavak szintje nő, míg az elágazó láncú aminosavak plazmakoncentrációja csökken. Ennek a jelentősége abban rejlik, hogy aromás láncú aminosavak hatására a központi idegrendszerben a dopamin és a noradrenalin által indukált neurotranszmisszió blokkolása következik be. Így a központi idegrendszer gátlás alá kerül. ==== Mangán mérgezés ==== Mivel a máj felelős a mangán (Mn) exkréciójáért, a máj betegségek együtt járhatnak a plazma Mn-szint emelkedésével illetve az agy Mn akkumulációjával. Ez pedig jelentős befolyással bír a glutamát és a dopamin-függő neurotranszmisszióra. ==== A kevert neurotranszmitterek megváltozása ==== Kísérletesen indukált HE esetében a taurin (gátló neurotranszmitter) szint nő, ez pedig korrelál a HE súlyosbodásával. Egyéb neurotranszmitterek hatásában is változás figyelhető meg: így az opioidok, a melatonin, a merkaptán illetve a rövid láncú zsírsavak szintje is megváltozik HE esetén. Összegezve tehát, a HE minden anyagra hatással van, ami a bélflóra produktumból származtatható. Ezek hatását egyes tanulmányok tagadják, mások alátámasztják. Végeredményben a HE patogenezise legjobban úgy magyarázható, mint több összefüggő faktor hatás együttese. A megfelelő kezelés kiválasztásához szükséges a HE klinikai tüneteit kialakító tényezők alapos megértése. A HE patogenezisének legfontosabb aspektusait a jövőbeni kutatások tovább tisztázhatják, emellett újabb teóriák bevezetésére is mód nyílhat, amelyek hozzájárulhatnak a szindróma mélyebb megértéséhez. ''(Salgado és Cortes, 2013)'' === A HE hatása a tanulásra === Egy, az Oviedoi Egyetemen végzett kutatás eredményeként kiderült, hogy a HE hatással van a koncentrációs képességre és a memóriára is, ezáltal csökkentve a tanulás hatékonyságát. A megállapítást egy fordított tanulásra alapozott kísérlet, és az agy tanulásért felelős területein végbemenő metabolikus változások vizsgálata alapján tették.A kísérletben 14 hím patkány teljesítményét figyelték meg a Morris-féle vízi útvesztő tesztben, közülük 8 rendelkezett PSS illetve az ennek következményeként kialakult HE-val, és 6 egészséges egyed alkotta a kontrollcsoportot. A teszt során az állatoknak egy négy, egyforma kvadránsra felosztott, vízzel teli medencében kellett az adott kvadránsban elhelyezett víz alatti kilépőt megtalálni.''(3. Ábra)'' A medence körül több, a tájékozódást elősegítő tárgy is található volt. Egy kísérleti szekció alatt minden egyednek 4db egyperces, azonos időközökkel elválasztott próbálkozási lehetősége volt, hogy megtalálja a kilépőt. A fent leírtakat 4 napon keresztül ismételték, majd a kilépőt áthelyezték a medence pontosan átellenes részére, és a patkányok ismét 4 próbálkozási lehetőséget kaptak a kilépő új helyeződésének megtanulására. A kilépő megtalálásának időtartama, az időtartam csökkenése a kísérlet előrehaladtával, az egyes kvadránsokban eltöltött idő, a sebesség és a megtett távolságok feljegyzésre kerültek. A kísérlet után 90 perccel az állatokat lefejezték, agyukat érintetlenül lefagyasztották, majd a megfelelő kezelési eljárások után hisztokémiai vizsgálatnak vetették alá. A vizsgálat, és a feljegyzett adatok alapján az alábbi következtetések vonhatóak le: * a PSS csoportba tartozó patkányok lassabban tanulták meg a kilépő helyeződését * a kilépő fordított helyeződését pedig képtelenek voltak memorizálni Eredmény: Az új körülményekhez szükséges adaptációs készség csökken, amit az ezen funkcióért felelős agyterületekben mérhető citokróm-oxidáz koncentrációjának csökkenése is mutat (a kontroll csoportnál mért koncentrációhoz képest). ''(Méndez és mtsai, 2011)'' ||<tablebgcolor="#eeeeee" tablestyle="float:center;font-size:0.85em;margin:0 0 0 0; "style="padding:0.5em; ;text-align:center"> {{attachment:morris.jpg|felugró szöveg}} <<BR>>'''3. Ábra'''<<BR>>''Morris-féle vízi útvesztő'' || |
| Line 128: | Line 124: |
A GABA hipotézis a megnövekedett, vagy lecsökkent érzékenységre alapul GABA-val (GABA: gamma aminobutric acid - egy gátló neurotranszmitter) szemben. A GABA a béltraktusból származik. HE esetén a plazma GABA szintje nő, mivel a máj kiválasztó funkciója csökken. Ez esetben a vér-agy gát átjárhatósága nő, így a GABA bejut az agyba és aktiválja a receptor komplexet. A klorid csatornák nyitnak, és az így fellépő hyperpolarizáció miatt gátlás alakul ki a központi idegrendszerben. Kialakítva a HE tüneteinek egy részét. Ez magyarázza a következő jelenséget: Egy akut májelégtelenség miatt kómában lévő nyúl modellben vizuális ingerek által keltett akciós potenciál kialakulást mértek. Az eredmények megegyeztek a drogokkal indukált kómában mérhető potenciál értékekkel. A drogok a GABA receptor komplexet aktiválták úgy, mint benzodiazepin, vagy barbiturát agonisták. ''E. ''''Benzodiazepin szerű ligandok növekedése'' A máj csökkenő filtrációs funkciójának következtében a benzodiazin szerű anyagok koncentrációja megemelkedik a plazmában. A benzodiazin receptorok az astrocyták mitokondriumainak külső membránján helyezkednek, és a számuk megemelkedik mind az akut, mind a krónikus HE esetén. A receptoroknak szerepe van a neuroszteroidok szintézisében, ezen anyagok pedig GABA agonisták. A GABA és az ammónia teória nem kizárólagosak. Egyes tanulmányokban az ammónia közvetlenül emeli a GABA általi neurotranszmissziót illetve növeli a benzodiazepin agonisták hatását. ''F. ''''Megváltozott szerotoninerg szisztéma'' Megfigyelhető emberek és állatok HE-je esetében szerotonin, Ser receptor és monoamin oxidáz szintjének emelkedése. Humán kísérletek során leírták egy szerotonin praecursor, a triptofán koncentrációjának megemelkedését a plazmában májelégtelenség során. Az összefüggés a plazma triptofán szintje és a HE között még nem teljesen bizonyított, de feltehetően nem jelentős a szerepe a patogenezisben. ''G. ''''Megváltozott aminosav metabolizmus'' HE során az aromás aminosavak szintje nő, míg az elágazó láncú aminosavak plazmakoncentrációja csökken. Ennek a jelentősége abban rejlik, hogy aromás láncú aminosavak hatására a központi idegrendszerben a dopamin és a noradrenalin által indukált neurotranszmisszió blokkolása következik be. Így a központi idegrendszer gátlás alá kerül. ''H. ''''Mangán mérgezés'' Mivel a máj felelős a mangán (Mn) exkréciójáért, a máj betegségek együtt járhatnak a plazma Mn-szint emelkedésével illetve az agy Mn akkumulációjával. Ez pedig jelentős befolyással bír a glutamát és a dopamin-függő neurotranszmisszióra. ''I. ''''A kevert neurotranszmitterek megváltozása'' Kísérletesen indukált HE esetében a taurin (gátló neurotranszmitter) szint nő, ez pedig korrelál a HE súlyosbodásával. Egyéb neurotranszmitterek hatásában is változás figyelhető meg: így az opioidok, a melatonin, a merkaptán illetve a rövid láncú zsírsavak szintje is megváltozik HE esetén. Összegezve tehát, a HE minden anyagra hatással van, ami a bélflóra produktumból származtatható. Ezek hatását egyes tanulmányok tagadják, mások alátámasztják. Végeredményben a HE patogenezise legjobban úgy magyarázható, mint több összefüggő faktor hatás együttese. A megfelelő kezelés kiválasztásához szükséges a HE klinikai tüneteit kialakító tényezők alapos megértése. A HE patogenezisének legfontosabb aspektusait a jövőbeni kutatások tovább tisztázhatják, emellett újabb teóriák bevezetésére is mód nyílhat, amelyek hozzájárulhatnak a szindróma mélyebb megértéséhez. '''II/4. A HE hatás a tanulásra''' Egy, az Oviedoi Egyetemen végzett kutatás eredményeként kiderült, hogy a HE hatással van a koncentrációs képességre és a memóriára is, ezáltal csökkentve a tanulás hatékonyságát. A megállapítást egy fordított tanulásra alapozott kísérlet, és az agy tanulásért felelős területein végbemenő metabolikus változások vizsgálata alapján tették. A kísérletben 14 hím patkány teljesítményét figyelték meg a Morris-féle vízi útvesztő tesztben, közülük 8 rendelkezett PSS illetve az ennek következményeként kialakult HE-val, és 6 egészséges egyed alkotta a kontrollcsoportot. A teszt során az állatoknak egy négy, egyforma kvadránsra felosztott, vízzel teli medencében kellett az adott kvadránsban elhelyezett víz alatti kilépőt megtalálni. A medence körül több, a tájékozódást elősegítő tárgy is található volt. Egy kísérleti szekció alatt minden egyednek 4db egyperces, azonos időközökkel elválasztott próbálkozási lehetősége volt, hogy megtalálja a kilépőt. A fent leírtakat 4 napon keresztül ismételték, majd a kilépőt áthelyezték a medence pontosan átellenes részére, és a patkányok ismét 4 próbálkozási lehetőséget kaptak a kilépő új helyeződésének megtanulására. A kilépő megtalálásának időtartama, az időtartam csökkenése a kísérlet előrehaladtával, az egyes kvadránsokban eltöltött idő, a sebesség és a megtett távolságok feljegyzésre kerültek. A kísérlet után 90 perccel az állatokat lefejezték, agyukat érintetlenül lefagyasztották, majd a megfelelő kezelési eljárások után hisztokémiai vizsgálatnak vetették alá. A vizsgálat, és a feljegyzett adatok alapján az alábbi következtetések vonhatóak le: * a PSS csoportba tartozó patkányok lassabban tanulták meg a kilépő helyeződését * a kilépő fordított helyeződését pedig képtelenek voltak memorizálni à az új körülményekhez szükséges adaptációs készség csökken, amit az ezen funkcióért felelős agyterületekben mérhető citokróm-oxidáz koncentrációjának csökkenése is mutat (a kontroll csoportnál mért koncentrációhoz képest). '' {{file:///C:/Users/Borka/AppData/Local/Temp/OICE_C96069C6-188F-452D-BC0F-67BB8B718B51.0/msohtmlclip1/01/clip_image004.jpg|Description: C:\Users\Lőrinc\Desktop\1457077_10151965659424526_2035898882_n.jpg|width="605",height="411",v:shapes="Kép_x0020_293"}} '''''' |
|
| Line 183: | Line 126: |
| '''III. Egyéb idegrendszeri hatások''' | == III. Egyéb idegrendszeri hatások == A fent leírtak mellett egyéb neurológiai tünetek is jelentkezhetnek, akár az állapot műtéti kezelése után is. |
| Line 185: | Line 129: |
| A fent leírtak mellett egyéb neurológiai tünetek is jelentkezhetnek, akár az állapot műtéti kezelése után is. | Egyes tanulmányok szerint a CPSS beavatkozásos csökkentése után a vizsgált kutyák 12%-a mutatott idegrendszeri tüneteket, melyek nem voltak összefüggésben sem a HE-val, sem pedig a hypoglycaemiával, mivel a vizsgált kutyák vérében mind az ammónia, mind a vércukorszint közel állt a normálishoz.A tapasztalt tünetek súlyossága változó, előfordult közöttük ataxia, dezorientáció, de motorikus rohamok is, melyek egyes esetekben epilepsziás státuszig fejlődtek. A szövődmények megjelenésének oka nem bizonyult egyértelműnek, de felismertek bizonyos faktorokat (fajta, nem, kor), melyek növelhetik a kialakulás kockázatát. ''(Tisdall és mtsai, 2000)'' |
| Line 187: | Line 131: |
| Egyes tanulmányok szerint a CPSS beavatkozásos csökkentése után a vizsgált kutyák 12%-a mutatott idegrendszeri tüneteket, melyek nem voltak összefüggésben sem a HE-val, sem pedig a hypoglycaemiával, mivel a vizsgált kutyák vérében mind az ammónia, mind a vércukorszint közel állt a normálishoz. | Egyéb kutatások, melyek az artériás és a portális vérben előforduló belsőleges benzodiazepin receptor ligandok (EBZ) koncentrációját vizsgálták, kimutatták, hogy a kutatásban résztvevő CPSS-el rendelkező kutyák nagy részének vérében jelentősen magasabb az EBZ szint. Mivel a gasztrointesztinális traktus vére az, ami sönt által kikerüli a májat, az emelkedett ligand koncentráció arra enged következtetni, hogy az EBZ termelés ezen szakaszon intenzív. Ha a sönt műtéti úton csökkentésre kerül, a szisztémás keringésbe kerülő gasztrointesztinális vér mennyisége is csökken, így következetesen az EBZ szint is alacsonyabb lesz, ami az EBZ eredeti, gátló hatásának ellentétét, stimulációt vált ki. Ez lehet a műtéti beavatkozások után jelentkező motorikus rohamok előfordulásának lehetséges oka. ''(Aronson és mtsai, 1997)'' |
| Line 189: | Line 133: |
| A tapasztalt tünetek súlyossága változó, előfordult közöttük ataxia, dezorientáció, de motorikus rohamok is, melyek egyes esetekben epilepsziás státuszig fejlődtek. A szövődmények megjelenésének oka akkor még nem bizonyult egyértelműnek, de felismertek bizonyos faktorokat (fajta, nem, kor), melyek növelhetik a kialakulás kockázatát. Későbbi kutatások, melyek az artériás és a portális vérben előforduló belsőleges benzodiazepin receptor ligandok (EBZ) koncentrációját vizsgálták, kimutatták, hogy a kutatásban résztvevő CPSS-el rendelkező kutyák nagy részének vérében jelentősen magasabb az EBZ szint. Mivel a gasztrointesztinális traktus vére az, ami sönt által kikerüli a májat, az emelkedett ligand koncentráció arra enged következtetni, hogy az EBZ termelés ezen szakaszon intenzív. Ha a sönt műtéti úton csökkentésre kerül, a szisztémás keringésbe kerülő gasztrointesztinális vér mennyisége is csökken, így következetesen az EBZ szint is alacsonyabb lesz, ami az EBZ eredeti, gátló hatásának ellentétét, stimulációt vált ki. Ez lehet a műtéti beavatkozások után jelentkező motorikus rohamok előfordulásának lehetséges oka. '' '' '''IV. Diagnosztika''' |
== IV. Diagnosztika == |
| Line 203: | Line 136: |
| · vörösvérsejtek méretének csökkenése | * vörösvérsejtek méretének csökkenése |
| Line 205: | Line 138: |
| · fehérvérsejtek számának emelkedése | * fehérvérsejtek számának emelkedése |
| Line 207: | Line 140: |
| · összfehérje szám, albumin, BUN (blood urea nitrogen) mennyiségének csökkenése | * összfehérje szám, albumin, BUN (blood urea nitrogen) mennyiségének csökkenése |
| Line 209: | Line 142: |
| · éhgyomri és etetés utáni epesavak mennyiségének emelkedése | * éhgyomri és etetés utáni epesavak mennyiségének emelkedése |
| Line 211: | Line 144: |
| · vérammónia szint emelkedése | * vérammónia szint emelkedése |
| Line 213: | Line 146: |
| · Protein C koncentráció csökkenése | * Protein C koncentráció csökkenése |
| Line 215: | Line 148: |
| A laborvizsgálatok mellett a PSS kimutatható más módszerekkel is. Hasi röntgenfelvételen a máj általában kisebb, zsugorodott. Ultrahangvizsgálattal is megkereshető a sönt. Szcintigráfia során radioaktív anyagokat juttatnak a vastagbélbe vagy a lépbe és egy speciális kamerával követik ezek keringésbeli útját. Ha az anyagok több, mint 5%-a közvetlenül a szívbe jut, PSS jelenléte feltételezhető. Portogram készítése során kontrasztanyagokat injektálnak a hasűri erekbe, majd röntgenfelvételt készítenek a területről. Ez egy invazív eljárás, azonban jól láthatóan bizonyítja a sönt jelenlétét és helyzetét, és megfelelő eszközök segítségével műtét közben is elvégezhető. CT vizsgálattal az intra- és extrahepatikus sönt is jó eséllyel kimutatható. | A laborvizsgálatok mellett a PSS kimutatható más módszerekkel is. Hasi röntgenfelvételen a máj általában kisebb, zsugorodott. Ultrahangvizsgálattal is megkereshető a sönt. Szcintigráfia során radioaktív anyagokat juttatnak a vastagbélbe vagy a lépbe és egy speciális kamerával követik ezek keringésbeli útját. Ha az anyagok több, mint 5%-a közvetlenül a szívbe jut, PSS jelenléte feltételezhető. Portogram készítése során kontrasztanyagokat injektálnak a hasűri erekbe, majd röntgenfelvételt készítenek a területről. Ez egy invazív eljárás, azonban jól láthatóan bizonyítja a sönt jelenlétét és helyzetét, és megfelelő eszközök segítségével műtét közben is elvégezhető. CT vizsgálattal az intra- és extrahepatikus sönt is jó eséllyel kimutatható ''(Tobias, 2003)''. |
| Line 217: | Line 150: |
| '''V. Kezelés''' | == V. Kezelés == Extrahepatikus sönt esetén lehetséges a sönt műtéti úton történő okklúziója. Ilyenkor a söntöt a lehető legközelebb zárják le a vena cava-ba történő betorkollásához. Az ameroid konstriktor használata hatékony módja a sönt lezárásának, ami egy acélhüvelybe foglalt kazein gyűrű. A kazein folyadékabszorpciója során megduzzad és lezárja az eret ''(Tobias, 2003)''. |
| Line 219: | Line 153: |
| Extrahepatikus sönt esetén lehetséges a sönt műtéti úton történő okklúziója. Ilyenkor a söntöt a lehető legközelebb zárják le a vena cava-ba történő betorkollásához. Az ameroid konstriktor használata hatékony módja a sönt lezárásának, ami egy acélhüvelybe foglalt kazein gyűrű. A kazein folyadékabszorpciója során megduzzad és lezárja az eret. | == VI. Felhasznált irodalom == [[http://onlinelibrary.wiley.com/doi/10.1111/j.1532-950X.1997.tb01483.x/abstract|Aronson L.R., Gacad R.C., Kaminsky-Russ K., Gregory C.R., Mullen K.D. (1997): Endogenous Benzodiazepine Activity in the Peripheral and Portal Blood of Dogs With Congenital Portosystemic Shunts, Veterinary Surgery 26:(3) 189-193]] [[http://www.vet.utk.edu/clinical/sacs/shunt/index.php|College of Veterinary Medicine, Tennessee, USA]] [[http://arxiv.org/ftp/arxiv/papers/1111/1111.2957.pdf|Méndez M., Méndez-López M., López L., Aller M.A., Arias J., Arias J.L. (2011): Portosystemic hepatic encephalopathy model shows reversal learning impairment and dysfunction of neural activity in the prefrontal cortex and regions involved in motivated behavior, Journal of Clinical Neuroscience 18:(5) 690-4.]] [[https://s3.amazonaws.com/assets.prod.vetlearn.com/d7/a169a0bc0e11e2b140005056ad4734/file/PV2013_Salgado1_CE.pdf|Salgado M., Cortes Y. (2013): Hepatic Encephalopathy, Etiology, Pathogenesis, and Clinical Signs]] [[http://onlinelibrary.wiley.com/doi/10.1111/j.1748-5827.2000.tb03150.x/abstract|Tisdall P.L.C. , Hunt G.B., Youmans K.R., Malik R. (2000): Neurological dysfunction in dogs following attenuation of congenital extrahepatic portosystemic shunts, Journal of Small Animal Practice 41:(12) 539-546]] [[http://www.vet.utk.edu/clinical/sacs/shunt/MVD-Brochure-FINAL2013-09-26.pdf|Tobias K.M. (2013): Brief Overview of Portosystemic Shunts]] ---- (Az ábrák és a táblázat saját készítésűek) |
A portoszisztémás sönt idegrendszeri következményei
Contents
I. A betegségről általában
A portoszisztémás sönt (PSS) egy érrendszert érintő anomália, minek jelenlétekor a hasüregi szervektől a vér a máj megkerülésével közvetlenül a szívbe jut, így a felszívott tápanyagok a szisztémás keringésbe kerülnek. A máj végzi a tápanyagok későbbi felhasználás céljából történő raktározását, bizonyos, szervezetre káros anyagok biztonságossá alakítását, illetve fehérjéket és más molekulákat szintetizál. PSS esetén a máj nem képes elvégezni ezen feladatait, minek következtében toxinok szaporodnak fel a véráramban. Ezen kívül az állat hiányt szenved azokban a tápanyagokban, amelyek alapvető fontosságúak a növekedés energiaszükségletének biztosításában.
Különböző típusú portoszisztémás söntöket különböztetünk meg attól függően, hogy mikor alakulnak ki, a májon belül vagy kívül, és hány ér alkotja a söntöt.
Egyszeres sönt
Általában veleszületett, a vena portae-t a vena cava caudalishoz köti.
extrahepatikus - a veleszületett söntök közül a leggyakoribb, elsősorban kistestű fajtákra jellemző (yorkshire terrier, schnauzer, uszkár, máltai, Shih Tzu, tacskó)
intrahepatikus – nagyobb testű kutyákra jellemző (ír farkas, golden és Labrador retriever, szamojéd)
Máltaiban és ír farkasban örökletes, feltételezések szerint yorkie-ban is, míg macskákban mindkét típus előfordulhat.
Többszörös sönt
Szerzett, a vena portaeban uralkodó tartósan magas nyomás hatására és cirrhosis esetén alakul ki. A német juhászok és a dobermannok hajlamosak a betegségre, ez a rendellenesség műtéttel nem korrigálható
Minden emlős magzat rendelkezik ductus venosussal, ami a magzat májából a szívbe továbbítja a vért (az anyai méh látja el a feladatokat). Ez fiziológiás esetben zárul az utód születése után, ha ez nem történik meg, intrahepatikus sönt alakul ki (patent ductus venosus). Veleszületett extrahepatikus sönt esetén egy májon kívüli ér abnormálisan fejlődik, és a ductus venosus zárulása után is nyitott marad.
Veleszületett portoszisztémás sönt (CPSS) által érintett kutya klinikai tünetei
CPSS-el bíró kutyák esetén a tünetek fiatal korban jelentkeznek, kivéve, ha a vér megszakításokkal áramlik és a sönt kisméretű. Az ilyen egyedek kisebb testűek, alulfejlettek, gyenge izomzattal és egészségtelen küllemű bundával rendelkeznek. Viselkedésbeli problémák is előfordulnak, mint a gyengeség, csendes magatartás, apátia. Az idegrendszeri tünetek általában súlyosabbak, főleg alacsony vércukorszint és nagy mennyiségű protein bevitele esetén. Előfordulhat fel-alá járkálás, körözés, látászavar, a fej falhoz való odanyomása és rohamok. Mivel a máj nem dolgoz fel fehérjéket és ammóniát, utóbbi nagy mennyiségben kerül a kiválasztórendszerbe, ahol kristályokat képezhet (ammónium-biurát, urát kövek). Ez húgyúti gyulladáshoz és fertőzéshez vezethet. Az érintett kutyák képtelenné válnak vizeletük koncentrálására, így több vizeletet ürítenek, ezáltal többet is isznak. A tünetek között előfordulhat továbbá szédülés, étvágyvesztés, hányás, nyálzás, illetve gyomorfekély is kialakulhat.
Többszörös, szerzett portoszisztémás sönt által érintett kutya klinikai tünetei
Ezen rendellenesség esetén idősebb korban lépnek fel a tünetek, néha kölykökben is kialakulhatnak. Sok esetben a máj károsodásának következménye a sönt kialakulása, például egy bizonyos méreg fogyasztása komoly májbetegséghez vezet, a májnak megnő az ellenállása. A kutya szemfehérje, bőre, ínye sárgás színelváltozást mutat, ha az epeutak is érintettek. Nagyon magas portális nyomás vagy hypoproteinaemia esetén a filtráció mértéke nő, pangó hasűri folyadék keletkezk (ascites). A máj kiesett működése miatt véralvadási zavarok, bevérzések jelenhetnek meg (Tobias, 2003).
II. Hepatikus encefalopátia
A hepatikus encefalopátia (HE) úgy definiálható, mint a máj működésbeli zavarának következtében kialakuló neurológiai tünet együttes, mely tulajdonképpen a központi idegrendszerben a csökkenő neuron aktivitás által létrehozott abnormális mentális státusz. A HE leggyakrabban PSS következménye. A patogenezis nem teljesen tisztázott, inkább csak teóriák vannak a kialakulásával kapcsolatban. A csökkenő neuron aktivitást lényegében az okozza, hogy a toxikus anyagcsere termékek akkumulálódnak az agyban, mivel valamilyen okból kifolyólag nem bomlanak le a májban.
Csoportosítás
- A HE a májjal kapcsolatos megbetegedések és a klinikai tünetek alapján csoportokba sorolható.
1. Klinikai tünetek alapján. Ezt a csoportosítást az alábbi táblázat szemlélteti. (Táblázat 1.)
|
2. A humán orvostudomány 3 fő típusba sorolja a HE-t a máj diszfunkciói alapján, és ezt a csoportosítást az állatorvoslás is átvette.
- Az A típusú HE májelégtelenséggel van kapcsolatban.
- A B típus PSS jelenlétével van összefüggésben, azonban májelégtelenséggel nem társul.
- A különböző máj parenchima elégtelenséggel és portális vérnyomás emelkedéssel kapcsolatos C típus gyakran társul szerzett PSS-el. Ez a leggyakoribb humán esetekben, míg állatoknál a B a leggyakrabban előforduló HE típus.
Patogenezis
Egy egyedüli máj vagy idegrendszeri abnormális metabolizmus sem magyarázza teljesen a HE összes tünetét, bár a hyperammonaemia valószínűleg kulcsszereppel bír a HE kialakulásában.
Teóriák
Megváltozott ammónia metabolizmus
|
Az ammónia négy mechanizmus során keletkezik a szervezetben: (1) ureázt termelő mikroorganizmusok által a vastagbélben, amelyek a bélben lévő fehérjéket és az ureát bontják, (2) a táplálékból felvett aminosavak májban végbemenő metabolizmusa, (3) a glutamin enterocytákban zajló metabolizmusa, és (4) perifériás szövet (izom) katabolizmusa. A vérben található ammónia több, mint 50 %-a a bélben történő fehérje- és ureabontásból származik. Normál ammónia metabolizmus során (1. Ábra) az ammónia eléri a májat a portális keringésen keresztül. Az ammónia nagy része az urea ciklusba kerül majd a vesék által exkretálódik. A maradék felhasználódik a glutamát-glutamin átalakulás során a glutamin szintetáz segítségével. A végtermék a keringésbe kerül és metabolizálódik a bél mucosájában, illetve a vesében, így újra felszabadítva az ammóniát. Az első tézis a túlzott ammónia akkumuláción alapszik. A különböző eredetű máj elégtelenségek következtében csökken az ammónia detoxifikáció, míg PSS során az ammóniában gazdag vér közvetlenül a szisztémás keringésbe jut, így okozva hyperammonaemiát. Az agy mentes az urea ciklustól, helyette a hatékony ammónia eltávolítás érdekében glutamin szintézis folyik az astrocytákban. Normális esetben a folyamat a következő: Az idegi stimuláció glutamát felszabadulást eredményez, ami egy, a preszinaptikus sejtekből származó, serkentő neurotranszmitter. Az astrocyták felveszik a felesleges glutamátot a szinaptikus résből, majd a vérből származó ammóniával együtt glutaminná alakítják azt. A glutamin ezután aktívan kiválasztódik az astrocytából és a preszinaptikus idegvégződés veszi fel, ahol ismét glutamáttá alakul, így újra felhasználhatóvá válik a neurotranszmissziós folyamatokban. Az astrocyta ezáltal megvédi az agyat a túlzott ingerületátviteltől. Hyperammonaemia esetén fokozódik a glutamin termelés, a leadás viszont gátlódik, ezáltal felhalmozódik a sejtekben. Az ozmotikusan aktív glutamin vizet vonz a sejtbe, agyi ödémát okozva.
A sejten belüli ödémát súlyosbítja az astrocyta ammónia metabolizmusa, ezt „Trójai faló” hipotézisként ismerjük. A hipotézis szerint amikor az ammónia reagál a glutamáttal az astrocytán belül, glutamint alkotva, a glutamin a mitokondriumokba kerül. A mitokondrium ammóniaszint-emelkedése reaktív nitrogén és oxigén gyökök kialakulásához vezet, ami meggátolja az astrocytát a hatékony intracelluláris térfogatszabályozásban. Ez további cytotoxikus agyi ödémához vezet. Az ammónia felhalmozódásának eredményeképp csökken az agyi glükóz és oxigén metabolizmus, nő a vérkeringés redisztribúciója a kérgi területről a szubkortikális régiókhoz, és a vér-agy gát permeabilitása emelkedik ammóniára nézve. Az astrocyták megduzzadása az akut HE kritikus komponense. Az A típusú HE során fellépő agyi ödéma növekvő intrakraniális nyomáshoz, agysérvhez és halálhoz vezet. Kismértékű agyi ödéma rendszerint a B és C típusú HE során jelentkezik. A hyperammonaemia számos agyra gyakorolt hatása ellenére a vérammónia szint nincs szoros összefüggésben a HE klinikai tüneteivel, ami arra enged következtetni, hogy az ammónia nem az egyedüli tényező a HE kialakításában.
Az ammóniával kapcsolatos teória rengeteg tünetet megmagyaráz, de így is sok a patogenezis lefedetlen területe.
Gyulladás
Egyes kutatások igazolták, hogy összefüggés van a gyulladásos folyamatok, mediátoraik (pl.: citokinek, tumor nekrózis faktorok vagy interleukin-6) és a HE kialakulásában. Lehetséges teóriák magyarázzák, hogyan befolyásolja a gyulladás a citokinek által irányított változásokon keresztül a vér-agy gát permeabilitását, így megváltoztatva a glutamát felvételt és a GABA receptor expressziót.
Glutamát transzmisszió megváltozása
A központi idegrendszer glutamáterg neurotranszmitter szisztémája megváltozik akut és krónikus HE során. Ahogy azt a fentiekben leírtuk az astrocyták védik az agyat a túlzott neurotranszmissziótól, úgy, hogy gátolják a glutamát kiszabadulását a preszinaptikus idegvégződésekből. A hyperammonaemia csökkenti az astrocyták glutamát felvételét, ami a megemelkedett extracelluláris glutamát szinthez vezethet.
A glutamát transzporter GLT-1 „down-regulációja” (A GLT-1 egy esszenciális transzporter a szinapszisban lévő gultamát inaktivációja során) volt megfigyelhető hyperammonaemiás patkányok esetében, mind PSS-el rendelkezőkben, mind kísérletesen indukált máj elégtelenségben szenvedő egyedekben. IV-es fokozatú HE során a magas ammónia koncentráció inaktiválja a neuronokból klorid iont eltávolító ionpumpát, depolarizálva ezzel a neuronokat és előidézve a neurológiai izgatottságot és a roham előtti státuszt.
Továbbá az idegrendszer emelkedő glutamát koncentráció általi stimulálása rohamokat is okozhat A és B, ritkábban C típusú HE-ben szenvedő állatokban.
GABA agonisták szintjének megemelkedése
|
A GABA hipotézis a megnövekedett, vagy lecsökkent érzékenységre alapul GABA-val (GABA: gamma aminobutric acid - egy gátló neurotranszmitter) szemben. A GABA a béltraktusból származik. HE esetén a plazma GABA szintje nő, mivel a máj kiválasztó funkciója csökken. Ez esetben a vér-agy gát átjárhatósága nő, így a GABA bejut az agyba és aktiválja a receptor komplexet. A klorid csatornák nyitnak, és az így fellépő hyperpolarizáció miatt gátlás alakul ki a központi idegrendszerben. Kialakítva a HE tüneteinek egy részét. Ez magyarázza a következő jelenséget:
Egy akut májelégtelenség miatt kómában lévő nyúl modellben vizuális ingerek által keltett akciós potenciál kialakulást mértek. Az eredmények megegyeztek a drogokkal indukált kómában mérhető potenciál értékekkel. A drogok a GABA receptor komplexet aktiválták úgy, mint benzodiazepin, vagy barbiturát agonisták.(2.Ábra)
Benzodiazepin szerű ligandok növekedése
A máj csökkenő filtrációs funkciójának következtében a benzodiazin szerű anyagok koncentrációja megemelkedik a plazmában. A benzodiazin receptorok az astrocyták mitokondriumainak külső membránján helyezkednek, és a számuk megemelkedik mind az akut, mind a krónikus HE esetén. A receptoroknak szerepe van a neuroszteroidok szintézisében, ezen anyagok pedig GABA agonisták.
A GABA és az ammónia teória nem kizárólagosak. Egyes tanulmányokban az ammónia közvetlenül emeli a GABA általi neurotranszmissziót illetve növeli a benzodiazepin agonisták hatását.
Megváltozott szerotoninerg szisztéma
Megfigyelhető emberek és állatok HE-je esetében szerotonin, Ser receptor és monoamin oxidáz szintjének emelkedése. Humán kísérletek során leírták egy szerotonin praecursor, a triptofán koncentrációjának megemelkedését a plazmában májelégtelenség során. Az összefüggés a plazma triptofán szintje és a HE között még nem teljesen bizonyított, de feltehetően nem jelentős a szerepe a patogenezisben.
Megváltozott aminosav metabolizmus
HE során az aromás aminosavak szintje nő, míg az elágazó láncú aminosavak plazmakoncentrációja csökken. Ennek a jelentősége abban rejlik, hogy aromás láncú aminosavak hatására a központi idegrendszerben a dopamin és a noradrenalin által indukált neurotranszmisszió blokkolása következik be. Így a központi idegrendszer gátlás alá kerül.
Mangán mérgezés
Mivel a máj felelős a mangán (Mn) exkréciójáért, a máj betegségek együtt járhatnak a plazma Mn-szint emelkedésével illetve az agy Mn akkumulációjával. Ez pedig jelentős befolyással bír a glutamát és a dopamin-függő neurotranszmisszióra.
A kevert neurotranszmitterek megváltozása
Kísérletesen indukált HE esetében a taurin (gátló neurotranszmitter) szint nő, ez pedig korrelál a HE súlyosbodásával. Egyéb neurotranszmitterek hatásában is változás figyelhető meg: így az opioidok, a melatonin, a merkaptán illetve a rövid láncú zsírsavak szintje is megváltozik HE esetén. Összegezve tehát, a HE minden anyagra hatással van, ami a bélflóra produktumból származtatható. Ezek hatását egyes tanulmányok tagadják, mások alátámasztják.
Végeredményben a HE patogenezise legjobban úgy magyarázható, mint több összefüggő faktor hatás együttese. A megfelelő kezelés kiválasztásához szükséges a HE klinikai tüneteit kialakító tényezők alapos megértése. A HE patogenezisének legfontosabb aspektusait a jövőbeni kutatások tovább tisztázhatják, emellett újabb teóriák bevezetésére is mód nyílhat, amelyek hozzájárulhatnak a szindróma mélyebb megértéséhez. (Salgado és Cortes, 2013)
A HE hatása a tanulásra
Egy, az Oviedoi Egyetemen végzett kutatás eredményeként kiderült, hogy a HE hatással van a koncentrációs képességre és a memóriára is, ezáltal csökkentve a tanulás hatékonyságát. A megállapítást egy fordított tanulásra alapozott kísérlet, és az agy tanulásért felelős területein végbemenő metabolikus változások vizsgálata alapján tették.A kísérletben 14 hím patkány teljesítményét figyelték meg a Morris-féle vízi útvesztő tesztben, közülük 8 rendelkezett PSS illetve az ennek következményeként kialakult HE-val, és 6 egészséges egyed alkotta a kontrollcsoportot.
A teszt során az állatoknak egy négy, egyforma kvadránsra felosztott, vízzel teli medencében kellett az adott kvadránsban elhelyezett víz alatti kilépőt megtalálni.(3. Ábra) A medence körül több, a tájékozódást elősegítő tárgy is található volt. Egy kísérleti szekció alatt minden egyednek 4db egyperces, azonos időközökkel elválasztott próbálkozási lehetősége volt, hogy megtalálja a kilépőt. A fent leírtakat 4 napon keresztül ismételték, majd a kilépőt áthelyezték a medence pontosan átellenes részére, és a patkányok ismét 4 próbálkozási lehetőséget kaptak a kilépő új helyeződésének megtanulására. A kilépő megtalálásának időtartama, az időtartam csökkenése a kísérlet előrehaladtával, az egyes kvadránsokban eltöltött idő, a sebesség és a megtett távolságok feljegyzésre kerültek. A kísérlet után 90 perccel az állatokat lefejezték, agyukat érintetlenül lefagyasztották, majd a megfelelő kezelési eljárások után hisztokémiai vizsgálatnak vetették alá. A vizsgálat, és a feljegyzett adatok alapján az alábbi következtetések vonhatóak le:
- a PSS csoportba tartozó patkányok lassabban tanulták meg a kilépő helyeződését
- a kilépő fordított helyeződését pedig képtelenek voltak memorizálni
Eredmény: Az új körülményekhez szükséges adaptációs készség csökken, amit az ezen funkcióért felelős agyterületekben mérhető citokróm-oxidáz koncentrációjának csökkenése is mutat (a kontroll csoportnál mért koncentrációhoz képest). (Méndez és mtsai, 2011)
|
III. Egyéb idegrendszeri hatások
A fent leírtak mellett egyéb neurológiai tünetek is jelentkezhetnek, akár az állapot műtéti kezelése után is.
Egyes tanulmányok szerint a CPSS beavatkozásos csökkentése után a vizsgált kutyák 12%-a mutatott idegrendszeri tüneteket, melyek nem voltak összefüggésben sem a HE-val, sem pedig a hypoglycaemiával, mivel a vizsgált kutyák vérében mind az ammónia, mind a vércukorszint közel állt a normálishoz.A tapasztalt tünetek súlyossága változó, előfordult közöttük ataxia, dezorientáció, de motorikus rohamok is, melyek egyes esetekben epilepsziás státuszig fejlődtek. A szövődmények megjelenésének oka nem bizonyult egyértelműnek, de felismertek bizonyos faktorokat (fajta, nem, kor), melyek növelhetik a kialakulás kockázatát. (Tisdall és mtsai, 2000)
Egyéb kutatások, melyek az artériás és a portális vérben előforduló belsőleges benzodiazepin receptor ligandok (EBZ) koncentrációját vizsgálták, kimutatták, hogy a kutatásban résztvevő CPSS-el rendelkező kutyák nagy részének vérében jelentősen magasabb az EBZ szint. Mivel a gasztrointesztinális traktus vére az, ami sönt által kikerüli a májat, az emelkedett ligand koncentráció arra enged következtetni, hogy az EBZ termelés ezen szakaszon intenzív. Ha a sönt műtéti úton csökkentésre kerül, a szisztémás keringésbe kerülő gasztrointesztinális vér mennyisége is csökken, így következetesen az EBZ szint is alacsonyabb lesz, ami az EBZ eredeti, gátló hatásának ellentétét, stimulációt vált ki. Ez lehet a műtéti beavatkozások után jelentkező motorikus rohamok előfordulásának lehetséges oka. (Aronson és mtsai, 1997)
IV. Diagnosztika
Amennyiben a kutyában portoszisztémás sönt jelenlétét feltételezik, több módszert alkalmazhatunk ennek igazolására. PSS-el rendelkező kutya esetén a teljes vérkép, vizelet és epesavak analízise során a következő változások figyelhetőek meg:
- vörösvérsejtek méretének csökkenése
- fehérvérsejtek számának emelkedése
- összfehérje szám, albumin, BUN (blood urea nitrogen) mennyiségének csökkenése
- éhgyomri és etetés utáni epesavak mennyiségének emelkedése
- vérammónia szint emelkedése
- Protein C koncentráció csökkenése
A laborvizsgálatok mellett a PSS kimutatható más módszerekkel is. Hasi röntgenfelvételen a máj általában kisebb, zsugorodott. Ultrahangvizsgálattal is megkereshető a sönt. Szcintigráfia során radioaktív anyagokat juttatnak a vastagbélbe vagy a lépbe és egy speciális kamerával követik ezek keringésbeli útját. Ha az anyagok több, mint 5%-a közvetlenül a szívbe jut, PSS jelenléte feltételezhető. Portogram készítése során kontrasztanyagokat injektálnak a hasűri erekbe, majd röntgenfelvételt készítenek a területről. Ez egy invazív eljárás, azonban jól láthatóan bizonyítja a sönt jelenlétét és helyzetét, és megfelelő eszközök segítségével műtét közben is elvégezhető. CT vizsgálattal az intra- és extrahepatikus sönt is jó eséllyel kimutatható (Tobias, 2003).
V. Kezelés
Extrahepatikus sönt esetén lehetséges a sönt műtéti úton történő okklúziója. Ilyenkor a söntöt a lehető legközelebb zárják le a vena cava-ba történő betorkollásához. Az ameroid konstriktor használata hatékony módja a sönt lezárásának, ami egy acélhüvelybe foglalt kazein gyűrű. A kazein folyadékabszorpciója során megduzzad és lezárja az eret (Tobias, 2003).
VI. Felhasznált irodalom
College of Veterinary Medicine, Tennessee, USA
Salgado M., Cortes Y. (2013): Hepatic Encephalopathy, Etiology, Pathogenesis, and Clinical Signs
Tobias K.M. (2013): Brief Overview of Portosystemic Shunts
(Az ábrák és a táblázat saját készítésűek)