Ide kerül majd a szöveg. Kérem az első sort érintetlenül hagyni!
Az amfetamin és a limbikus rendszer
Az amfetamin az alkaloidok közé tartozó, mesterségesen előállított szerves vegyület. Neve az alfa-metil-feniletilamin nevű vegyület rövidítéséből származik. A farmakológiában az összes hasonló kémiai szerkezetű vegyületet amfetaminszármazéknak nevezzük, melyek közül a legelterjedtebbek: amfetamin (Speed), metamfetamin, és a metiléndioxi-metamfetamin, azaz MDMA (Ecstasy). Funkcionálisan sok tulajdonságában hasonlítanak a kokainnal. Pszichostimulánsok, azaz a szinaptikus idegrendszer izgalmát váltják ki. Emiatt a tulajdonságuk miatt népszerű tudatmódosító szerek: használójuk eufórikus állapotba kerül, sokszor enyhén hallucinácinál is. Számos viselkedésbeli változást idéznek elő, mely azzal magyarázható, hogy hatással vannak az agy egy speciális területére, a limbikus rendszerre.
A limbikus, vagy határkérgi rendszert a hipotalamusszal szoros kapcsolatban álló, az agykéreg és a hipotalamusz által határolt agyterület. Ez a rendszer felelős az érzelmek, viselkedés és ösztönök kontrolljáért, valamint a memória működése is hozzá köthető. Alkotói az amigdala, a hippokampusz, funkcionálisan a gyrus cinguli (neocortex), a septalis area, a septum pellucidum és számos törzsdúc adja. Ezen törzsdúcok egyike a testhelyzetet és mozgást nagyban befolyásoló csíkolt test (corpus striatum). A csíkolt test dorsalis része a farkalt magból (nucleus caudtus) és a putamenből áll. Az agy jutalmazó redszerét alkotó ventrális régiót a nucleus accumbens és a tuberculum olfactorium alkotja. Az amfetamin leginkább a csíkolt testre fejti ki hatásait.
Contents
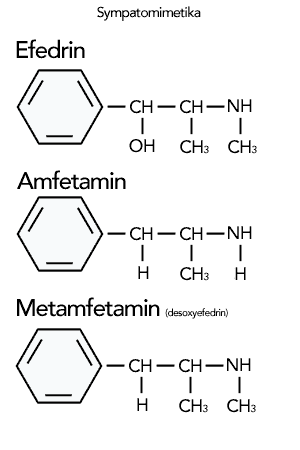
Az amfetamin szerkezete
Szerkezetileg leginkább a természetben is fellelhető efedrinhez, a közöséges csikófark (Ephedra dystachia) által termelt fenil-etilamin származékhoz hasonlít.
|
Az amfetamin általános hatásai
- érszűkítő
- vérnyomásemelő
- hörgőtágító
- étvágycsökkentő
- entaktogén
- fájdalomcsillapító
- eufórikus érzés, hallucinációk kiváltása
Az amfetamin felezési ideje 12 óra. A fenti a jelenségek az aktív szakasz alatt jelentkeznek, intenzitásuk a fogyasztott drog mennyiségétől függ. Miután a szer kiürült a szervezetből, levertség, fáradtság, szomjúság és szénhidrátok utáni vágy jellemző.
Felhasználása
Amfetamin, mint gyógyszer
Az amfetamin fent említett hatásai miatt korábban gyógyászati alapanyagként terjedt el. Narkolepszia, elhízás, figyelemhiányos hiperaktivitás, sőt néha még a részben elégtelen dopaminellátás okozta Parkinson-kór kezelésére is használták.
Amfetamin, mint drog - káros hatások
Manapság leginkább élénkítő hatású kábítószerként kerül forgalomba. Rendszeresen használva addiktív, mivel az amfetamin által nagyban befolyásolt dopamin receptorok mennyisége a növekvő számú inger hatására folyamatosan csökken, ezáltal a korábbi, megszokott mennyiségű pszichoaktív anyag már nem váltja ki a várt hatást, kialakul a függőség. Ez a folyamat a neuroadaptációs mechanizmus (Katona, 2007). Az amfetamin maga például 2-3 hét rendszeres használat után az esetek nagy részében függőséget alakít ki.
Függőség kialakulása esetén, nagy dózisban paranoid-skizofréniát okoz. Rendszeres fogyasztása esetén emellett az agy limbikus rendszere olyan mértékű irreverzibilis károsodást szenved el, hogy az korai Alzheimer-kórra jellemző tüneteket produkál. Kis dózisban felerősíti az egyszerű, általános motoros aktivitást, nagyobb dózisban pedig a fajspecifikus mozgásformák felerősödését eredményezi. (Seiden, Sabol és Ricaurte, 1993) Rusyniak kísérleteiben metamfetamin-függő személyeknél kognitív viselkedési zavarokat és neurológiai abnormalitásokat figyelt meg. (Rudyniak, 2013) A függőség jelentős közegészségügyi probléma, mely a mindennapokra is ható pszichiátriai és neuropatológiás zavarokat okoz. (Henry et al, 2010). Ezért kialakulásának, mechanizmusának pontosabb megismerése érdekében folyamatos kutatások folynak.
Manapság leginkább élénkítő hatású kábítószerként kerül forgalomba. Rendszeresen használva addiktív anyag. Függőség kialakulása esetén, nagy dózisban paranoid-skizofréniát okoz. Rendszeres fogyasztása esetén emellett az agy limbikus rendszere olyan mértékű irreverzibilis károsodást szenved el, hogy az korai Alzheimer-kórra jellemző tüneteket produkál.Kis dózisban felerősíti az egyszerű, általános motoros aktivitást, nagyobb dózisban pedig a fajspecifikus mozgásformák felerősödését eredményezi. (Seiden, Sabol és Ricaurte, 1993) Rusyniak kísérleteiben metamfetamin-függő személyeknél kognitív viselkedési zavarokat és neurológiai abnormalitásokat figyelt meg. (Rusyniak, 2013) A függőség jelentős közegészségügyi probléma, mely a mindennapokra is ható pszichiátriai és neuropatológiás zavarokat okoz. (Henry et al, 2010). Ezért kialakulásának, mechanizmusának pontosabb megismerése érdekében folyamatos kutatások folynak.
Hatásmechanizmus - biokémiai vonatkozások
A pszichostimuláns vegyületek hatásmechanizmusa azon alapul, hogy szerkezetük hasonlít a központi idegrendszer serkentő neurotranszmittereire, a katekolaminokra (dopamin, adrenalin, noradrenalin) vagy az indolvázas szerotoninra (Újváry, 2000). Ezek a kemikáliák a pre- és posztszinaptikus membránreceptorokon keresztül teremtenek kapcsolatot a szinapszisokban. Az amfetamin-vegyületcsalád tagjai ezen molekuláris kommunikáció normális működését befolyásolják, mivel adrenerg, szerotoninerg és dopaminerg hatással rendelkeznek. Magasabb amfetamin adag a a katekolaminok és a serotonin kibocsátását is fokozza, míg az alacsonyabb dózis főleg csak a katekolaminokét. (Leyton et al. 2002) Ezzel toxikus vagy pszichoaktív hatást fejtenek ki. Az amfetamin stimulálta dopaminkibocsátás önmagában jelentéktelenebb mértékben okoz hangulatjavulást és nem is túl erősen stimuláló hatású. Ezekért a hatásokért az ilyen esetekben felszabaduló noradrenalinnak és szerotoninnak is nagyon fontos szerepe van.
Hatásmechanizmus - élettani vonatkozások
A szájon át beadott amfetamin hatása jelentéktelenebb és jobban körülírható, mint az intravénásé (ugyanolyan mennyiségben). (Leyton et al. 2002)
A dopaminkibocsátás serkentése
Egy 1988-ban végzett kísérletben agydialízissel vizsgálták, milyen változást okoz szabad mozgásban nem gátolt patkányok agyában, ha emberek által használt drogokat fogyasztanak.(Di Chiara és Imperato, 1988.) Az opiátok, az alkohol, a nikotin, az amfetamin és a kokain a nucleus accumbensben különösen emelték az ectracelluláris dopamin koncentrációt és hipermotilitást okoztak. Ezzel szemben azok a drogok, melyeket az emberek nem használnak tudatmódosító szerként, nem váltottak ki szinaptikus dopaminkoncentráció-növekedést. (atropin, imipramin-antidepresszáns, difenilhidramin-antihsiztamin). Ebből arra következtettek, hogy a függőséget okozó drogok közös tulajdonsága a dopaminkoncentráció-emelkedést kiváltó hatásuk. Az amfetamin és a kokain elvonják elősegíti dopamin (illetve kisebb mértékben a noradrenalin és a szerotonin) fokozott kiáramlását, gátolja a neurotranszmitterek lebontását végző MAO (monoamino-oxidáz) enzimrendszert és a reuptake-et a preszinaptikus membránon keresztül a nucleus accumbensben (Kreek, La Forge és Butelman, 2002.), az opiátok, a nikotin és az etanol pedig serkenti a dopaminerg receptorok működését.
Az amfetamin hatásmechanizmusának egy másik kulcslépése az, hogy csökkenti a raclopride (a D2 dopamin receptorok szelektív antagonistája) kötési potenciálját (a rendelkezásre álló neuroreceptorok számától és a ligand-receptor kötés affinitásától függő változó) a ventrális corpus striatumban. Ez fokozza a drog újbóli fogyasztásának vágyát és egyéni hajlamtól függően az újdonság erős keresését váltja ki a felhasználóból. Ezen jelenségek az amfetamin által kiváltott dopamin kibocsátásnak köszenhetők. Ennek az extracelluláris dopamin többletnek a viselkedési hatása azonban még vitatott, csupán az agy jutalmazási rendszerével való összefüggés tisztázott. Az ilyenkor jelentkező eufórikus érzésről sem tudni, hogy a dopamin többlet hatása-e, vagy a drogé, magáé.
Friss kutatások szerint a mezolimbikus dopamin transzmisszió közelebbi kapcsolatban lehet a a vágyakozás keltéséhez, mint magához az eufória megteremtéséhez, vagyis a dopamin inkább a motivációs állapotokat szabályozza.
A csíkolt test régióinak jellegzetességei
A dorsalis és ventralis corpus striatum neuroanatómiai összeköttetései tisztázottak. Főemlősökben a corpus striatum ventralis része dopaminlöketeit leginkább a középagy tegmentumának dorsális részéből, bementi információit (input) pedig a limbikus struktúráktól, az amygdalától, a középső és orbitofrontális kéregtől és az elülső cortex stingularis-tól kapja. Ezek a rendszerek fontos szerepet játszanak a jutalmazásban, az effektíven fontos hatások megfigyelésében és a jutalomra és büntetésre való reagálásban. (Ezzel szemben a dorsalis corpus striatumra ható dopaminlöketek a középagy alsó részéből származnak.)
Állatkísérletek már bebizonyították a ventrális csíkolt test dopaminra való reakciója alapoz meg néhány bizonyos erősen motivált viselkedésformát, azonban ahhoz, hogy ezen folyamatok érzelmekre gyakorolt hatását is megértsük, emberi példákat is vizsgálnunk kell. Ez pozitronemmissziós tomográfia segítségével történhet meg, ami egy olyan funkcionális, vagyis nem anatómiai, képalkotó eljárás, amely háromdimenziós képet ad a test egy adott területéről. Ezen módszerrel bizonyos szövetek élettani jellemzői is vizsgálhatóvá válnak egy adott pillanatban. Az amfetamin okozta, eufóriával járó endogén dopamin koncentráció változás mértéke eltérőnek bizonyult a különböző csíkolt test régiókban, a ventrálisban erősebb. Ezen rész dopamin kibocsátásának mértéke pozitív összefüggésben van az amfetaminra adott hedonista érzettel. (Drevets et al. 2001)
A pszichostimuláns drogok okozta dopaminkibocsátás a csíkolt test ventrális részén belül is a nucleus ccumbensben a legjelentősebb. (Carboni et al. 1989)
Nucleus accumbens
A csíkolt test ventralis részenek egyik alkotója, a nucleus accumbens egy kérgi és egy magi régióval rendelkezik. Bár az amfetaminos kezelés mindkét régióra hatással van, az más-más eredményt okoz.
Ha egy élőlény sokáig nem volt kitéve valamilyen hatásnak, előfordulhat, hogy nincs is rákényszerítve, hogy feltétlenül megtanulja kezelni azt, így egy ideig látens gátlás alakul ki erre a stimulusra nézve, ami késleltetett kondícionálódást eredményez. Ez a jelenség akut skizofréniás betegeknél nem jelentkezik. Állatkísérletek által bizonyított, hogy a mezolimbikus dopamin rendszer szerepet kap ebben a folyamatban, sőt a nucleus accumbens magi és kérgi régiói kissé eltérő funkciókkal rendelkeznek. Patkányok nucleus accumbensének magi régióját károsítva a látens gátlás akadálytalanul működik tovább, a kérgi régió sérülése viszont ezen folyamat kiesését okozza. A sérült kérgű, de ép maggal rendelkező állatok ezen kívül nagyobb motoros aktivitást mutattak amfetamin kezelés után, mint az érintetlen agyú kontrolcsoport tagjai. (Weiner et al. 1996) Így feltételezhető, hogy a magi és a kérgi régió egymásra valamilyen szabályozó hatással lehet.
Egy 1988-ban végzett kísérletben agydialízissel vizsgálták, milyen változást okoz szabad mozgásban nem gátolt patkányok agyában, ha emberek által használt drogokat fogyasztanak.(Di Chiara és Imperato, 1988.) Az opiátok, az alkohol, a nikotin, az amfetamin és a kokain a nucleus accumbensben különösen emelték az ectracelluláris dopamin koncentrációt és hipermotilitást okoztak. Ezzel szemben azok a drogok, melyeket az emberek nem használnak tudatmódosító szerként, nem váltottak ki szinaptikus dopaminkoncentráció-növekedést. (atropin, imipramin-antidepresszáns, difenilhidramin-antihsiztamin). Ebből arra következtettek, hogy a függőséget okozó drogok közös tulajdonsága a dopaminkoncentráció-emelkedést kiváltó hatásuk. Az amfetamin és a nikotin a elvonják a dopamint a szinapszis preszinaptikus oldaláról és gátolják az újrafelvételt, az opiátok, a nikotin és az etanol pedig serkenti a dopaminerg receptorok működését. Az ennek következtében fellépő kellemes örömérzet az oka annak, hogy emberek és állatok esetében idővel egyaránt nő az amfetamin-felvétel gyakorisága. (Cadet et al, 2013).
A nucleus accumbens és a glutamát
A pszichostimulánsoknak leginkább a nucleus accumbens dopamin neurotanszmissziójára hatva módosítják a viselkedést. Bizonyos kutatások azonban azt bizonyítják, hogy ezek neurológiai és a viselkedésbeli hatások megelőzhetők a serkentő aminosav receptorok antagonistáinak alkalmazásával, így a folyamatban szerepe lehet a leáltalánosabb serkentő neurotranszmitternek, a glutamátnak is. Eszerint a pszichostimulánsok alkalmazása megváltoztathatja a nucleus accumbens dopaminrendszerének glutamátra adott válaszkészségét. A kísérleti patkányok ventrális tegmentális régiójának glutamátra adott válasza jelentősen felerősödött amfetaminos kezelés után, míg ezzel ellentétben a nucleus accumbensük neuronjai amfetamin beadása után szignifikánsan kevésbé lettek érzékenyek a glutamát serkentő hatására. Így a viselkedés megváltoztatásában a glutamát receptorok megváltozott transzmissziójával is összefüggésben van a dopamin jelátviteli útjában. (White et al. 1995)
Epigenetikai és transzkripciós változások
Az amfetamin bizonyítottan károsítja az idegrendszert, hosszabb távú használata a limbikus rendszer károsodásához vezet, ugyanis sejtszintű elváltozásokat okoz. A szer okozta agyi és viselkedésbeli változások sokkal jelentősebbek a kezdeti neurofarmakológiai hatásoknál. A pszichostimulánsok ugyanis több kísérlet által bizonyítottan biokémiai adaptációt okoznak az agyi monoaminnal működő jelátviteli pályáknál, főleg a dopamin esetében. Patkányokon végzett kíséretek alapján kiderült, hogy ezen drogok hosszú távú használat esetén azért is viselkedésmódosító hatásúak, mert képesek a szinaptikus kapcsolatokat átrendezni a nucleus accumbensben és a prefrontális kéregben. Ha a patkányokat mozgási lehetőség nélkül hosszan kezelték pszichostimulánsokkal a nucleus accumbens egy speciális sejtjének a medium spiny neuronnak a dendrit-ág és a dendrit-tüske-, illetve a prefrontális kéreg V-piramidális sejtjeinek apikális-dendrittüske száma megnőtt. (Robinson és Kolb, 2008)
Az amfetamin ezen kívül befolyásolja a gének expresszióját és a fehérjék transzkripciójának intenzitását. (Cadet et al, 2013)
Korai elváltozások
Patkányok szabadon adagolhattak maguknak amfetamint nyolc napon át, napi 15 órában, majd két órával az utolsó adagolás után elaltatták őket. Kvantitatív PCR-rel vizsgálták a génexpressziót a nucleus accumbensben és a corpus striatumban, ahol összesen 543 transzkripcióban történt változás. (xy ábra) Azon gének expressziója, melyek részt vesznek a transzkripció szabályozásában, a sejt-sejt interakcióban, az idegrendszer működésében, és neurológiai betegségek génhálózatában, fokozódott (356 gén).