A hosszútávú alvásmegvonás élettani hatása
Témavezető: Jócsák Gergely
Készítették:
Városi Dominika
Makk Tímea
Klenovszki Dóra
Contents
Az alvás definíciója
Az alvást úgy lehetne definiálni mint eszméletlenség, amiből az egyed különböző ingerek hatására felébreszthető. Fontos különbség a kóma és az alvás között, hogy előbbi állapotban lévő egyedet vagy személyt nem lehet felébreszteni. (Guyton és Hall, 2006) Az alvás mindig jellegzetes testhelyzet felvételével jár, az állat bizonyos fokig mozdulatlan marad, és érzékszervi ingerelhetősége megváltozik. Ezt a három jellegzetességet nevezhetjük akár az alvás "kritériumainak" is. (Goldschmidt és Halász, 1983)
Az alvás szerepe
Az alábbi szerepek csupán feltételezések; az alvás élettani funkciója még mindig tisztázatlan és vizsgálatok tárgyát képezi.
Az alvás funkciója lehet pihenés: mint inaktivitás. A vázizmok mozgása jelentősen lecsökken, de nem állíthatjuk, hogy meg is szűnik, mivel a testhelyzet változhat. A pihenő funkciót továbbá bizonyítja az is, hogy alvás során a katabolikus (lebontó) folyamatok helyett az anabolikus (felépítő) folyamatok kerülnek előtérbe.
Energiamegtakarítás: alvás közben az energiafelhasználás csökken. Fontosságát mutatja, hogy sok élőlénynél felfedezhetők alvási periódusok, pedig alvás közben a prédaállat nem tud elmenekülni a ragadozó elől. Ha tehát nem lenne az alvásnak kulcsfontosságú szerepe a szervezet normál működésének fenntartásában, az élőlények nem aludnának.
Az alvás további szerepe az újjáépülés. A növekedési hormon (growth hormone, GH) szintje elalvás után 3-5 órával a legmagasabb, elérheti a nappali érték 200-szorosát is. Ennek a hormonnak nagy az anabolikus aktivitása; fokozza az aminosavak sejtekbe jutását, a fehérjeszintézist, és a glükoneogenezist. (Bódizs, 2000)
Az alvás szakaszai
Az alvásnak két szakasza különíthető el, amik egymást váltogatva jelentkeznek. (Guyton és Hall, 2006)
1. Lassú hullámú alvás szakasz: más szóval a mélyalvás szakasza, az alvás első órájában jelentkezik. Csökken a perifériás erek tónusa, a vérnyomás, a respirációs ráta, és a metabolikus aktivitás.
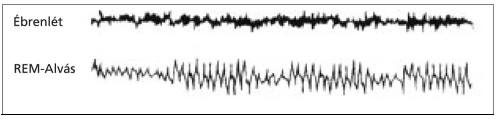
2. Rapid Eye Movement (REM) szakasz: az alvás 25%-át teszi ki, átlagosan 90 percenként jelentkezik, és 5-30 percig tart. Az alvásnak ezt a szakaszát lehet összefüggésbe hozni az álmodással. A pulzus és a légvételek rendszertelenné válnak. Jellegzetes agyi aktivitás mérhető, azonban a REM szakasz agyhullámai különböznek az ébrenlét során detektálhatóktól. (1. ábra)
|
Egyes állattörzsek alvási sajátosságai
Lábasfejűeknél, ízeltlábúaknál megfigyelhetőek alvási időszakok; az éjjeli és nappali lepkék elkülönítése például ez alapján történik.
A halak, a kétéltűek, és a hüllők törzsében jellegzetes testhelyzetekben történő időszakos mozdulatlanságot írtak le, ugyanakkor az EEG- görbén nem láthatók az alvásra jellemző hullámok; a szakaszok nem elkülöníthetők.
Evolúciósan először a madaraknál, majd az emlősöknél jelenik meg az állandó testhőmérséklet, így általánosságban több energiára van szükségük, anyagcseréjük fokozott. Ebből egyértelműen következik, hogy alvásigényük is nagyobb. Alvási szakaszaik könnyen elkülöníthetők az EEG-n. (Goldschmidt és Halász, 1983)
Az alváshiány
Az alváshiányt más szóval insomniának nevezzük. Leginkább a lassú hullámú alvási szakasz kiesése vezethet negatív következményekhez.
Okok
Insomnia adódhat fizikai fájdalomból; ilyenkor általában a lefekvésre való képtelenség vezet a kialvatlansághoz. Ezt okozhatja ízületi, vagy épp hasűri fájdalom. Az Egyesült Államokban leírtak egy esetet, ahol egy lónak a vastagbelében található két hatalmas bélkő következtében a bele hozzá volt tapadva a rekeszizomhoz. Ez a rendellenesség lefekvéskor iszonyú fájdalmat okozott volna, ezért az állat inkább egész nap állt, míg végül alváshiány alakult ki. (Justin és Kovács, 2016)
Nagy mennyiségű stresszor jelenléte is okozhatja az alváshiányt. Ilyen stresszor lehet a hangos zaj, a nem megfelelő hőmérséklet, és a hirtelen környezetváltozás (például ha egy ménesben tartott lovat külön karámba raknak egyedül, vagy ha egy családi kutya menhelyre kerül). (Goldschmidt és Halász, 1983)
Jóllakáskor a gastrointestinális traktusból hipnogén hormonok szabadulnak fel: kolecisztokinin, inzulin, delta-alvást induláló peptid; feltehetőleg ezek okozzák az evés utáni álmosságot. Az emésztőrendszer megbetegedése, vagy épp éhezés folytán tehát alvászavar és nyugtalanság léphet fel. A máj és a vese megbetegedésénél ugyancsak megfigyelhetőek ezek a tünetek. (Bódizs, 2000; Landsberg, 2014)
Kutatások bizonyították, hogy az agy bizonyos területeit stimulálva természetes alváshoz hasonló állapotot lehet indukálni. Ilyen területek a raphe magvak a híd és a nyúltvelő környékén (az innen felszálló rostok kapcsolatba lépnek a thalamusszal, a hypothalamusszal és a limbikus rendszerrel is), a nucleus tractus solitarii, és a hypothalamus rostralis része. Az agy ezen részei alvást elősegítő faktorokat termelnek (muramyl-peptid, serotonin), így ezeknek a területeknek a sérülése intenzív ébrenléttel jár. (Guyton és Hall, 2006)
Öregedő kutyáknál megfigyelhető a kognitív funkciók hanyatlása; náluk normális, ha kevesebbet alszanak éjszaka és megváltozik az alvás-ébrenlét ciklusuk, tehát az időskori insomnia nem kóros. (Landsberg, 2014)
Következmények
Az alváshiány sok szempontból hatással van az egészségre. A káros egészségügyi hatások még mindig alulértékeltek és alábecsültek a klinikai gyakorlatban, főleg a humán egészségügyben. Az alvásnak fontos hatása van a test minden szervére, ezért az alváshiány helyrehozhatatlan károkat okoz (Lima, 2014). Az alvás egy helyreállító folyamat, ami megteremti az egyensúlyt a pszichés és fizikai egészség között. Hiánya összefüggésbe hozható az elhízással, kettes típusú diabetes-el, hypertensio-val és különböző cardiovascularis betegségekkel. A központi idegrendszerre is hatással van az insomnia: ingerlékenységhez, súlyosabb esetekben viselkedési zavarokhoz, akár pszichózishoz is vezethet. Ez alapján feltételezhető, hogy az alvásnak az egyik legfontosabb szerepe a normál agyműködés visszaállítása, valamint a központi idegrendszer egyes funkcióinak kiegyensúlyozása. (Guyton és Hall, 2006) Az alvásidő csökkenése és az alvás minőségének romlása egyre elterjedtebb a modern társadalomban. Mind a rövidtávú, mind a hosszútávú alvásmegvonás megemelkedett mortalitási kockázattal jár.
Hatása az urinális anyagcserére
Annak megértése, hogy a metabolit szintek hogyan változnak 24 óra alatt, döntő fontosságú a klinikai vizsgálatok során. Továbbá a kapcsolat az alváshiány és a metabolikus rendellenességek között, mint például a cukorbetegség és az elhízás folyamatos kutatásokat igényel a pontosabb kezelések miatt. (Davies és mtsai, 2015)
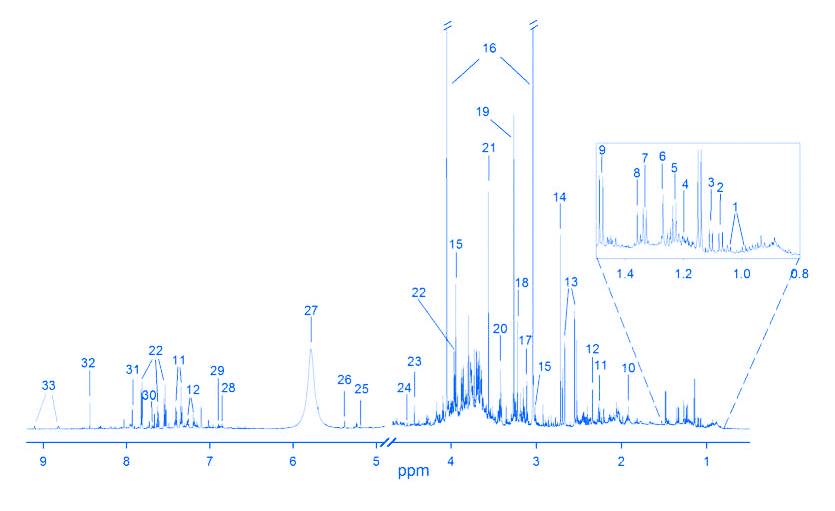
Emberek között végzett kutatások szerint (erősen szabályozott környezet, vizelet gyűjtés 8 órás intervallumonként, vizsgálva NMR spektroszkópiával [2. Ábra]) 32 azonosított metabolit közül 32 mutatott ritmikusságot az első 24 órás alvásmegvonás után, a második napon pedig mindössze 5.
Nyolc metabolitnak jelentősen megnövekedett a szintje alvásmegvonás alatt (taurin, formiát, citrát, 3-indoxil-szulfát, karnitin, 3-hidroxiizobutirát, TMAO és acetát), nyolc pedig szignifikánsan csökkent (dimetil-amin, 4-DTA, kreatinin, aszkorbát, 2-hidroxiizobutirát , allantoin, 4-DEA, 4-hidroxi-fenilacetát). Ezek az adatok azt jelzik, hogy a mintavételi idő, az alvás jelenléte vagy hiánya, és az alvásmegvonás válasza ezekre, rendkívül fontosak a vizelet metabolikus biomarkereinek monitorozására, azonosítására. (Giskeodegard és mtsai, 2015)
|
Anyai alváshiány hatása
Az alváshiány vemhesség alatt is komoly problémát jelent, mert egyaránt hatással van az anyára és az újszülöttekre is. Egyre több bizonyíték mutatja, hogy az alvásmegvonás fizikális, hormonális, emocionális, és neurológiai problémákat okoz. Például csökkent neurogenesis-t, csökkent hippocampus-függő térbeli tanulást, memória zavarokat, továbbá a hím utódok szexuális viselkedésének redukálódását.
Egy friss tanulmány szerint (Peng és mtsai, 2016) az alvásmegvonás hatásai összefüggnek a vemhesség előrehaladottságával. A kísérletben (3.Ábra) vemhes patkányokat vizsgáltak az első, második, és harmadik trimeszterben. Az utódok emocionális és kognitív funkcióit tesztelték a posztnatális napokban (42-56 nap). A patkányokban szorongásos-depresszív viselkedést, illetve csökkent memóriát, tanulási készséget figyeltek meg. Kimutatható volt az is, hogy az anya-állatban szignifikánsan redukálódott a hippocampalis-neurogenesis a kontrollhoz képest.
|
Hatás a belső szervekre
Az alvásmegvonás bizonyítottan enyhe szervi károsodásokat indukál. Egy korábbi tanulmányban (Liu és mtsai, 2015) a hím egerekre gyakorolt hatásokat vizsgálták 0-72 órás alvásmegvonásban különböző módosított kísérleti platformokon.
Az állatokból tüdő, vese, szív, hasnyálmirigy és vérmintákat gyűjtöttek különböző periódusokban, amiket biokémiai és hisztológiai módszerekkel vizsgáltak.
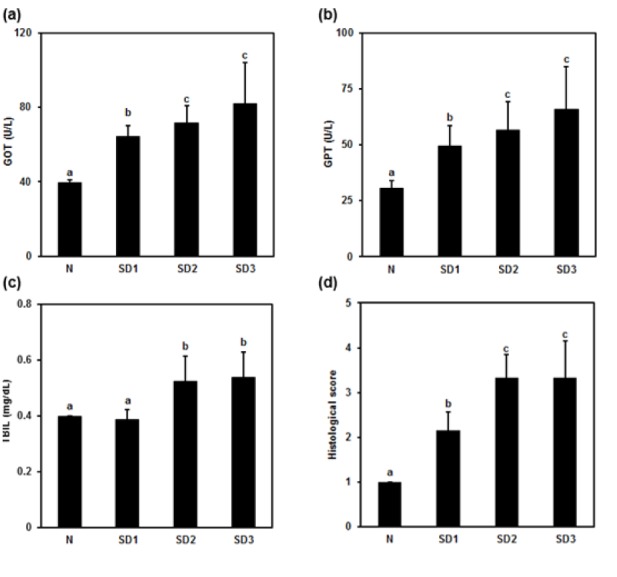
A kísérletben glutamát-oxálacetát-transzamináz (GOT), glutamát-piruvát-transzamináz (GPT), teljes billirubin (TBIL), kreatin-foszfokináz (CPK), laktát-dehidrogenáz (LDH), kreatini, nitrogén-monoxid (NO), tumor nekrózis faktor (TNF) és interleukin (IL) szintet mértek. Szövettanilag kiderült, hogy a vizsgált egerekben enyhe-középsúlyos máj-és tüdőkárosodás mutatkozott. (Srinivasan és mtsai, 2015)
|
Az alvástól megvont egerekben szignifikánsan megemelkedett a GOT, GPT, TBIL, LDH szint (4. Ábra), amik a károsodásokat indukálták.
A vizsgálat eredménye azt mutatja, hogy az alváshiány emberekben is több szervi károsodást okozhat, ami negatívan befolyásolja a szív-és érrendszer egészségét.
Hatás az immunrendszerre
Extracelluláris stimulus hatására az immunrendszer egy komplex jelátviteli kaszkádon megy keresztül. Feltételezések szerint fontos szerepe van a megfelelő mennyiségű alvásnak az immunrendszer helyreállításában. Számos tanulmány kimutatta, hogy kapcsolat áll fenn a szervezet védekező mechanizmusának romlása és az alváshiány közt, beleértve a fokozott hajlamosságot a patogén fertőzésekre. (Lisandro Lungato és mtsai, 2012)
Kétirányú kommunikáció van az agy és az immunrendszer közt. A hypotalamo-hypofizeális tengely, az autonóm idegrendszer, és az agy közvetlen makromolekula ürítése a keringésbe, egy olyan hálózatot alakít ki, amely által az alvó/ébren lévő agy képes a testi funkciókat befolyásolni. Hasonlóképpen, a citokin szintváltozások modulálják a központi idegrendszert akár közvetlenül, vagy a vagus ideg útján, így befolyásolva az alvó/ébren lévő agyat. Ez a két befolyásoló rendszer szerves részét képezi a homeosztázisnak. A rendezetlen alvási ciklus ezt a jól összehangolt rendszert zavarja meg. (Jodi B. Dickstein, Harvey Moldofsky, 2004)
Egy korábbi tanulmány (Rechtschaffen és mtsai, 1983) kimutatta, hogy patkányok esetén elhúzódó alváshiány (~30nap) halált okozott, konkrét okok nélkül. Egy későbbi tanulmányban (Everson, 1993) a korábbi kísérletet megismételve felfedezték, hogy opportunista baktériumok jelentek meg a patkányok vérében. Láz, vagy más akut fázis reakció nem mutatkozott a bakteraemia során. Újabb kutatások azt mutatták, hogy az alvásmegvonás mikrobák felhalmozódásához vezetett a hasűri nyirokcsomókban. Ezek az eredmények összhangban vannak azokkal az elméletekkel, melyek szerint az alvásmegvonás immunszuppresszióhoz vezet. Azonban kísérletekkel demonstrálták, hogy hasonló körülmények között a tumor sejtek lassabban osztódtak, illetve a tumorok mérete nagyobb ütemben csökkent. (Jodi B. Dickstein, Harvey Moldofsky, 2004)
Hatás a lépsejtekre
A kálcium (Ca2+) egy univerzális második hírvivő molekula az eukariótákban, amely számos sejttani folyamatot szabályoz. Emlősökben a sejtek Ca2+raktára az endoplazmatikus retikulum (ER). Az ER mellett a mitokondrium és a Golgi-apparátus is részt vesz a sejten belüli (intracelluláris) Ca2+szint szabályozásában. A Ca2+-szint változása elengedhetetlen az immunsejtek aktivitásához, szerepet játszik a citokin exocitózisban, az antigén prezentáló sejtek interakcióiban és a T-sejtek génexpressziójában. (Lisandro Lungato és mtsai, 2012)
SD hatására a lép sejtjeiben (splenocyták) kimutatták, hogy az intracelluláris Ca2+-szint erőteljesen csökken, főleg az endoplazmatikus retikulum (ER) kalcium raktárában. Ezek az eredmények arra utalnak, hogy SD hatására az endoplazmatikus retikulum károsodása által romlik a Ca2+ jelátvitel. (Lisandro Lungato és mtsai, 2012)
Megfigyelték, hogy az alváshiányban szenvedő állatokban, a vér monocyta száma a lépben csökkent szignifikánsan. A vizsgálatban lévő alvástól megvont egereknél patogénnel indukált vérmérgezést okozva a bakteriális terhelés a lépben jelentősen magasabb volt három nappal a fertőzést követően. Ezek az egerek csekélyebb eséllyel élték túl a fertőzést a kontroll csoporthoz képest. (J. Hahn és mtsai, 2015)
Hatás a makrofágok nitrogén-monoxid(NO) termelésére
Az immunrendszer sok sejtjében mutatható ki nitrogén-monoxid- szintézis. Elsősorban a citokinek által aktivált makrofágok termelnek és juttatnak a keringésbe nagy koncentrációban nitrogén-monoxidot, s ennek az immunválaszt kiváltó tumor sejtek, baktériumok stb. elpusztítása a célja. A nitrogén-monoxid azáltal fejt ki citotoxikus hatást, hogy a célsejtek enzimjeit nitrozilthiol-komplexekké alakítja, ezáltal bénítva működésüket.
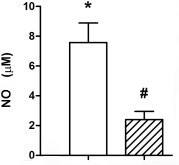
A makrofágok aktivitását vizsgálva arra jutottak, hogy az alvástól megvont egerekben jelentősen alacsonyabb mennyiségű NO keletkezett a makrofágokban annak ellenére, hogy indukálták azok NO termelését. A csökkent NO termelés redukálja a makrofágok fertőzés és daganat ellenes aktivitását, ezáltal fokozva ezek kockázatát. (Anderson Sá-Nunes és mtsai, 2015)
|
Hatás a humorális immunválaszra
Immunglobulin (Ig) szint és komplement rendszer aktivitás a vérszérumban elengedhetetlen az immunrendszer megfelelő működéséhez és segítenek megérteni, hogy alvás és ébrenlét alatt hogyan működnek a károsodásokat helyreállító folyamatok a szervezetben, illetve hogy az alváshiány milyen következményekhez vezet.
Az influenza elleni immunitást célzó vizsgálatok (Renegar és mtsai, 1998) SD esetén egerekben kimutatták, hogy az SD nem okozta szignifikánsan a szérumban lévő influenza specifikus IgG antitestek szintjének csökkenését, sőt azt találták, hogy a kontroll egerekhez képest magasabb volt az IgG szint. Sebgyógyulási vizsgálatokkal is ugyanerre az eredményre jutottak a sebkörnyéki területen mért IgG szint alapján.
Minden immunglobulin és komplement paraméter szint emelkedése mutatkozott normál határokon belül, kivéve az IgG-t ami egy kissé magasabb volt ennél. Emögött a citokin felszabadulás állhat (IL-2, IL-6). Ezek alapján látható, hogy az alvás-ébrenlét aktivitás fontos szerepet játszik a humorális immunitásban. Feltételezhető, hogy az ébrenlét szükséges az immunrendszer megfelelő működéséhez, míg a hosszú távú alvás kóros folyamatnak tekinthető az immunrendszer működésében. (Liu Hui és mtsai. 2006)
Hatások a cardiovascularis rendszerre
|
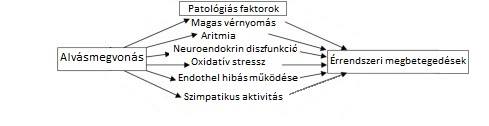
Az alváshiány az érrendszeri megbetegedésekhez patológiás faktorok megjelenésével, mint például a magas vérnyomás, aritmia, endothel hibás működése, neuroendokrin diszfunkció, szimpatikus aktiválás, oxidatív stressz járul hozzá (6.Ábra).
Hosszú távú vizsgálatok arra utaltak, hogy az SD szorosan összefügg a szívinfarktus és a szívelégtelenség növekvő morbiditási és mortalitási rátájával. Az alvás időtartama és a szívkoszorúér- megbetegedés (coronary heart disease, CHD) negatívan korrelálnak, rövid alvásidő fokozott CHD kockázattal jár. Bár a legfőbb kockázati tényezők a koleszterin, a dohányzás, és a cukorbetegség, az SD ugyanazon patológiás tényezőket váltja ki, így ennek is nagy szerepe van ebben. (Jie Wang és mtsai, 2015)
Magas vérnyomás
A vérnyomás számos fiziológiai folyamat által szabályozott. A vese folyadék filtrációja és reabszorpciója befolyásolja a vér mennyiségét, ami hormonális szabályozás alatt áll, melyben a renin-angiotenzin rendszer a legfontosabb. A szív kontraktilitása, a perctérfogat és a perifériás ellenállás is nagyon fontos tényezője a vérnyomásnak. Ezek az autonóm idegrendszer hatása alatt állnak a baroreceptorok által kiváltott baroreflexekkel. Baroreceptorok megtalálhatók a szívben, az aortaívben és a nyaki ütőér (a. carotis communis) kettéágazódásánál létrejövő kiöblösödésben (sinus caroticus). Ezek a receptorok érzékelik a vérnyomás megváltozását és információt küldenek az agyban lévő nyúltvelői centrumba, így a vérnyomás normalizálásában van szerepük.
Tartós alvásmegvonás következtében növekedés tapasztalható a szisztolés és diasztolés vérnyomás emelkedésében egyaránt. A hyperextenzióhoz társul a fokozott CHD kockázat, a koszorúerek utóterhelésének növelésével súlyosbodhat a szív vérellátásának csökkenése (szív-ischaemia), ami szövetelhaláshoz és funkcióvesztéshez vezethet. (Janet M. Mullington és mtsai, 2008, Jie Wang és mtsai, 2015)
Neuroendokrin diszfunkció
Neuroendokrin diszfunkció okozta SD hormonszekréciós rendellenességeken keresztül hathat a CHD-ra. Megváltozhat például a melatonin ritmus, renin-angiotenzin rendszer aktivációja, kortizol, katecholamin, és különböző metabolitok szintje, ami rontja a baroreceptorok funkcióját. (Janet M. Mullington és mtsai, 2008, Jie Wang és mtsai, 2015)
Endothel hibás működése
Az endothel (endothelium) egyrétegű laphám, mely az erek legbelső, a testfolyadékkal közvetlenül érintkező részét alkotja. Az endothelnek fontos lokális szabályozó funkciója van, melyet humorális faktorok termelésével végez. Az általa termelt NO felelős az erek tágasságának növeléséért (dilatatio) és a vér thrombocytáinak aggregációjának gátlásáért. Ezek következtében fiziológiás hatása az értágítás által létrejövő vérnyomás-csökkenés. SD hatására a NO biológiai hozzáférhetősége csökken azáltal, hogy csökken az előállításához szükséges NO-szintáz enzim, kofaktor, vagy szubsztrát mennyisége. NO hiányában csökken az endothelfunkció, az endothel által termelt vérér összehúzó faktor, az endothelin aránya nő, szimpatikus működés növekedésével egyetemben. Az endothel sérülése ebben az esetben érösszehúzódást vált ki, csökkenti a helyi véráramlást, növeli a neutrofil granulocyta és adhéziós molekulák szintjét, ami vérlemezke-aggregációt és a trombus képződést okoz. (Janet M. Mullington és mtsai, 2008, Jie Wang és mtsai, 2015, Michelle Kohansieh és Amgad N. Makaryus, 2015)
Oxidatív stressz
Az alvásmegvonás oxidatív stresszel is jár együtt. Oxidatív stresszről beszélünk, ha a szabadgyökök és az antioxidánsok nincsenek egyensúlyban. A Szabadgyökök (Reactive Oxygen Species - ROS) mint az oxigén (O2) gyorsan reagálnak más anyagokkal és inaktiválják a NO-t. Így ha az erek oxidatív stressznek vannak kitéve, csökkenhet a NO biológiai elérhetősége. Normális élettani körülmények között ezt a stresszt csökkentik az endogén antioxidánsok, így téve lehetővé hogy a szervezet fenntarthassa a megfelelő NO szintjét. (Janet M. Mullington és mtsai, 2008, Jie Wang és mtsai, 2015)
Az oxidatív stressz tulajdonképpen egy egyensúlyhiány a reaktív nitrogén és oxigén vegyületek keletkezése és eliminálása között. Kapcsolatba hozható a különböző immunhiányos betegségekkel, rákkal, valamint a szív- és érrendszeri problémákkal is. Továbbá szerepe van az öregedésben, az érelmeszesedésben, valamint a neurodegeneratív betegségek kialakulásában is. (Turrens, 2003 [49])
Ébrenlét alatt folyamatosan keletkeznek szabad gyökök, köszönhetően a fokozott metabolikus aktivitásnak.
Szimpatikus aktiváció
Pulzusszám variabilitás megfigyelése rámutatott, hogy a szimpatikus szabályozás túlsúlyban van (a paraszimpatikus pedig csökkentett aktivitásban van) alvásmegvonáskor, ez pedig a szív elektromos aktivitásának instabilitásához, trombózishoz és érelmeszesedéshez vezethet. (Jie Wang és mtsai, 2015, Michelle Kohansieh és Amgad N. Makaryus, 2015)
Szívritmuszavar
Számos tanulmánnyal alátámasztották, hogy az SD növelheti a szívritmuszavar előfordulását a biológiai ritmus megváltozásával, vagy fizikai stressz következményében. A korai kamrai összehúzódások látenciaidejét is meghosszabbíthatja, ami kamrai tahycardiához vezet, azaz gyakoribb összehúzódást eredményez. (Jie Wang és mtsai, 2015)
Összegzés
A hosszútávú alvásmegvonás élettanban betöltött szerepe kulcsfontosságú. Az alvás alapvető szerepet játszik az egyed mentális, érzelmi és fiziológiai jólétében. Kutatások bizonyítják, hogy hatásai széleskörűen kiterjednek a szervezet biokémiai folyamataira és összességében elmondható, hogy ezeket kivétel nélkül negatívan befolyásolják. A klinikai gyakorlatban egyre inkább fontosabbá válik ezen hatások megismerése, ezért az alvásmegvonás hatásai máig kutatás tárgyát képezik.
Irodalomjegyzék
Yan P., Wei W., Tao T., Dong Z. (2016): Maternal sleep deprivation at different stages of pregnancy impairs the emotional and cognitive functions, and suppresses hippocampal long-term potentiation in the offspring rats. Molecular Brain (2016), 9:17, DOI:10.1186/s13041-016-0197-3
Giskeodegard F. G., Davies K. S., Revell L. V., Keun H. (2015): Diurnal rythms in the human urine metabolome during sleep and total sleep deprivation. Scientific Reports (2015), 5:14843, DOI:10.1038/srep14843
Srinivasan P., Dur-Zong Hsu, Yu-Hsuan Fu, Ming L. (2015): Sleep deprivation-induced multi-organ injury:role of oxidative stress and inflammation. EXCLI Journal (2015), 14:672-683-ISSN 1611-2156
Sá-Nunes A., Bizzarro B., Egydio F., Barros M. S., Sesti-Costa R., Soares E. M., Pina A., Russo M., Faccioli L. H., Tufik S., Andersen M. L. (2015): The dual effect of paradoxical sleep deprivation on murine immune functions. Journal of Neuroimmunology (2016), doi:10.1016/j.jneuroim.2015.11.013
Dickstein J. B., Moldofsky H. (2004): Sleep, cytokines and immune function. Sleep Medicine Reviews (1999), doi:10.1016/S1087-0792(99)90003-5
Hui L., Hua F., Diandong H., Hong Y. (2006): Effects of sleep and sleep deprivation on immunoglobulins and complement in humans. Brain, Behavior, and Immunity (2007), doi:10.1016/j.bbi.2006.09.005
Hahn J., Günter M., Autenrieth S. (2015): Impact of sleep on innate immune cells. Brain, Behavior, and Immunity (2015), doi:10.1016/j.bbi.2015.06.162
Lungato L., Gazarini M. L., Paredes-Gamero E. J., Tersariol I. l.S. , Tufik S., D'Almeida V. (2012): Sleep deprivation impairs calcium signaling in mouse splenocytes and leads to a decreased immune response. Biochimica et Biophysica Acta (BBA) - General Subjects (2012), doi:10.1016/j.bbagen.2012.09.010
Kohansieh M. és Makaryus A. N., (2015): Sleep Deficiency and Deprivation Leading to Cardiovascular Disease. International Journal of Hypertension (2015) 615681, doi: 10.1155/2015/615681
Wang J., Yuan R., Guo L., Xiong X., Liu W. (2015): The pathological effects of sleep deprivation on coronary heart disease and treatment using Chinese medicine tranquilization. Complementary Therapies in Medicine (2016), doi:10.1016/j.ctim.2015.12.004
Mullington J. M., Haack M., Toth M., Serrador J. M., Meier-Ewert H. K. (2008): Cardiovascular, Inflammatory, and Metabolic Consequences of Sleep Deprivation. Progress in Cardiovascular Diseases (2009), doi:10.1016/j.pcad.2008.10.003
Felhasznált weboldalak
http://www.sciencedirect.com/science/article/pii/S0165572815300801
http://www.sciencedirect.com/science/article/pii/S1087079299900035
http://www.sciencedirect.com/science/article/pii/S088915910600331X
http://www.sciencedirect.com/science/article/pii/S0889159115003797
http://www.sciencedirect.com/science/article/pii/S0304416512002656
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4606167/
http://www.sciencedirect.com/science/article/pii/S0965229915300261
http://www.sciencedirect.com/science/article/pii/S0033062008000911
További felhasznált irodalom
Guyton, Hall - Textbook of Medical Physiology (Elsevier Saunders, 2006)
Bódizs Róbert - Alvás, álom, bioritmusok (Medicina, 2000)
Dr. Goldschmidt Dénes, Dr. Halász Péter - Alvás, álom, álmatlanság (Medicina, 1983)
Justin Sára, Kovács Réka - A ló kialvatlansága (Pegazus magazin, 2016. március, XII. évfolyam, 3. szám, 42-45. oldal)
Ábrák:
1. Készítette: Városi Dominika
2. Átszerkesztette: Kovács Andrea
3. Szabadon felhasználható: https://en.wikipedia.org/wiki/Laboratory_rat#/media/File:Sleep-deprivation-flowerpot-technique-jepoirrier.jpg
4. Szabadon felhasználható: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4669910/figure/F2/
5. Készítette: Makk Tímea
6. Készítette: Makk Tímea