Neurotranszmitterek és érzelmek kapcsolata
Contents
1. Bevezetés
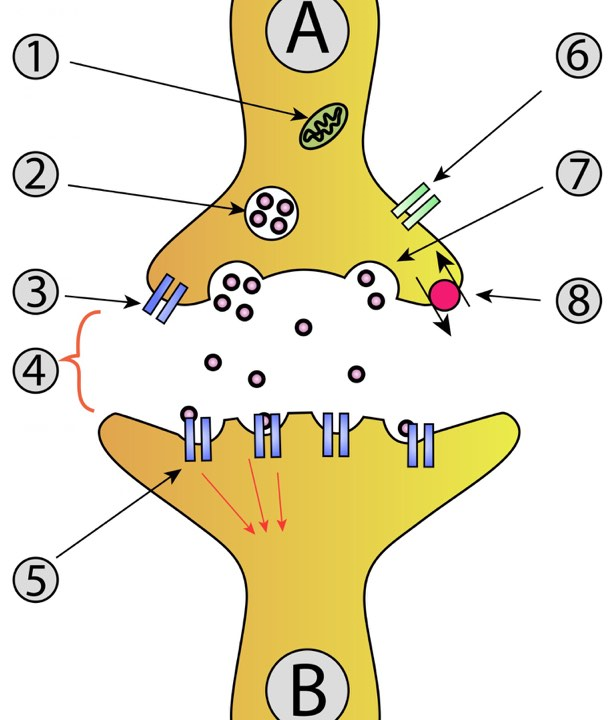
A testünkben termelődő neurotranszmitterek fontos szerepet játszanak viselkedésünk és érzelmeink szabályozásában. Ezen molekulák a kémiai szinapszisban vesznek részt, mely során egy neuron kapcsolatot létesít egy (vagy több) másik neuronnal, izom – vagy mirigysejttel. A folyamat lényege, hogy amikor az ingerület eléri az axonvégződést, az ott megtalálható szinaptikus hólyagok (bennük a neurotranszmitterekkel) exocitózissal a két neuron közötti szinaptikus résbe ürülnek, majd hatásukra a fogadó sejt továbbítja az ingerületet (1. ábra).
|
1. ábra: Kémiai szinapszis: A:preszinaptikus neuron; B:posztszinaptikus neuron; 1.:mitokondrium; 2.:szinaptikus hólyag; 3.:autoreceptor; 4.:szinaptikus rés; 5.:posztszinaptikus receptor; 6.:ioncsatorna; 7.:vesiculum exocitózisa; 8.:visszavett neurotranszmitter |
Egyes kutatások szerint érzelmi és viselkedésbeli reakcióinkban – egyéb hormonokkal, agyi és gerincvelői területekkel, és más neurotranszmitterekkel együttműködve – három fő neurotranszmitter játszik szerepet: a szerotonin, a noradrenalin és a dopamin. Ezek mennyiségének és arányainak eltolódása nemcsak hangulatbeli ingadozásokhoz, hanem komoly mentális betegségekhez is vezethet, például depresszióhoz, bipoláris zavarhoz, Parkinson-kórhoz. (Lövheim, 2011)
2. Érzelmek háromdimenziós modellje
A szerotonint az agy raphé nuclei sejtei termelik, a dopamint a substantia nigra és a ventralis tegmentalis, a noradrenalint pedig a locus coeruleus.
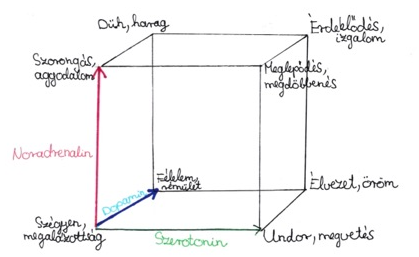
A szerotonin felelős a kielégültség, a belső erő és a magabiztosság meglétéért. A dopamin a motivációt, a jutalomérzetet, a megerősítést váltja ki, a noradrenalin pedig a figyelmet és a cselekvést. A háromdimenziós modellben az x tengelyen helyezzük el a szerotonint, az y tengelyen a noradrenalint, a z tengelyen pedig a dopamint (2. ábra). Az origó értelemszerűen azt az állapotot jelzi, mikor nem történik neurotranszmitter-leadás, a nyilak vége pedig egy-egy neurotranszmitter maximális mennyiségét jelöli. Fontos, hogy a modell egyben azt is megmutatja, hogy ezek a molekulák nem függetlenek egymástól, így alakulnak ki az érzelmek árnyalati és a reakciók sokszínűsége (Lövheim, 2011).
|
2. ábra: Az érzelmek 3D-s modellje |
Silvan Tomkins pszichológus nyolc, a koordinátarendszerbe illeszthető alapérzelmet határozott meg a huszadik században. Ezek között kettő pozitív: érdeklődés/izgalom és élvezet/öröm, egy semleges: meglepődés/megdöbbenés, és öt negatív van: szorongás/kín, félelem/rémület, szégyen/megalázottság, undor/megvetés és düh/harag. (Lövheim, 2011)
Az alábbi táblázat mutatja, hogy melyik érzelem a koordinátarendszer mely pontján helyezkedik el, az alapján, hogy a neurotranszmitterek milyen mennyiségben vannak jelen.
1. táblázat: a három fő monoamin |
|||
alapérzelmek |
szerotonin |
dopamin |
noradrenalin |
érdeklődés/ izgalom |
magas |
magas |
magas |
élvezet/ öröm |
magas |
magas |
alacsony |
meglepődés/ megdöbbenés |
magas |
alacsony |
magas |
szorongás/ kín |
alacsony |
alacsony |
magas |
félelem/ rémület |
alacsony |
magas |
alacsony |
szégyen/ megalázottság |
alacsony |
alacsony |
alacsony |
undor/ megvetés |
magas |
alacsony |
alacsony |
düh/ harag |
alacsony |
magas |
magas |
2.1. A szerotoninról általában
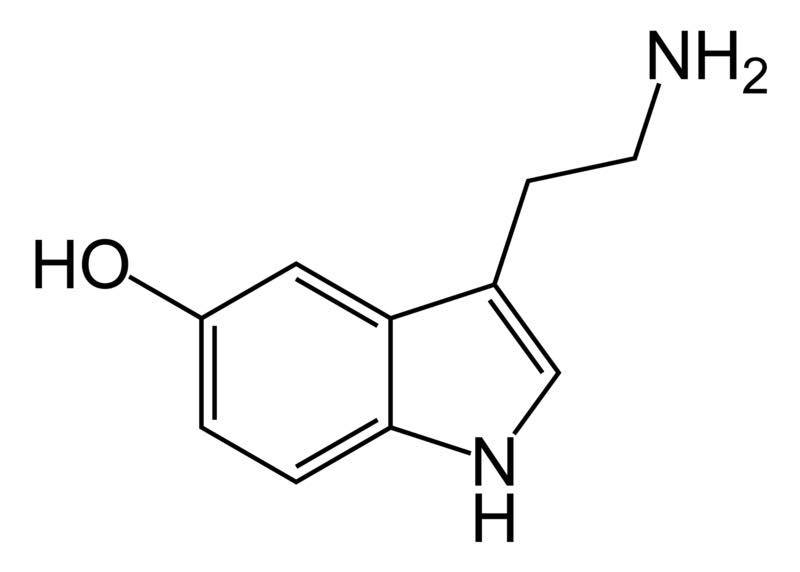
A szerotonin kémiai elnevezés szerint 5-hidroxitriptamin (5-HT), prekurzora a triptofán (3. ábra). Ahogy már korábban említésre került, az agy raphé nuclei sejtjei termelik, azon belül is frontalisan a B5 és B8 (a medialis raphé nucleus), B6 és B8 (a dorsalis raphé nucleus), valamint a B9 nevezetű sejtek (a lemiscus medialis körül diffúzan). Caudalisan találhatóak a B1-B3 sejtek. Az érzelmek irányításában a B5-B9 sejtcsoportok vesznek részt, befolyásolva a magasabb mentális működést, beleértve a kedélyállapotot, a félelmet a szorongást, a kognitív funkciókat stb. (Olivier, 2014)
|
3. ábra: A szerotonin képlete |
3. A szerotonin kapcsolata különböző érzelmekkel
3.1. A szerotonin és stressz kapcsolata
Egy eredetileg vérnyomás-csökkentőnek szánt gyógyszerről, a flezinoxánról embereken történő vizsgálatok során kiderült, hogy a humán gyógyászatban nincs vérnyomás-csökkentő hatása, valamint később az, hogy állatokban szorongás-gátlóként működik, melyet a szerotonin 5-HT1A-receptorán keresztül fejt ki. A flezinoxán mellett a buspiron és a tandospiron nevű receptor agonisták is hasonló hatással bírnak.
A Gi/Go fehérje 5-HT1A-receptorhoz kapcsolódásával különböző intracelluláris kaszkádokat indít el, mint a cAMP képződés gátlása, kalcium-csatornák gátlása és nátrium-csatornák aktiválása. Bizonyított, hogy a raphé nuclei 5-HT1A autoreceptorai különböznek a posztszinaptikus 5-HT1A heteroreceptoroktól: az autoreceptorok Gαi3 G-proteint használnak, a heteroreceptorok pedig Gα0 típusút. Ezek az anatómiai helyzetük miatt vesznek részt a szorongás kialakulásában.
Korábbi tanulmányokra alapozva patkányok és egerek stresszel járó hőemelkedés (stress-included hyperthermia, SIH) modelljét hozták létre, vizsgálva a szerotonin antagonisták stresszoldó hatását. A kísérlet során többszöri rektális hőmérsékletmérést végeztek. Az első hőmérési procedúra stressz - választ váltott ki az állatokban, ami a hőmérés eredményén, a pulzusszámon és a kortikoszteron szinten egyértelműen látható volt. A SIH intenzitása a stresszor erősségétől függ. Patkányok esetén a vizsgáló helyiségbe való belépés egy rövidebb, kisebb SIH-et vált ki, mint az új ketrecbe helyezés. Vizsgálatok során a stresszor intenzitásának változtatásával a hőemelkedéses válasz intenzitását mérték. Ennek eredménye egy intenzitás-függő növekedés lett.
Az 5-HT1A-receptor antagonistáknak a preszinaptikus autoreceptorok aktiválódása által létrejövő belső hipotermikus hatásuk mutatható ki. Arra a hipotézisre alapozva, miszerint a hipotermia preszinaptikusan közvetített, a szorongást gátló gyógyszer posztszinaptikus receptorokon keresztül fejti ki hatását. Az 5-HT1A receptor antagonisták hipotermikus hatása egerekben hasonló, mint emberekben. Ezek a receptor antagonisták szerotonerg receptorokon keresztül hatnak a rosztrális medulla raphe pallidus területén, értágulatot és csökkentett hőtermelődést okozva a barna zsírzsövetben, csökkentve a stresszel járó testhőmérséklet-emelkedést.
Az SSRI anyagokkal való kezelés csillapítja az 5-HT1A-receptor agonista által okozott hipotermiát egészséges egyedekben ugyanúgy, mint depressziós, szorongásos betegekben. Mindez azt bizonyítja, hogy az alulszabályozott 5-HT1A autoreceptorok részt vesznek az SSRI anyagok felismerésében.
Elegendő bizonyíték áll rendelkezésre, mely azt bizonyítja, hogy az egyén stresszre való érzékenysége genetikailag is meghatározott, tehát nem csak a szerotonin játszik szerepet a szorongás kialakulásában. (Olivier, 2014)
3.2. A szerotonin és szexuális viselkedés kapcsolata
Olivier kutatásában a patkányok mediális hipotalamuszának viselkedéssel kapcsolatos feladatait vizsgálta. Különböző anterior és poszterior vágásokat ejtve kiderült, hogy a hipotalamusz elülső részén végzett lézió súlyos, negatív változást idézett elő a szexuális viselkedésben.
Az SSRI anyagok használatának első évtizedében alig volt feljegyzés ezen anyagok szexuális hatásairól. Az idő előrehaladtával egyre több információ állt rendelkezésre: kiderült, hogy az összes SSRI anyag gátló hatással bír a hímek és nőstények szexuális funkcióira.
Kutatók az SSRI anyagok szexuális működési zavarokra való hatását tanulmányozták Wistar patkányokon. A kísérlet eredményeként megállapították, hogy az egyes patkányok stabil szexuális fenotípust mutatnak. Egy 30 perces tesztben, melyben egy hormonálisan indukáltan ivarzó nőstény nyitott, udvarló viselkedést tanúsít, a hím patkányok 0-5 ejakulációt produkáltak. Azt feltételezték, hogy azoknak az állatoknak, melyek keveset ejakuláltak probléma lehet a szexuális funkcióikkal. Az átlagos, közepes mennyiségben ejakulált patkányok ideálisak az antidepresszánsokkal kapcsolatos további vizsgálatokhoz, mert ezek az állatok érzékenyek azokra a gyógyszerekre, melyek stimulálják vagy gátolják a szexuális viselkedést. A többhetes kísérlet alapján megállapították, hogy az SSRI anyagok gátló hatással bírnak a hím patkányok szexuális viselkedésére, de csak hosszútávú adagolás esetén. A kísérlet konklúziója, hogy rövidtávú SSRI kezelés esetén nem jelentkezik gátló hatás.
A fenti kísérletet szűz patkányokkal is elvégezték. Itt ismételten nem volt gátló hatása az SSRI anyagoknak. Végül szexuálisan kimerült patkányokkal is megismételték a kísérletet azt feltételezve, hogy ezen patkányok érzékenyebbek a gátló gyógyszerekkel szemben, de ebben az esetben sem volt felismerhető a gátló hatás.
Mindez figyelemre méltó, ugyanis a rövidtávú SSRI kezelés hatással van a szerotonerg neurotranszmisszióra: mérések alapján fokozza a szinapszisokban a szerotonin mennyiségét az agy különböző területein.
Emberekben található egy úgynevezett SERT gén, melynek szerepe van a szerotonerg rendszer működésében. Ennek a SERT génnek a polimorfizmusa befolyásolja a gén biológiai aktivitását. Patkányok esetében polimorfizmusok helyett a génkiütés hasonló hatást vált ki. Kísérletsorozatban vizsgálták a génkiütött SERT génnel rendelkező patkányokat, amiktől redukált szexuális viselkedést vártak a vad típusú génnel rendelkező patkányokkal szemben. A kísérlet alapján a feltételezés beigazolódott: a SERT génre homozigóta patkányok szexuális aktivitása alacsonyabb a vad típussal rendelkező patkányoknál, mivel a heterozigóták nem különböznek a vad típustól. A SERT génnek fontos szerepe van a patkányok szexuális viselkedésében. Élethosszig tartó SERT gén hiány aberrált szerotonerg rendszer fejlődéséhez vezet, valamint a szexuális aktivitást 50%-kal csökkenti. (Olivier, 2014)
3.3. A szerotonin és félelem kapcsolata
A klasszikus félelem kondicionálás során egy alapvető semleges stimulust (kondicionált stimulus, például tónus vagy fény) párosítanak egy averzív stimulussal (nem kondicionált stimulus, például rövid elektromos sokkolás). Ennek a párosításnak az eredménye, hogy a semleges stimulus averzív tulajdonságot szerez. A fenti stimulusra adott válasz állatok esetében jellegzetes: ez a félelem, mely megnövekedő pulzussal, vérnyomással és jellegzetes viselkedésformákkal, például lemerevedéssel jár.
Ha egy állat hosszabb időn keresztül ki van téve egy kondicionált stimulusnak a nem kondicionált stimulus hiányában, akkor fokozatos csökkenés jelentkezik a félelem kiváltódásban . Ahelyett, hogy az eredeti emlék törlődne, a félelemhez való alkalmazkodás egy új tanulási folyamatként jelenik meg, ami gátolja az eredeti félelem-emléket.
Emberekben az amygdala vagy az insula károsítása esetén is tudatosan érzékelhetőek az érzelmek, többek között a pánik is, habár a félelem kondicionálás amygdala károsítás esetén nem működik.
Léziót és inaktivációt alkalmazó tanulmányok alapján az amygdala laterális magja határozható meg a (nem)-kondicionált stimulusok legfőbb központjaként, ahová a kortikális és szubkortikális területekről is érkeznek információk.
Az amygdala és a hippocampus területe 5-HT-receptorokban gazdag. Ezt az alábbi kutatás bizonyította: megvizsgálták, hogy a szerotonin hogyan hat a félelem kondicionálásra és csökkentésére. A kísérlet során fontos volt szem előtt tartani az 5-HT receptorok sokféle altípusát. Rendszeres 5-HT2A -receptor agonisták injekciózásával fokozták az elkerülési memóriát és a pislogás kondicionálását. Alzheimer-kórban szenvedő betegek esetében csökkent kapcsolódási képességet figyeltek meg ezeknél a receptoroknál (Bauer, 2014).
3.4. A szerotonin és agresszió kapcsolata
Hím egerekkel való kísérletek során azt figyelték meg, hogy a hipotalamusz mediális részének elektromos ingerlése agresszív viselkedéshez, illetve a táplálkozással és a szexuális működéssel kapcsolatos komplex viselkedési mechanizmusok változásához vezet. Ez megmagyarázza az agresszió kezelésére alkalmazott gyógyszerek szedatív hatását, illetve, hogy miért okoztak mozgási problémákat és egyéb nemkívánt következményeket. Ezért olyan új gyógyszereket kellett keresni, amik specifikusan az agressziót gátolják.
Az alapvető feltételezés a szerotoninnal és az agresszióval kapcsolatban még mindig áll, miszerint az 5-HT gátolja az agressziót. Ezt az inverz kapcsolatot állatokkal és humán vonalon végzett kutatások is alátámasztották. A kutatások során az is kiderült, hogy a triptofán is hat közvetetten a hangulatingadozásokra és az agresszióra: a növekvő triptofán -szint csökkenti az agressziót.
Az agresszióval kapcsolatos kutatások során nemcsak a triptofán mennyiségét, hanem a megfigyelt állatok más élettani paramétereit is érdemes mérni. Ennek egyik módja, hogy egymással szemben agresszív viselkedést mutató (egymással harcoló) állatokat vizsgálunk, és a harc előtt, közben és után veszünk mintákat az állatoktól. Ezek során derült ki, hogy a dopamin szintje is növekvő aktivitást mutat a harc során. Valószínűleg a dopamin az agresszív érzelmek és viselkedési minták kialakulásában és lefolyásában, a szerotonin pedig ennek megszüntetésében játszik szerepet. Végül arra a következtetésre jutottak, hogy a szerotonin az agresszió mértékének beállításában is jelentős. Az utóbbi században a kutatók különbséget tettek a normális, fajspecifikus, és az abnormális, fokozott agresszió között. Normálisnak azt a fajta agressziót tekintjük, mely az egyed fajspecifikus mintázatot mutató válasza a környezetre, ellenben a fokozott agresszió nem minden egyedben mutatkozik meg, és mértéke nem arányos az egyedet érő környezeti inger erősségével. A normális és a fokozott agresszió különböző regulációjú. Ez utóbbit tekintjük kórosnak, és a szerotonin szintje is csak ebben az esetben alacsonyabb, mint a szervezet alap szerotonin -szintje.
A szerotonerg rendszer nem homogén, elektrofiziológiásan, funkcionálisan és anatómiailag is differenciált. Az agy vizsgálatával kapcsolatos kutatások során ezen kívül megfigyelték, hogy a hipotalamusz ingerlése is válthat ki agresszív viselkedést: a hipotalamusz stimulációjakor a megfigyelt állat olyan agresszív viselkedési formákat mutat, amelyeket egy ellenfél egyed megjelenésekor szokott produkálni (mozgásaktivitás, fogcsattogtatás).
Az agresszív viselkedést ezeken kívül a génexpresszió manipulálásával is befolyásolhatjuk. Knockout egerekkel végzett kísérletek során a 14 féle szerotonin-receptor közül az 5-H T1A és 5-HT1B receptort vizsgálták. A kutatások során arra derült fény, hogy míg az 5-HT1Areceptor kiütésével a vizsgált egerek szelídebbek, ám félősebbek voltak, ezzel ellentétben azok az állatok, melyekben az 5-HT1B receptort ütötték ki, még agresszívabb viselkedést mutattak. Ebből arra következtethetünk, hogy az 5-H T1A receptor stimulációja fokozza, míg az 5-HT1B receptoré csökkenti az agressziót. Ezt későbbi humán kísérletek is alátámasztották, melyben azok az emberek mutattak magasabb agressziót, akiknél a prefrontális kéregben az 5-HT1A receptorok sűrűsége, vagy szerotoninhoz való affinitása magasabb volt.
Emberben az agresszió összefüggésbe hozható a szuicid hajlammal, mivel mindkét viselkedési probléma összefügg az alacsony szerotonerg működéssel, de ettől még lehetséges, hogy a két jelenség egymástól függetlenül szabályozott.Továbbá a szerotonin alacsony szintje, illetve teljes hiánya okozhat lobbanékony (impulzív) természetet, vakmerőséget. (Olivier, 2014)
3.5. A szerotonin és depresszió kapcsolata
A neuronális reuptake-mechanizmust először a noradrenalinnal, majd a szerotoninnal vizsgálták. Ennek a mechanizmusnak fontos reguláló szerepe van a szerotonerg neuronok aktivitásában, illetve az alacsony katekolamin-aktivitás és a depresszió között is mutattak ki összefüggést. Ezen a kutatási vonalon elindulva a gyógyszergyártó cégek olyan anyagokat próbáltak előállítani, amik blokkolják a katekolaminok visszavételét a szinaptikus résből. Később azt is kimutatták, hogy az 5-HT fontos szerepet játszik a depresszió kialakulásában, és ezeket a tényeket együttesen a "depresszió -szerotonin hipotézisének" nevezzük (Werner és Covenas, 2010).
4. Antidepresszánsok és szerotonin
Napjaink leghatásosabb antidepresszánsai szervezetünk szerotonin szintjét befolyásolják. Depressziós állapotban az agy szerotonin szintje jelentősen lecsökken. A szerotonerg antidepresszánsok különböző mechanizmusok során növelik ezen neurotranszmitter mennyiségét.
Depresszió során a betegnek jelentősen romolhatnak a kognitív funkciói: memória, tanulás, komplex problémamegoldó-képesség, figyelem megtartása és pszichomotoros funkciók . Ennek ellenére depressziós eseteknél gyakori, hogy a betegséggel kapcsolatos memória jobban, míg a pozitív eseményekkel kapcsolatos kevésbé hatékony, mint az egészséges egyedeknél. Ezek a jelenségek sokszor megfigyelhetőek már gyógyult betegeknél is, bár általában nem szignifikáns a vizsgálatok alapján. Továbbá probléma merülhet fel depresszió során a döntéshozatalban, valamint erősebb hajlam alakulhat ki a negatív ingerek befogadására. Ezeket a tipikus jegyek az úgynevezett Dysfunctional Attitudes Scale (DAS) által értékelhetőek.
Az antidepresszánsok a kognitív funkciókban okoznak elsőként változásokat, ez akár a beadás utáni első-második órában jelentkezhet. Az érzelmi információk feldolgozásában (elsősorban az arckifejezések felismerésében) maximum egy hét után érezhető változás, míg a páciens hangulatának javulásához akár hetek is szükségesek.
Az antidepresszánsok kutatásának alapja négy eljárásra épül: 1. szerotonerg antidepresszánsok, 2. a szerotonin receptor agonisták és antagonisták, 3. triptofán-adagolás és 4. triptofán-megvonás hatásai. (Merens és mtsai, 2007)
4.1. Szerotonerg antidepresszánsok: szelektív szerotoninvisszavétel-gátlók hatása (SSRI)
Kutatók rövid-távú kísérletek során hasonlították össze az SSRI hatásait egészséges és a múltban depresszióval kezelt nőkön, arckifejezés-felismerés által. Utóbbiak előzetes vizsgálatok során jobban teljesítettek a félelem azonosításában. Harminc perc múlva az intravénásan beadott citalopram ezt a különbséget megszüntette, azonban egészséges nőknél felerősítette a félelem-felismerés arányát. A szubjektív szorongás érzete mindkét csoport esetében felerősödött, bár a depressziós múlttal rendelkezőknél erősebben volt megfigyelhető. Ezek alapján lehetséges, hogy a kognitív sebezhetőség érzékenyebb a rövidtávú antidepresszáns-adagolásra.
Ismételt SSRI adagolás mellett egészséges nőknél csökken a félelem és a düh felismerésének aránya, és nőtt a pozitív memória mértéke. A kedélyállapot változása viszont csak már felépült depressziós betegeknél volt megfigyelhető (Merens és mtsai, 2007).
4.2. Szerotonin receptor agonisták és antagonisták hatásai
2003-ban kísérleteket folytattak a d-fenfluramin és a clonidin (egy receptor agonista, mint placebo) hatásairól az érzelmi zavarokon, valamint az 5-HT2 receptor elérhetőségén az agykéregben.
Három különböző csoportot állítottak ki: az elsőben kezeletlen depressziós betegek, a másodikban korábban már a depresszív epizódon kívül önbántalmazó viselkedést mutató páciensek voltak (mindegyikük borderline személyiségzavarral diagnosztizált), a harmadikban pedig egészségesek. Ennek oka az a felismerés, hogy öngyilkos áldozatoknál – depressziós tünetekkel vagy nélkül is – sokkal magasabb 5-TH2 receptort találtak a prefrontális kéregben.
Az eredmények a következőek voltak: az érzelmi zavarok erősen mutatkoztak d-fenfluramin adagolása után egészséges jelentkezőkben. Egy második kísérlet kimutatta, hogy az érzelmi zavarok depressziós betegeknél erősen összefüggenek az 5-TH2 receptor sűrűségével, azonban ez nem volt igaz az önbántalmazó és az egészséges vizsgáltaknál, sőt az önbántalmazó csoportnál egyáltalán nem találtak összefüggést e tényezők között. Ezek által feltételezték, hogy az eredmény oka az, hogy a borderline személyiségzavarban sok más pszichológiai tényező is szerepet játszik, mely befolyásolja az érzelmi zavarok és a szerotonin kapcsolatát, így egyedül ez a kezelési módszer nem lesz hatásos a betegeknél.
Később a szerotonin antagonisták hatását az érzelmek feldolgozásában is megfigyelték. Ehhez egészséges önkénteseknek ondansetront adtak szájon át. A kísérlet a következő eredménnyel zárult: ez az anyag csökkentette a negatív ingerekre adott válasz erősségét, azonban nem volt hatással sem a kedélyállapotra, sem az arckifejezések felismerésére (Merens és mtsai, 2007).
4.3. Triptofán adagolásának hatásai
L-triptofán adagolása, mint a szerotonin prekurzora, emeli annak agyi szintjét. A triptofánt intravénásan és szájon át is (alpha-lactalbumin) be lehet juttatni a szervezetbe. Az alpha-lactalbumin javította a memória működését egészséges, stresszre érzékeny önkénteseknél, valamint a vizuális memóriát is, azonban lelassította az egyszerű motoros válaszokat, anélkül, hogy a hangulatot befolyásolta volna mind egészséges, mind depressziós pácienseknél . A félelem és a boldogság arckifejezését is hamarabb ismerték fel a vizsgáltak.
Hosszabb távú kezelés esetén az eredmény meglepő volt: csak egészséges nőknél figyeltek meg gyorsulást a boldogság, és csökkenést az undor felismerésében. Kedélyállapot-változás itt sem volt észrevehető, de a negatív stimulusokra gyengébben reagáltak (Merens és mtsai, 2007).
4.4. Triptofán megvonásának hatásai
Kis dózisú akut triptofán megvonás (ATD) hatására egészséges jelentkezőknél csak kicsi hangulatbeli ingadozást detektáltak, a depresszióval küzdők csoportjában a kezelés napján semmilyen, az azt követő napon pedig kisebb változásokat figyeltek meg; a kedélyállapotban azonban egyetlen esetben sem volt számottevő a változás).
ATD nagy dózisban a várakozásokhoz híven 50-60%-os visszaesést okozott a már gyógyult depressziós betegeknél. Általánosságban erősödtek a negatív reakciók és a hajlam a negatív érzelmekre, károsodott a rövidtávú memória, és a pozitív arckifejezések felismerése.
Egy másik kísérletsorozat a gyógyult depressziós betegek között két csoportot különített el: a gyógyszeresen kezelt és a gyógyszeres kezelés nélkül felépülteket. A kísérlet során kiderült, hogy a múltban kezelt önkéntesek esetén az ATD emelte a szociális szorongás és a depressziós tünetek mértékét; azonban a kezelés nélkül gyógyult (és az egészséges kontrollcsoport) sem kedélyállapotára, sem az érzelemfeldolgozására nem volt hatással. A következtetés, hogy az ATD valószínűleg gátolja az antidepresszánsok helyes működését (a kezelt betegek nem SSRI-vel, hanem más szerotonerg antidepresszánsssal kezelték) (Merens és mtsai, 2007).
5. Összegzés
Az évtizedek óta tartó kutatások ellenére is sok bizonytalanság övezi az agyi működést. Az érzelmek irányítására, összehangolására, meghatározására is igaz ez. A szerotonin, mint neurotranszmitter, kis mennyisége ellenére az érzelmek széles skáláját befolyásolja. Hatását sosem teljesen önállóan fejti ki, de bizonyítottan nagy hatással bír a hangulatra és az ösztönös, életben maradáshoz elengedhetetlen reakciókra. E molekula megismerésének segítségével komoly eredményeket értek el- többek között- a depresszió sikeres kezelésében is.
6. Felhasznált források
6.1. Irodalomjegyzék
• Bauer, E. P. (2014): Serotonin in fear conditioning processes. Behavioural Brain Research 277: 68-77 https://doi.org/10.1016/j.bbr.2014.07.028
• Lövheim, H. (2011): A new three-dimensional model for emotions and monoamine neurotransmitters. Medical Hypotheses 78: 341-348 https://doi.org/10.1016/j.mehy.2011.11.016
• Merens, W.; Van der Does, A.J. W.; Spinhoven, P. (2007): The effects of serotonin manipulations on emotional information processing and mood. Journal of Affective Disorders 103: 43-62 https://doi.org/10.1016/j.jad.2007.01.032
• Olivier, B. (2014): Serotonin: A never-ending story. European Journal of Pharmacology 753: 2-18 https://doi.org/10.1016/j.ejphar.2014.10.031
•Werner, F. M.; Covenas, R. (2010): Classical Neurotransmitters and Neuropeptides Involved in Major Depression: a Review. International Journal of Neuroscience 120: 455-470 https://doi.org/10.3109/00207454.2010.483651
6.2. Ábrajegyzék
1. ábra: szinapszis https://en.wikipedia.org/wiki/Synaptic_vesicle#/media/File:Synapse_diag1.svg
2. ábra: 3D-s modell. Lövheim, H. (2011): A new three-dimensional model for emotions and monoamine neurotransmitters. Medical Hypotheses 78: 341-348. alapján saját készítésű.
3. ábra: a szerotonin képlete https://upload.wikimedia.org/wikipedia/commons/d/dd/Serotonin-skeletal.png
6.3. Táblázatjegyzék
1. táblázat: a három fő monoamin. Lövheim, H. (2011): A new three-dimensional model for emotions and monoamine neurotransmitters. Medical Hypotheses 78: 341-348. alapján saját készítésű.