A tőgy immunológiája
Contents
Bevezetés
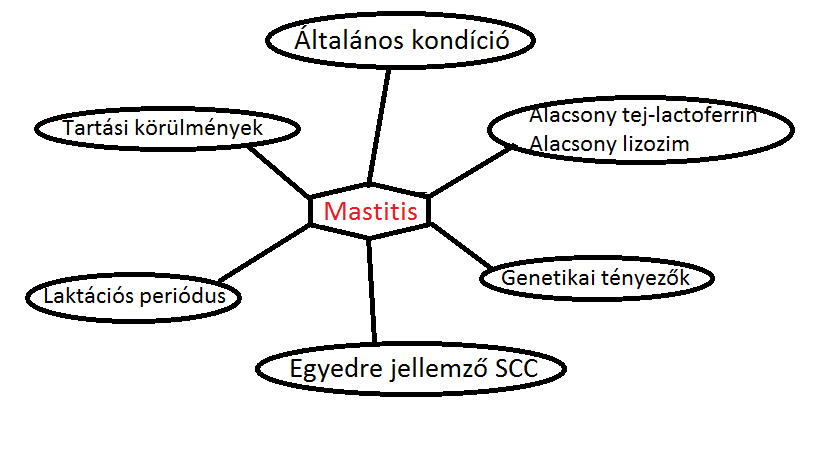
A tejelő szarvasmarha-állományok megbetegedései közül is kiemelkednek a tőgyet érő gyulladásos elváltozások. A mastitis (tőgygyulladás) a legnagyobb gazdasági kárral járó megbetegedés. A mastitis megjelenési formája nagyban függ a pathogén típusától, a fertőzésre adott válasz igen sokrétű a kiváltó kórokozótól függően. A mastitis kialakulását, lefolyását igen sok tényező befolyásolja mind állomány-, mind egyedszinten (1. ábra). A következőkben ezen igen változatos védekezési mechanizmusokat szeretnénk bemutatni egy kicsit részletesebben.
|
A tőgy anatómiai és szövettani jellemzése
A tőgy a kültakaró egyik módosulta, amit kívülről cutis takar,de nincsen subcutis. A szervet felületes és mély pólya (fascia superficialis/profunda mammae) függeszti fel. A mély pólyának két lamina lateralis-a és két lamina medialis-a van. Ezekről a főlemezekről ún. melléklemezek erednek (lamallae suspensoriae), melyek a mirigylebenykék között haladnak. A mély pólyán belül találjuk a rendezetlen tömöttrostos kötöszövetből álló kötőszövetes tokot (capsula mammae), amey az interstitium része. Ebből lazarostos kötőszövetből felépülő sövények indulnak ki, melyek szintén az interstitium részei, és lebenyezetté teszik a szervet. Ennek a lazarostos kötőszövetnek a folytatása képez burkot a mirigyvégkamrák (periglanduláris ksz.) és a kivezető csövek (peritubuláris ksz.) körül. A szerv parenchyma-ját a mirigyvégkamrák és a hozzájuk tartozó kivezető csövek teszik ki. (Röhlich, 2006) A mirigyvégkamrák bogyószerűek és őket egyrétegben bélelik az epithelsejtek (MEC= Mammary Epithelial Cell). Második legnagyobb számban jelenlévő sejftéleség az MFC (Mammary Fibroblast Cell) és ezenkívül a permamensen jelenlévő boMdM (bovine Monocyta-derived Macrophag). A hámsejteket lamina basalis veszi körül, majd ezt a periglandularis kötőszövet övezi. Myoepithel sejtek is találhatóak a kamrák falában, melyeknek feladata a tej ürítése. Laktációs időszakban a tőgy állományának 70%-a MEC (Günther és mtsai, 2016). A mirigykivezető csatornák rendszere: az intralobularis kivezető csövekkel kezdődik, melyek közvetlenül a mirigyvégkamrákból indulnak ki. Ezek kilépve a kamrákból interlobuláris kivezető csövekké (ductus lactiferi, tejutak) szedődnek össze, melyek a tejmedencében (sinus lactiferi) végződnek. Ennek van egy pars glandularis és egy pars papillaris része. A kettő határán szűkület található, melyben a Fürstenberg-féle vénagyűrű (circulus venosus papillae) foglal helyet, ami vegetatív idegrendszeri hatásra a nyílást zárni képes. A pars papillaris tölcsérszerűen szűkül, és végül ductus papillaris-ban végződik. Itt záróizom és tejfaggyú (lactosebum) felelős a megfelelő záródásért. (Fehér, 2006) Természetesen a tejmirigy szövettani képe nagyon eltérő egy tejelő és egy nem tejelő állatban. A tejmirigy képe emellett az egyedfejlődés során is jelentősen változik. Artériás vérellátásáért az a. pudenda externa-ból eredő a. mammaria cranialis et caudalis felelős. A vénás vért a circulus venosus mammae-ból kiinduló v. epigastrica cranialis superficialis (cranialisirányba), v. pudenda externa és a v. labialis (caudalisirányba) szállítja el, illetve jelentős szerepe van még a v. subcutanea abdominis-nek is. Nyirokcsomók közül elsősorban a lnn. inguinales superficiales-eknek (lnn. mammari) van komolyabb jelentőségük. A tőgy beidegzéséért elsősorban n. genitofemoralis felelős, emellett a n. pudendus-nak és a n. ilioinguinalis-nak is szerepe van az innervációban. (König, 2004)
Védekezési mechanizmusok
A védekezési mechanizmusok két csoportra oszthatók, ezek a veleszületett immunitás (nem specifikus) és a specifikus immunitás. A nem specifikus immunelemek aktiválódnak először a fertőzés korai fázisában. A veleszületett immunitás elmei a macrophagok, NK-sejtek, neutrophil granulocyták és egyes lízist okozó faktorok. A tőgy szekretáló volta miatt vérellátása gazdag, laktációs periódusban pedig hatványozottabban több vért kap mint szárazon állás időszakában. A jó vérellátás következménye, hogy a tőgy szövetében a neutrophil granulocyták és a macrophagok nagy számban vannak jelen, nagy arányban kitapadva fertőzésmentes időszakban is. A tőgy jellegzetes képlete a Fürstenberg-féle rozetta, az elsőszámú védelmi vonal, mely mint anatómiai barrier veszt rész a védekezésben. A sphincter izmok megakadályozzák a kórokozók bejutását a fejések közötti időszakban. A ductus papillaris keratinizáltságának is szerepe van a védelemben, így a keratinréteg megsérülése jelentősen növeli a baktériumfertőzés kockázatát. Szárazon állás időszakában a keratin teljesen el is zárhatja a ductust. Ezen kívül a keratinréteg tartalmaz antimicrobiális anyagokat is. Ezek közé tartoznak például észterezett és nem észterezett zsírsavak, mint a mirisztinsav (C14H28O2), palmitoleinsav(C16H30O2), linolsav (C18H32O2), illetve pozitív töltésű proteinek, melyek képesek a pathogénhez kötődni, sejtfalukat károsítani és ozmotikus viszonyaikat megváltoztatni. Amennyiben a kórokozó "túljutott" a nem specifikus elemeken, abban az esetben a specifikus immunrendszer aktiválódik. A tőgyben az immunrendszer mindkét típusának tökéletes működése szükséges a kialakulandó mastitis leküzdése érdekében (Sordillo és Streicher, 2002).
A tőgygyulladás lefolyása és kialakulása
A következőkben egy gyulladás általános lefolyását és körülményeit ismertetjük.
Ha egy fertőző ágens bekerül a tőgybe, azok leggyakrabban a testi sejtek közül az epitheliális sejtekkel érintkeznek először (Griesbeck-Zilch., 2009). Az epitheliális sejtek felületén számos toll-like receptor ( TLR-2 és TLR-4) található.A TLR-eket PAMP-ok (pathogen-derived molecular patterns) aktiválják mint ligandok, tőgyfertőzés esetében általában ez a baktériumok által termelt endotoxinokat jelenti. A kötődés kaszkádreakciót indít be, melynek végén az NF-kb transzkripciós faktor aktiválódik. Ez a faktor több mint 200 immun-gén expresszióját regulálja (Hoesel és Schmid, 2013). Az endotoxinok általában a sejtfal felületén található különböző liposzacharidok. Amint ezeket az anyagokat egy sejt érzékeli, egyrészt mRNS transzkripciót fokozás történik, ami gyulladási faktorok szintézisét és ürülését idézi elő, mint például a cytokinekhez tartozó IL-6 vagy a chemokinekhez tartozó IL-8 (Griesbeck-Zilch., 2009). Másrészt antigén-prezentáció megy végbe. A tehén 18-as kromoszómáján található egy kvalitatív jellemet kódoló locus, mely a gyulladási faktoroknak a termelését szabályozza(Kühn 2009.). A gyulladás kialakításában a veleszületett immunitás (innate immunity) játszik szerepet. Ennek vannak celluláris és humorális tagjai. A humorális tagok közül a különböző komplement fehérjék, a lizozim és a lactoferrin (egy vasat tartalmazó, összetett globuláris fehérje) a legfontosabbak. A sejtes elemek közül a neutrophil granulocyták a legaktívabbak. Először a neutrophil granulocyták érkeznek a baktérium-fertőzött területre, pozitív kemotaxissal, kitűnő migrációs és diapedesises képességüket kihasználván. Különböző faktorok nem léte mellett is képesek bekebelezni a baktériumokat, de leginkább a felszabaduló gyulladási faktorok és a specifikus immunrendszer serkentése mellett lépnek ki a kapillárisok falán keresztül. A neutrophil granulociták két módon hatástalanítják a baktériumokat. Egyrészt bekebelezi őket, és emésztés után egy fehérjét termelnek és adnak le a környezetükbe, mely hálózatot alakít ki. Ebbe a hálózatba a baktériumok felakadnak, így mozgásuk korlátozottá válik, ezáltal csökken a terjedésük sebessége és könnyebbé válik a bekebelezésük, angolul ezt neutrophil extracellular trap-nek hívják (Burvenich, 2007). A fehérvérsejtek ezenkívül reaktív oxigén gyököket (ROS) is termelnek. Mivel a gyökök ugyanolyan veszélyesek a saját sejtekre mint a kórokozókra, termelésüket a szervezet különböző cytokinekkel erősen szabályozza. Dendrtitikus sejtek és macrophagok is tartózkodnak a tőgy szövetében. Ezek óriási mennyiségű cytokin termelésére képesek. Pathogén-specifikus immunválaszban való számszerű szerepük még nem tisztázódott.
A tőgy morfológiája és fertőzésekkel szembeni érzékenysége közötti összefüggés
Egy tanulmány szerint a tőgy fertőzésekkel szembeni érzékenységét, és így a tej SCC szintjét (mely növekedésével egyenesen arányos a tőgy fertőzöttségi foka) mind a mirigytestnek (corpus mammae) és a csecsbimbónak (papilla mammae) az alakja, mind a csecsbimbónak a hossza és a vastagsága jelentősen befolyásolja (1. táblázat). A kutatás során fertőzött tőgyeket vizsgáltak, és az egyes tőgyek morfológiai különbségei és a fertőzöttségi fok közötti összefüggéseket keresték. Fontos megjegyezni a tanulmány későbbi megértéséhez, hogy a tőgy egészségi állapotát a tej SCC szintjével könnyen megállapíthatjuk. Az SCC szint nemcsak a tej minőségéről, hanem az egész állatról általános egészségügyi információt szolgáltat.
A tőgy alakja szerint két csoportot különíthetünk el: megereszkedett és szabályos. Megereszkedett tőgy esetében magasabb SCC-t mértek, mint a szabályos alakúnál. Valószínűleg ennek az erősebb fertőzési hajlamnak a megereszkedés lehet az egyik legfontosabb összetevője, – egy másik kutatás szerint – hiszen így a tőgy könnyebben sérül, érintkezik kórokozókkal, fertőződik. A csecsbimbó alakja szerint megkülönböztetünk laposat, hegyeset vagy befordultat. A vizsgálat során lapos csecsbimbó esetén mérték a legmagasabb SCC-szintet, ezt követte a befordult, majd a hegyes típus (1. táblázat). Kissé hegyes és befordult csecsbimbók fogékonyabbak mastitis-re, mivel könnyebben felhalmozódik bennük tej, s így táptalajt nyújtanak egyes baktériumoknak. Ezen kevésbé előnyös csecsbimbó-formákat tenyésztéssel azonban könnyen szelektálhatjuk. A tejminták analízise azt is kimutatta, hogy a csecsbimbó vastagsága és hossza, illetve a tőgy fertőzésekkel szembeni érzékenysége között egyenes arányosság van, így mind a hosszú, mind a vastag csecsbimbók esetén magas SCC-t mértek (Bharti és mtsai, 2015).
SCC átlagok az egyes tőgyformákban és csecsbimbó alakokban |
||
Jellemvonások |
Megfigyelések száma |
Átlagok (standard hibával) |
Megereszkedett |
74 |
6.393±0.037 |
Szabályos |
292 |
5.120±0.034 |
Lapos |
46 |
6.189±0.105 |
Befordult |
90 |
5.850±0.068 |
Hegyes |
230 |
5.030±0.035 |
1. táblázat (Bharti és mtsai, 2015) |
||
A tőgy jellemző fertőzései
Vírusos fertőzések
Papillomavírusok
A papillomavírusok kicsi, burok nélküli, duplaszálú DNS-vírusok, melyek legfőképp gerincesek bőr és nyálkahártyáinak epithelsejtjeinek magjában multiplikálódnak és okoznak szemölcsöket. A szarvasmarhát fertőző papillomavírus, BPV (Bovine Papillomavirus) felelős a bőr és tőgy papillomatosisáért, emellett egyéb rosszindulatú daganatokat okozhat a húgyhólyagban és a felsőbb emésztőtraktusban (Campo, 2002). Az eddig ismert BPV-ket (BPV1-13) genomuk feltérképezése után négy csoportba sorolják, ezek: Deltapapillomavirusok ( BPV1, 2, 13), Xipapillomavírusok (BPV3, 4, 6, 9, 10, 11, 12), Epsilonpapillomavírusok (BPV5, 8), és a BPV7. BPV-fertőzés világszerte előfordul, és habár nem okoz olyan mértékű gazdasági kárt, mint az E. coli eredetű mastitis, a szemölcsök, fekélyesedés, hámsérülések következtében romlik a tejtermelés, illetve a különböző hámsérülések miatt az állat jóval fogékonyabbá válik mastitisre. Az esetek többségében a tőgyet érő papillomatosisos elváltozások hátterében a BPV6 áll, ugyanakkor az összes többi BPV (különösen a BPV7, 9, 10) is okozhat tőgy-papillomatosist. Szövettani vizsgálatok alapján jóindulatú daganatra lehet következtetni, függetlenül a háttérben jelen lévő BPV típusától. A BPV-fertőzést a hámszövet jellegzetes kórszövettani elváltozásai kísérik. (Tozato és mtsai, 2013)
Leukémia vírusok
A szarvasmarha leukémia vírusa, a BLV (Bovine Leukemia Virus) a Retroviridae családba tartozik. Szarvasmarha-állományok egyik legelterjedtebb vírusa, de Európa egyes területei már mentesek tőle. Megjelenhet tartós lymhocytosisként (PL), ekkor a keringő lymphocyták száma megemelkedik, illetve ritkábban B-sejt lymphomaként (Della Libera és mtsai, 2015). BLV a fertőzött szarvasmarháknál az esetek 20-30 százalékában tartós lymphocytosisként jelentkezik ( Gillet és mtsai, 2007)
A kéknyelv-betegség vírus 8-as szerotípusának (BTV-8) hatása a tejtermelésre
A BTV-8 fertőzés jelentős változásokat idéz elő a tejtermelésben - derült ki egy holland kísérletből, melyben a vizsgálat kezdetén még szeronegatív tehenek tejtermelésének a fertőzés hatására kialakult változásait figyelték meg.
A fertőzött állatok idővel szeropozitívak lesznek, hiszen vérükben már kimutatható a BTV-8 ellenanyag. A BTV-8-tel fertőzött állat tejtermelése az antitestek megjelenése és vérből való kimutathatósága közötti időszakban csökken. (Ezen időszak hossza és a tejtermelés között negatív korreláció van.) Mivel szubklinkai fertőzésről beszélünk, ezért fontos megjegyezni, hogy ezen vírus (és emellett még sok más patogén is) által okozott infekció komoly gazdasági károkat okozhat, hiszen látszólag teljesen egészséges az állat. Mind az antitestek megjelenése előtt, mind a szeropozitív vérkép kialakulása után a tejtermelés teljesen normális képet mutat. (Santman-Berends és mtsai, 2011).
Bakteriális fertőzések
Baktériumok esetén a Gram-pozitív és Gram-negatív csoportba való tartozás határozza meg a kiváltott gyulladás jellemzőit. A Gram-negatív csoportba tartozó fajok akut mastitist váltanak ki, míg a Gram-pozitív baktériumok enyhébb, általában tünetmentes, de hosszú ideig (akár 2 hónapig) fennálló gyulladást okoznak, mely normálistól eltérő tejtermeléssel jelentkezik. A mastitisek nagy hányadát a Gram-negatív Escherichia coli, e mellett a Gram-pozitív Staphylococcus aureus és Streptococcus uberis okozzák. E. coli fertőzés hatására nagymértékű cytokinszint emelkedés történik, míg a Gram-pozitív baktériumok, mint az S. aureus és S. uberis jóval kevésbé indukálják a gyulladási cytokinek termelését (Günther és mtsai, 2016). A fertőzést ért tőgynegyedekről a fertőzés átterjed a szomszédos, addig érintetlen negyedekre, tehát a tőgy mint egész ad választ az őt érő pathogén hatásokra. Az E. coli okozta fertőzés hordozza magában a legnagyobb gazdasági kár kockázatát. Az alom szennyezettsége, a nedves környezet, a felhalmozódó ürülék, a rossz tartási körülmények növelik a fertőzés kialakulásának valószínűségét. A mastitis súlyosságára, klinikai vagy szubklinikai voltára a tejben és vérben megjelenő egyes sejteknek a számából és arányából lehet következtetni. Egy Karan-fríz fajtájú szarvasmarha állományon végzett vizsgálat szerint (M. Alhussien és mtsai, 2015) a korai laktációs periódusban az összfehérvérsejtszám szignifikánsan a legmamagasabb az akut mastitises egyedeknél a vérmintákban (2. táblázat). A korai laktációs periódus abból a szempontból a legkritikusabb időszak, hogy ilyenkor a nem szekretáló tejtermelő epithelsejtek drasztikus celluláris, morfológiai, biokémiai változásokon mennek keresztül, így válva szekretáló sejtekké. E változások időszakában a tőgy fogékonyabb a fertőzésekre. Neutrophil granulocyta arány és a neutrophil granulocyták közti éretlen sejtek száma is szignifikáns különbséget mutat a gyulladásos egyedek javára. Az élő neutrophil granulocyták aránya szignifikánsan nagyobb a nem fertőzött csoportban.
Vér |
Egészséges |
Szubklinikai mastitis |
Akut mastitis |
összfehérvérsejtszám (×103) |
7293±35.52 |
8417±55.96 |
9237±95.55 |
Neutrophil (%) |
24.66±0.2 |
38.78±0.34 |
60.01±0.70 |
Szegmentált n. (%) |
97.5±0.46 |
97.25±0.49 |
96.88±0.54 |
Stab n. (%) |
2.5±0.46 |
2.75±0.49 |
3.125±0.54 |
Élő n. (%) |
93.33±0.31 |
84.42±0.51 |
80.78±0.60 |
Lymphocyta (%) |
57.29±0.27 |
48.29±0.22 |
19.44±0.46 |
Monocyta (%) |
6.23±0.17 |
3.98±0.07 |
5.42±0.20 |
Phagocytáló aktivitás |
0.54±0.02 |
0.25±0.01 |
0.30±0.01 |
2. táblázat (Alhussien és mtsai, 2015) |
|||
A tejminták eredménye szerint a fertőzött egyedekben szignifikánsan magasabb az SCC-szint mint nem mastitises állatokban, emellett nagyobb a neutrophil granulocyták aránya is. A vér eredetű mintákkal összevetve a tejben nagyobb számban jelennek meg neutrophil granulocyták mint a vérben. A neutrophil granulocyták között csökkent a szegmentált, ezzel együtt, csakúgy mint a vérben, nőtt a Stab alakok száma. Akut mastitises egyed élő neutrophil granulocytáinak aránya jelentősen alacsonyabb mint a vérbeli neutrophil granulocytáknál (3. táblázat).
Tej |
Egészséges |
Szubklinikai mastitis |
Akut mastitis |
SCC (×105) |
2.55±0.23 |
5.97±0.28 |
12.19±0.56 |
Neutrophil (%) |
18.5±0.45 |
43.29±0.58 |
77.4±0.59 |
Szegmentált n. (%) |
97.13±0.44 |
96.63±0.56 |
94.13±0.47 |
Stab n. (%) |
2.62±0.41 |
3.12±0.44 |
5.87±0.47 |
Élő n. (%) |
91.53±0.42 |
82.77±0.60 |
70.78±0.87 |
Limphocyta (%) |
14.58±0.48 |
11.58±0.36 |
5.60±0.25 |
Macrophag (%) |
66.92±0.68 |
45.13±0.62 |
17.00±0.63 |
Phagocytáló aktivitás |
0.45±0.01 |
0.37±0.01 |
0.34±0.01 |
3. táblázat (Alhussien és mtsai, 2015) |
|||
Az eredmények a mastitis során a tejben és vérben jellemző sejtszám változásokra mutatnak rá. Az SCC-szint mérése mellett leginkább tehát a neutophil granulocyták arányának és egyéb tényezőinek a vizsgálatával meg tudjuk határozni az állat állapotát és a gyulladás típusát.
Escherichia coli
Az E. coli baktériumból a sejtfal károsodása esetén a szövetközbe kijutó nagyszámú endotoxinok a következő 12-24 órában a legsúlyosabb esetekben az állat elpusztulását okozhatják. Egyéb esetekben magas láz és a keringési rendszer állapotának romlása miatti alacsony vérnyomás léphet fel. A tünetek közé tartozik még a csökkent tejhozam, a tej magasabb SCC szintje a fiziológiásnál, vörösség, illetve a testhőmérséklet emelkedése. Egyes esetekben a csecsbimbó endothelium rétegének sérülése következményében fehár alvadék is jelentkezik. Az összes esetben az érintett tőgynegyed melegsége, duzzadtsága figyelhető meg.
T-lymphocyta-k mennyiségének változása Staphylococcus és Streptococcus Mastitis esetén
Staphylococcus, illetve Streptococcus Mastitis esetén különböző T-lymphocyta típusok szaporodnak el nagy mennyiségben - derült ki egy amerikai kutatás során, melyen egészséges és fertőzött tehenek tőgyéből származó vér- és tejmintákat hasonlítottak össze.
A Staphylococcus-szal vagy Streptococcus-szal fertőződött tehenek vérében a γ-δ T-lymphocyták mennyiségének jelentős növekedése figyelhető meg, míg a tejükben a kb. 75%-kal nő a α-β T-lymphocyta-k száma és 100%-kal a γ-δ T-lymphocyta-k száma. Jelentős különbség van azonban az α-β T-lymphocyta-k mennyiségének emelkedésében Staphylococcus, illetve Streptococcus Mastitis esetén. Staphylococcus Mastitis esetén a CD4+ T-sejteknek, míg Streptococcus Mastitis esetén a CD4+, illetve a CD8+ T-sejteknek köszönhető a gyarapodás. A γ-δ T-lymphocyta-knál nem beszélhetünk ilyesfajta eltérésről. A γ-δ T-lymphycyta-k számának a növekedése mind Staphylococcus, mind Streptococcus Mastitis esetén a GD3.1+ T-sejteknek köszönhető, míg a GD197+ T-sejtek száma nem változik. (Soltys és Quinn, 1999)
Források
König, H. E.; Liebich, H. G.: Veterinary Anatomy of Domestic Mammals: Textbook and Colour Atlas 4th Edition (2004, Schattauer Verlag)
Fehér, Gy.: A háziállatok funkcionális anatómiája 3. (2006, Mezőgazda Kiadó)
Röhlich, P.: Szövettan (2006, Semmelweis Kiadó és Multimédia Stúdió)
Sordillo, L. M; Streicher, K. L.: Mammary Gland Immunity and Mastitis Susceptibility. Journal of Mammary Gland Biology and Neoplasia, 7: (2) 135-146.
Hoesel, B.; Schmid, J. (2013): The complexity of NF-kappaB signaling in inflammation and cancer. Mol Cancer. 2013;12:86. doi: 10.1186/1476-4598-12-86:http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3750319/
Soltys, J.; Quinn, M. T. (1999): Selective Recruitment of T-cells Subsets to the Udder during Staphylococcal and Streptococcal Mastitis: Analysis of Lymphocyte Subsets and Adhesion Molecule Expression. Infection and Immunity 67: (12) 6293-6302 http://www.ncbi.nlm.nih.gov/pmc/articles/PMC97032/
Bharti, P.; Bhakat, P.; Pankaj, P. K.; Bhat, S. A.; Prakash, M. A.; Thul, M. R.; Japheth, K. P. (2015): Relationship of udder and teat conformation with intra-mammary infection in crossbred cows under hot-humid climate. Veterinary World 8: (7) 898-901 http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4774684/
Tozato, C. C. et al. Braz J Microbiol. (2013): Teat papillomatosis associated with bovine papillomavirus types 6, 7, 9, and 10 in dairy cattle from Brazil. Brazilian journal of microbiology, 2013 Dec 10;44(3):905-9.:https://www.ncbi.nlm.nih.gov/pubmed/24516429
Campo, M. S. (2002): Animal models of papillomavirus pathogenesis. Virus research, 2002 Nov;89(2):249-61.:http://www.ncbi.nlm.nih.gov/pubmed/12445664
Della Libera, A. M. M. P., et al (2015): Effects of bovine leukemia virus infection on milk neutrophil function and the milk lymphocyte profile. Vet Res. 2015; 46(1): 2.:http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4297435/
Gillet, N. et al (2007): Mechanisms of leukomogenesis induced by bovine leukemia virus: prospects for novel anti-retroviral therapies in human. Retrovirology. 4:18. doi: 10.1186/1742-4690-4-18.:http://www.ncbi.nlm.nih.gov/pmc/articles/PMC1839114/
Günther, J.; Koy, M.; Berthold, A.; Schuberth, H. J.; Seyfert, H. M. (2016): Comparison of the pathogen species-specific immune response in udder derived cell types and their models. Vet Res. 2016; 47: 22. :https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4736154/
Alhussien, M.; Kaur, M.; Manjari, P.; Kimothi, S. P.; Mohanty, A. K.; Dang, A. K. (2015): A comparative study on the blood and milk cell counts of healthy, subclinical, and clinical mastitis Karan Fries cows. Vet World. 2015 May; 8(5): 685–689.:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4774734/
Santman-Berends, I. M.; Hage, J. J.; Lam, T. J.; Sampimon, O. C.; van Schaik, G. (2011): The effect of bluetongue virus serotype 8 on milk production and somatic cell count in Dutch dairy cows in 2008. Journal of Dairy Science 94: (3) 1347-1354 http://www.journalofdairyscience.org/article/S0022-0302(11)00089-0/fulltext
Griesbeck-Zilch, B.; Osman, M.; Kühn, Ch.; Schwerin, M.; Bruckmaier, R. H.; Pfaffl, M. W.; Hammerle-Fickinger, A.; Meyer, H. H. D.; Wellnitz, O. (2009): Analysis of key molecules of the innate immune system in mammary epithelial cells isolated from marker-assisted and conventionally selected cattle. Journal of Dairy Science, 92: (9) 4621-4633. http://www.journalofdairyscience.org/article/S0022-0302(09)70789-1/fulltext
Burvenich, C.; Bannerman, D. D.; Lippolis, J. D.; Peelman, L.; Nonnecke, B. J.; Kehrli Jr., M. E.; Paape, M. J. (2007):Cumulative Physiological Events Influence the Inflammatory Response of the Bovine Udder to Escherichia coli Infections During the Transition Period. Journal of Dairy Science, 90: E39-E54: http://www.journalofdairyscience.org/article/S0022-0302(07)72059-3/fulltext